
- •Раздел 1
- •Занятие 1
- •Цель занятия
- •Карбонаты щелочных металлов
- •Отделение ионов аммония
- •Действие щелочей и аммиака
- •Оксалат аммония
- •Родизонат натрия (или калия)
- •Занятие 2
- •Цель занятия
- •1. На чем основано разделение катионов согласно кислотно-основной классификации?
- •2. В какой строке перечислены все групповые реагенты, используемые в кислотно-основной схеме анализа?
- •Цель занятия
- •Цель занятия
- •Салициловая кислота (сульфосалициловая кислота)
- •Цель занятия
- •1. В растворе присутствуют hCl (0,1 моль/л) и h3bo3 (0,01 моль/л). Что можно сказать о рН данного раствора?
- •Действие щелочей
- •Действие щелочей
- •Действие щелочей
- •Гексацианоферрат (II) калия
- •Цель занятия
- •1. Что из перечисленного ниже верно? Гидроксиды алюминия, цинка, хрома (III) растворимы в:
- •5. Найдите ряд, в котором содержится больше всего катионов, выпадающих в осадок в виде гидроксидов и оксосолей при обработке анализируемого раствора избытком 6 м NaOh и 6 м nh3.
- •Цель занятия
- •5. Обнаружение анионов scn- и I-
- •Цель занятия
- •Занятие 9
- •Цель занятия
- •1. В насыщенном водном растворе какого из перечисленных ниже веществ равновесная концентрация ионов металла будет наименьшей (в скобках приведены значения ks)?
- •Занятие 10
- •Цель занятия
- •1. Какие из перечисленных ниже процессов невозможны (дайте ответ, не проводя расчётов)?
- •2. Какая из частиц, выделенных полужирным шрифтом, является самым сильным окислителем?
- •3. Какая из частиц, выделенных полужирным шрифтом, является самым сильным восстановителем?
- •7. Какой из малорастворимых электролитов, формулы которых приведены ниже, обладает самым малым произведением растворимости?
- •9. Вывод об отсутствии какого ряда анионов можно сделать, если известно, что при добавлении к анализируемому раствору разбавленного раствора сильной кислоты не происходит выделения пузырьков газа?
- •10. При добавлении к анализируемому раствору ki в кислой среде не происходит появления бурой окраски вследствие выделения иода. Все анионы какого ряда можно не искать при дальнейшем анализе?
- •Занятие 11
- •Цель занятия
- •Предварительные испытания
- •Занятие 12
- •Цель занятия
- •4. Какой из приведенных ниже графиков отражает зависимость константы распределения предельных монокарбоновых кислот между хлороформом и водой в зависимости от числа атомов углерода в молекуле кислоты?
- •2. Экстракция диметилглиоксиматов никеля и кобальта
- •3. Экстракция соединения комплексного аниона [SbCl6]- с малахитовым зеленым
- •4. Экстракционное разделение I- и Br-
- •5. Экстракция ионного ассоциата берберина с трихлорацетат-анионом
- •6. Экстракция ионного ассоциата димедрола с метиловым оранжевым
- •Раздел 2
Действие щелочей
Cd2+ + 2OH- Cd(OH)2
белый
Осадок растворим в кислотах.
2. Аммиак
Cd2+ + 2NH3 + 2H2O Cd(OH)2 + 2NH4+
При дальнейшем добавлении аммиака осадок растворяется:
Cd(OH)2 + 4NH3 [Cd(NH3)4]2+ + 2OH-
бесцветный
Гексацианоферрат (II) калия
2Cd2+ + [Fe(CN)6]4- Cd2[Fe(CN)6]
белый аморфный
4. Сульфид натрия
Cd2+ + S2- CdS
лимонно-жёлтый или оранжевый
Осадок растворяется при нагревании в минеральных кислотах.
3CdS + 2NO3- + 8H+ 3Cd2+ + 2NO + 3S + 4H2O
CdS + 2H+ + 4Cl- [CdCl4]2- + H2S
Реакции ионов Hg2+
1. Действие щелочей
Hg2+ + 2OH- HgO + H2O
жёлтый
2. Аммиак
HgCl2 + 2NH3 [H2NHg]Cl + NH4+ + Cl-
белый
Образующийся осадок растворим в кислотах
3. Иодид калия
Hg2+ + 2I- HgI2
оранжево-красный
Осадок растворим в избытке реагента
HgI2 + 2I- [HgI4]2-
бесцветный
При добавлении к полученному раствору аммиака выпадает красно-бурый осадок (см. реакции ионов NH4+).
1. В пробирку вносят 3-4 капли раствора соли Hg2+ и 1-2 капли раствора KI, а затем раствор KI добавляют по каплям до растворения образовавшегося осадка. К бесцветному раствору добавляют 1 каплю раствора NH3.
2. На фильтровальную бумажку наносят по 1 капле растворов соли Hg2+ и KI, а затем по каплям добавляют раствор KI до исчезновения окраски.
4. Сульфид натрия
Hg2+ + S2- HgS
чёрный
Образующийся осадок нерастворим в кислотах.
5. Дифенилкарбазид
H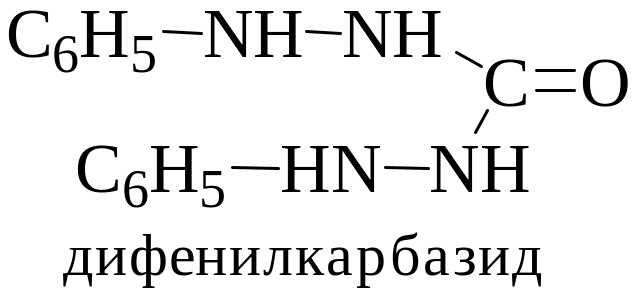 g2+
+ 2HДФК
Hg(ДФК)2
+ 2Н+
g2+
+ 2HДФК
Hg(ДФК)2
+ 2Н+
синий (фиолетовый)
Реакцию следует проводить при рН 1-3. Для создания рН используют HNO3 (добавлять HCl нельзя, так как образующийся HgCl2 не реагирует с дифенилкарбазидом).
На фильтровальную бумажку наносят по 1 капле растворов соли Hg2+, HNO3 и дифенилкарбазида.
6. Хромат калия
Hg2+ + CrO42- HgCrO4
жёлтый
При стоянии осадок краснеет (из-за образования основной соли).
7. Восстановление Hg2+ до металлической ртути
Hg2+ + Cu Hg + Cu2+
серебристый налёт
На медную пластинку наносят 1-2 капли раствора соли Hg2+ и 1 каплю раствора HNO3. Через несколько минут растворы удаляют (с помощью фильтровальной бумажки) и поверхность пластинки вытирают досуха.
ЗАНЯТИЕ 6
Цель занятия
Знать
общую характеристику химико-аналитических свойств, систематический и дробный анализ катионов IV - VI аналитических групп.
Уметь
выполнять анализ смеси катионов IV - VI аналитических групп.
Общая характеристика, систематический и дробный анализ катионов IV аналитической группы.
Общая характеристика, систематический и дробный анализ катионов V аналитической группы.
Общая характеристика, систематический и дробный анализ катионов VI аналитической группы.
Вывод об отсутствии каких катионов IV – VI аналитических групп можно сделать в том случае, если исследуемый раствор а) неокрашен; б) имеет рН 5.
Какие представители IV – VI аналитических групп могут находиться в исследуемом растворе, если он имеет сильнощелочную среду и не пахнет аммиаком?
Почему при добавлении концентрированного раствора NH4Cl к раствору, содержащему ионы [Al(OH)4]-, CrO42- и [Zn(OH)4]2- в осадок выпадает только Al(OH)3?
Почему раздельное обнаружение Fe2+ и Fe3+ проводят в предварительных испытаниях?
В каком порядке проводят растворение смеси Fe(OH)3, MnO(OH)2, Mg(OH)2 и почему?
Какое различие в химических свойствах SbOCl, SbO2Cl и BiOCl используется для разделения смеси ионов Sb3+, Sb(V) и Bi3+?
Каким образом отделяют Cu2+ от Ni2+ и Cd2+ согласно схеме кислотно-основного систематического анализа?
Какие катионы IV аналитической группы, также как и катионы VI аналитической группы, образуют хорошо растворимые в воде аммиакаты?
Каким образом можно обнаружить ион Co2+ в присутствии иона Fe3+?
Предложите возможный ход анализа растворов, содержащих следующие смеси катионов: а) Zn2+, Fe3+, Cd2+; б) Al3+, Mn2+, Cu2+; в) Cr3+, Hg2+, Mg2+.
