
- •2. Спектроскопические и другие оптические методы анализа
- •2.1. Основные характеристики электромагнитного излучения
- •2.2. Принципы аналитической оптической спектроскопии
- •2.3. Параметры спектральной полосы и использование спектров для химического анализа
- •2.4. Приборы для оптического спектрального анализа
- •2.4.1.Спектральные приборы и их основные характеристики
- •2.4.2. Приемники излучения
- •2.5. Атомно-эмиссионная спектроскопия
- •Виды атомизаторов
- •2.6. Атомно-адсорбционный спектральный анализ
- •2.7. Фотометрия растворов
- •Основные методы определения концентрации
- •Растворы сравнения (нулевые)
- •Отклонения от основного закона светопоглощения
- •Фотоколориметрическое титрование
- •2.8. Метод инфракрасной спектроскопии
- •2.9. Люминесцентный анализ
- •2.10. Рефрактометрический анализ
- •2.11. Поляриметрический метод анализа
- •2.12. Нефелометрия и турбидиметрия
2.6. Атомно-адсорбционный спектральный анализ
Атомно-абсорбционная спектроскопия – это аналитический метод обнаружения элементов, основанный на поглощении излучения свободными (невозбужденными) атомами.
Если на невозбужденный атом направить излучение с частотой, равной частоте резонансного перехода (т. е. перехода на уровень, ближайший к основному энергетическому состоянию), кванты света будут поглощаться атомами и интенсивность излучения будет уменьшаться. Таким образом, если в эмиссионной спектроскопии концентрация вещества связывалась с интенсивностью излучения, которое было прямо пропорционально числу возбужденных атомов, то в атомно-абсорбционной спектроскопии аналитический сигнал (уменьшение интенсивности излучения) связан с числом невозбужденных атомов.
Расчеты показывают, что число атомов в возбужденном состоянии незначительно по сравнению с числом атомов на основном (нижнем) уровне и не превышает 1-2 % от общего числа атомов. Это выгодно отличает атомно-абсорбционный анализ от эмиссионного, так как при прочих равных условиях величина аналитического сигнала оказывается связанной с большим числом атомов, чем в эмиссионной спектроскопии.
Существенно также, что число линий в спектре в условиях атомно-абсорбционного анализа невелико, поэтому наложения аналитических линий практически не происходит, хотя неселективное поглощение остается значительным.
Методики атомно-абсорбционного определения разработаны более чем для 70 элементов. Предел обнаружения с помощью этого метода составляет 10-5 – 10-6 мкг/мл.
Метод имеет также ряд ограничений. Так, не определяются элементы, резонансные линии которых лежат в далеком ультрафиолете(углерод, фосфор, галогены и др.). Недостатком является и невозможность одновременного определения нескольких элементов.
2.7. Фотометрия растворов
Растворы многих веществ имеют характерную окраску, обусловленную избирательным поглощением света ионами или молекулами. Например, окрашены комплексы [Fe(SCN)] 2+, [Cu(NH3)4] 2+ , ионы Cu2+, Ni2+, Co2+, Fe3+, Cr3+, CrO42-, MnO-4, органические соединения различных металлов.
Измеряя светопоглощение окрашенного раствора или сравнивая полученную окраску с окраской раствора известной концентрации, определяют содержание окрашенного вещества в анализируемом растворе.
Зависимость между интенсивностью окраски раствора и содержанием в нем окрашенного вещества описывается законом Бугера-Ламберта-Бера (основной закон светопоглощения):
I=I0∙10-εlc, или I/I0=10-εlc, где
I-интенсивность света, прошедшего через раствор;
I0-интенсивность падающего света;
ε- молярный коэффициент светопоглощения;
l-толщина слоя раствора, см;
с-концентрация раствора, моль/л.
Уменьшение интенсивности света, прошедшего через раствор, характеризуется коэффициентом пропускания (или просто пропусканием) Т:
Т= I/I0.
Взятый с обратным знаком логарифм Т называется оптической плотностью А:
А = –lg Т = – lg I/I0 = lg I0/I,
то есть оптическая плотность раствора прямо пропорциональна концентрации:
А= ε∙l∙c
Оптическая плотность раствора, содержащего несколько окрашенных веществ обладает свойством аддитивности, которое иногда называют законом аддитивности светопоглощения. В соответствии с этим законом поглощение света каким-либо веществом не зависит от присутствия в растворе других веществ. При наличии в растворе нескольких окрашенных веществ каждое из них будет давать свой аддитивный вклад в экспериментально определяемую оптическую плотность А:
А=А1+А2+…+Аn, где
А1, А2 и т.д.- оптическая плотность вещества 1, вещества 2 и т.д.
С учетом этого:
А= l ∙ (ε1c1+ ε2c2+…+ εncn)
Молярный коэффициент светопоглощения ε зависит от природы вещества, температуры и длины волны падающего света.
Интенсивность окраски при фотометрировании можно оценить визуально. Готовят серию растворов данного окрашенного соединения и помещают в одинаковые сосуды. В такой же сосуд вносят испытуемый раствор и сравнивают его окраску с более подходящим стандартным раствором известной концентрации. Однако визуальная фотометрия (ее называют метод стандартных серий) недостаточно надежна, поскольку результат зависит от субъективных особенностей наблюдателя.
Более объективно оценивается интенсивность окраски с помощью фотоколориметрического метода, в котором применяется прибор -фотоэлектроколориметр. В этом приборе (рис.2.4.) от источника (1) проходит через светофильтр (2) конденсорные линзы (3), кювету с раствором анализируемого вещества (4), светокомпенсирующий клин (5) и попадает на фотоэлемент (6).
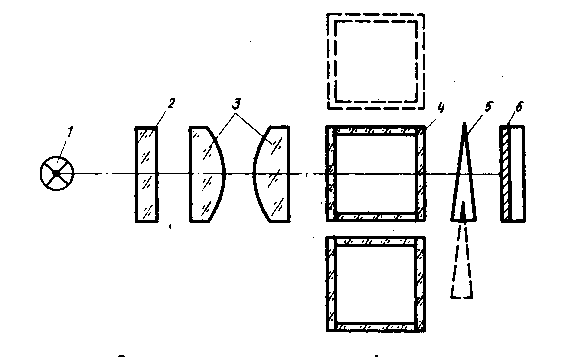
Рис. 2.4. Блок-схема фотоэлектроколориметра
В фотоэлементе слой полупроводника (AgS, Se, ZnSe) нанесен на металлическую пластинку. Световой поток, попадая на фотоэлемент, возбуждает электрический ток, сила которого определенным образом зависит от интенсивности освещения. Таким образом, непосредственное наблюдение окраски заменяется показаниями гальванометра.
Для увеличения чувствительности и точности фотометрического определения стремятся использовать поглощение не смешанного (белого) цвета, а лишь тех лучей, которые максимально поглощаются окрашенным раствором. Чтобы из всей видимой области спектра выделить лучи определенных длин волн, на пути световых потоков перед поглощающими растворами помещают избирательные поглотители света – светофильтры. Они пропускают лишь в определенном интервале длин волн и практически полностью поглощают лучи других длин волн.
