
- •1 Билет.
- •4 Билет
- •Магнитное поле в веществе
- •5 Билет
- •Вывод основного уравнения мкт
- •Закон Био́—Савара—Лапла́са Для тока текущего по контуру (тонкому проводнику)
- •Для распределенных токов
- •Следствия
- •6 Билет Распределение по вектору скорости
- •Распределение по проекции скорости
- •Распределение по модулю скоростей
- •[Править]в магнитостатике
- •[Править]в общем случае
- •Формула момента рычага
- •[Править]Сила под углом
- •[Править]Статическое равновесие
- •[Править]Момент силы как функция от времени
- •Движение заряженных частиц в магнитном поле
- •Законы — начала термодинамики
Законы — начала термодинамики
Традиционно считается, что термодинамика основывается на четырёх законах (началах), которые сформулированы на основе экспериментальных данных и поэтому могут быть приняты как постулаты.
* 0-й закон — нулевое начало термодинамики: Постулирует существование термодинамического равновесия и вводит понятие абсолютной температуры.
Термодинамическое
равновесие. Для
каждой изолированной термодинамической
системы существует состояние
термодинамического равновесия, которого
она при фиксированных внешних условиях
с течением времени самопроизвольно
достигает. Если две изолированные
системы
и
приведены
в контакт друг с другом, то после
достижения термодинамического равновесия
полной системой ![]() системы
и
находятся
в состоянии теплового (термического)
равновесия друг с другом. При этом каждая
из систем
и
в
отдельности также находится в состоянии
термодинамического равновесия. Это
равновесие не нарушится, если устранить
контакт между системами, а затем
восстановить его. Следовательно, если
установление контакта между двумя
системами
и
,
которые до этого были изолированными,
не приводит ни к каким изменениям, то
эти системы находятся в тепловом
равновесии друг с другом.
системы
и
находятся
в состоянии теплового (термического)
равновесия друг с другом. При этом каждая
из систем
и
в
отдельности также находится в состоянии
термодинамического равновесия. Это
равновесие не нарушится, если устранить
контакт между системами, а затем
восстановить его. Следовательно, если
установление контакта между двумя
системами
и
,
которые до этого были изолированными,
не приводит ни к каким изменениям, то
эти системы находятся в тепловом
равновесии друг с другом.
Закон
транзитивности теплового равновесия. Если
системы
и
находятся
в тепловом равновесии и системы
и ![]() находятся
в тепловом равновесии, то системы
и
также
находятся в тепловом равновесии между
собой. На основании этого закона делается
вывод о существовании абсолютной
температуры как термодинамического
параметра, обладающего свойствами
эмпирической температуры, но не зависящего
от способа её измерения. Равенство
температур есть условие теплового
равновесия систем (или частей одной и
той же системы).
находятся
в тепловом равновесии, то системы
и
также
находятся в тепловом равновесии между
собой. На основании этого закона делается
вывод о существовании абсолютной
температуры как термодинамического
параметра, обладающего свойствами
эмпирической температуры, но не зависящего
от способа её измерения. Равенство
температур есть условие теплового
равновесия систем (или частей одной и
той же системы).
* 1-й закон — первое начало термодинамики: Представляет собой формулировку обобщённого закона сохранения энергии для термодинамических процессов. В наиболее простой форме его можно записать как
![]() ,
,
где есть полный дифференциал внутренней энергии системы, а и есть элементарное количество теплоты, переданное системе, и элементарная работа, совершенная системой соответственно. Нужно учитывать, что и нельзя считать дифференциалами в обычном смысле этого понятия, поскольку эти величины существенно зависят от типа процесса, в результате которого состояние системы изменилось.
В
литературе можно встретить и другие
варианты приведённого выше соотношения,
отличающиеся от него знаками (![]() или
или ![]() )
перед
и
.
Отличия вызваны тем, что конкретный вид
этого уравнения зависит от соглашений,
называемых «правилами знаков для работы
и теплоты». Выше использовано
«теплотехническое правило знаков для
работы» (положительной считают работу,
совершаемую системой, когда она отдаёт
энергию, а отрицательной — работу,
совершаемую над системой, когда она
получает энергию) и «термодинамическое
правило знаков для теплоты» (положительной
считают теплоту, получаемую системой,
а отрицательной — теплоту, отдаваемую
системой). В «термодинамическом правиле
знаков для работы» положительной считают
работу, совершаемую над системой, а
отрицательной — работу, совершаемую
системой. Наконец, в «термохимическом
правиле знаков для теплоты» положительной
считают теплоту, отдаваемую системой,
а отрицательной — теплоту, получаемую
системой. Мнемоническое правило: в
термодинамической системе знаков
имеет
тот же знак, что и энергия, передаваемая
системе в виде работы или теплоты; в
остальных случаях знак
противоположен
знаку передаваемой энергии. Стандарта,
предписывающего использовать конкретный
набор правил знаков, не существует, так
что уместно рассматривать только степень
распространённости того или иного
правила в научной и учебной литературе.
По этому поводу однозначно можно говорить
лишь о том, что в современной литературе
предпочитают использовать термодинамическое,
а не термохимическое правило знаков
для теплоты.
)
перед
и
.
Отличия вызваны тем, что конкретный вид
этого уравнения зависит от соглашений,
называемых «правилами знаков для работы
и теплоты». Выше использовано
«теплотехническое правило знаков для
работы» (положительной считают работу,
совершаемую системой, когда она отдаёт
энергию, а отрицательной — работу,
совершаемую над системой, когда она
получает энергию) и «термодинамическое
правило знаков для теплоты» (положительной
считают теплоту, получаемую системой,
а отрицательной — теплоту, отдаваемую
системой). В «термодинамическом правиле
знаков для работы» положительной считают
работу, совершаемую над системой, а
отрицательной — работу, совершаемую
системой. Наконец, в «термохимическом
правиле знаков для теплоты» положительной
считают теплоту, отдаваемую системой,
а отрицательной — теплоту, получаемую
системой. Мнемоническое правило: в
термодинамической системе знаков
имеет
тот же знак, что и энергия, передаваемая
системе в виде работы или теплоты; в
остальных случаях знак
противоположен
знаку передаваемой энергии. Стандарта,
предписывающего использовать конкретный
набор правил знаков, не существует, так
что уместно рассматривать только степень
распространённости того или иного
правила в научной и учебной литературе.
По этому поводу однозначно можно говорить
лишь о том, что в современной литературе
предпочитают использовать термодинамическое,
а не термохимическое правило знаков
для теплоты.
Иногда в рассматриваемое выражение для первого начала наряду с работой и теплотой включают ещё и работу переноса массы (химическую работу), выделяя её из общего выражения для работы в отдельное слагаемое.
* 2-й закон — второе начало термодинамики: Второй закон термодинамики исключает возможность создания вечного двигателя второго рода. Имеется несколько различных, но в то же время эквивалентных формулировок этого закона.
1 — Постулат Клаузиуса. Процесс, при котором не происходит других изменений, кроме передачи теплоты от горячего тела к холодному, является необратимым, то есть теплота не может перейти от холодного тела к горячему без каких-либо других изменений в системе. Это явление называют рассеиванием или диссипацией энергии.
Приведем
второе начало термодинамики в ещё одной
формулировке Рудольфа
Юлиуса Клаузиуса (1865):
для любой квазиравновесной термодинамической
системы существует однозначная функция
термодинамического состояния ![]() ,
называемая энтропией, такая, что ее
полный дифференциал
,
называемая энтропией, такая, что ее
полный дифференциал ![]() . [3]
. [3]
2 — Постулат Кельвина. Процесс, при котором работа переходит в теплоту без каких-либо других изменений в системе, является необратимым, то есть невозможно превратить в работу всю теплоту, взятую от источника с однородной температурой, не проводя других изменений в системе.
* 3-й закон — третье начало термодинамики: Теорема Нернста: энтропия любой равновесной системы при абсолютном нуле температуры всегда равна нулю (традиционная формулировка). Здесь важно различать аксиомы, отражающие законы природы, и имеющие исторические корни соглашения, необходимые для построения шкалы измерения соответствующей термодинамической величины. Так, аксиомами являются утверждения, что и энтропия, и температура есть односторонне ограниченные величины, и что своих граничных значений обе величины достигают одновременно. Согласно стандартным соглашениям принято, что и энтропия, и температура ограничены снизу, т. е. не могут быть меньше некоторых предельных значений. Из этого логично вытекают следующие соглашения, согласно которым наименьшее значение энтропии принято равным нулю, а наименьшее (нулевое) значение температуры служит реперной точкой для построения термодинамической шкалы температур.
Диамагне́тики —
вещества, намагничивающиеся против
направления внешнего магнитного
поля.
В отсутствие внешнего магнитного поля
диамагнетики немагнитны. Под действием
внешнего магнитного поля каждый атом
диамагнетика приобретает магнитный
момент I
(а каждый моль вещества —
суммарный магнитный момент), пропорциональный
магнитной индукции H и направленный
навстречу полю. Поэтому магнитная
восприимчивость ![]() =
I/H у диамагнетиков всегда отрицательна.
По абсолютной величине диамагнитная
восприимчивость
мала
и слабо зависит как от напряжённости
магнитного поля, так и от температуры.
=
I/H у диамагнетиков всегда отрицательна.
По абсолютной величине диамагнитная
восприимчивость
мала
и слабо зависит как от напряжённости
магнитного поля, так и от температуры.
Большая
часть двигателей, используемых людьми,
— это тепловые двигатели. Устройства,
превращающие энергию топлива в
механическую энергию, называются
тепловыми двигателями. Любой тепловой
двигатель (паровые и газовые турбины,
двигатели внутреннего сгорания) состоит
из трех основных элементов: рабочего
тела (это газ), которое совершает работу
в двигателе; нагревателя, от которого
рабочее тело получает энергию, часть
которой затем идет на совершение работы;
холодильника, которым является атмосфера
или специальные устройства (рис.
28).
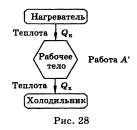 Ни один тепловой двигатель не может
работать при одинаковой температуре
его рабочего тела и окружающей среды.
Обязательно температура нагревателя
больше температуры холодильника. При
совершении работы тепловыми двигателями
происходит передача теплоты от более
горячих тел к более холодным. Рабочее
тело двигателя получает количество
теплоты Qн от нагревателя, совершает
работу А и передает холодильнику
количество теплоты Qx. В соответствии с
законом сохранения энергии
Ни один тепловой двигатель не может
работать при одинаковой температуре
его рабочего тела и окружающей среды.
Обязательно температура нагревателя
больше температуры холодильника. При
совершении работы тепловыми двигателями
происходит передача теплоты от более
горячих тел к более холодным. Рабочее
тело двигателя получает количество
теплоты Qн от нагревателя, совершает
работу А и передает холодильнику
количество теплоты Qx. В соответствии с
законом сохранения энергии ![]() .
В случае равенства речь идет об идеальном
двигателе, в котором нет потерь
энергии.
Отношение работы к энергии, которое
получило рабочее тело от нагревателя,
называют коэффициентом полезного
действия (КПД):
.
В случае равенства речь идет об идеальном
двигателе, в котором нет потерь
энергии.
Отношение работы к энергии, которое
получило рабочее тело от нагревателя,
называют коэффициентом полезного
действия (КПД):
![]() Паровая или газовая турбина, двигатель
внутреннего сгорания, реактивный
двигатель работают на базе ископаемого
топлива. В процессе работы многочисленных
тепловых машин возникают тепловые
потери, которые в конечном счете приводят
к повышению внутренней энергии атмосферы,
т. е. к повышению ее температуры. Это
может привести к таянию ледников и
катастрофическому повышению уровня
Мирового океана, а вместе с тем к
глобальному изменению природных условий.
При работе тепловых установок и двигателей
в атмосферу выбрасываются вредные для
человека, животных и растений оксиды
азота, углерода и серы. С вредными
последствиями работы тепловых машин
можно бороться путем повышения КПД, их
регулировки и создания новых двигателей,
не выбрасывающих вредные вещества с
отработанными газами.
Паровая или газовая турбина, двигатель
внутреннего сгорания, реактивный
двигатель работают на базе ископаемого
топлива. В процессе работы многочисленных
тепловых машин возникают тепловые
потери, которые в конечном счете приводят
к повышению внутренней энергии атмосферы,
т. е. к повышению ее температуры. Это
может привести к таянию ледников и
катастрофическому повышению уровня
Мирового океана, а вместе с тем к
глобальному изменению природных условий.
При работе тепловых установок и двигателей
в атмосферу выбрасываются вредные для
человека, животных и растений оксиды
азота, углерода и серы. С вредными
последствиями работы тепловых машин
можно бороться путем повышения КПД, их
регулировки и создания новых двигателей,
не выбрасывающих вредные вещества с
отработанными газами.
Работа, совершаемая двигателем, равна:
![]() ,
где:
,
где:
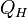 —
количество
теплоты, полученное от нагревателя,
—
количество
теплоты, полученное от нагревателя,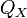 —
количество
теплоты, отданное охладителю.
—
количество
теплоты, отданное охладителю.
Коэффициент
полезного действия (КПД)
теплового двигателя рассчитывается
как отношение работы, совершаемой
двигателем, к количеству теплоты,
полученному от нагревателя: 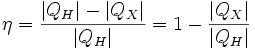
Часть
теплоты при передаче неизбежно теряется,
поэтому КПД двигателя менее 1. Максимально
возможным КПД обладает двигатель
Карно.
КПД двигателя Карно зависит только от
абсолютных температур нагревателя(![]() )
и холодильника(
)
и холодильника(![]() ):
):
![]()
Коэффициент полезного действия (КПД) теплового двигателя.Невозможность полного превращения внутренней энергии газа в работу тепловых двигателей обусловлена необратимостью процессов в природе. Если бы тепло могло самопроизвольно возвращаться от холодильника к нагревателю, то внутренняя энергия могла бы быть полностью превращена в полезную работу с помощью любого теплового двигателя. Согласно закону сохранения энергии работа, совершаемая двигателем, равна:
![]()
где Q1 - количество теплоты, полученное от нагревателя, а Q2 - количество теплоты, отданное холодильнику.
Идеальный двигатель, цикл Карно
Цикл Карно́ — идеальный термодинамический цикл. Тепловая машина Карно, работающая по этому циклу, обладает максимальным КПД из всех машин, у которых максимальная и минимальная температуры осуществляемого цикла совпадают соответственно с максимальной и минимальной температурами цикла Карно. Состоит из 2 адиабатических и 2 изотермических процессов.
Цикл Карно назван в честь французского военного инженера Сади Карно, который впервые его исследовал в 1824 году.
Одним из важных свойств цикла Карно является его обратимость: он может быть проведён как в прямом, так и в обратном направлении, при этомэнтропия адиабатически изолированной (без теплообмена с окружающей средой) системы не меняется.
Пусть тепловая машина состоит из нагревателя с температурой , холодильника с температурой и рабочего тела.
Цикл Карно состоит из четырёх стадий:
Изотермическое расширение (на рисунке — процесс A→Б). В начале процесса рабочее тело имеет температуру , то есть температуру нагревателя. Затем тело приводится в контакт с нагревателем, который изотермически (при постоянной температуре) передаёт ему количество теплоты . При этом объём рабочего тела увеличивается.
Адиабатическое (изоэнтропическое) расширение (на рисунке — процесс Б→В). Рабочее тело отсоединяется от нагревателя и продолжает расширяться без теплообмена с окружающей средой. При этом его температура уменьшается до температуры холодильника.
Изотермическое сжатие (на рисунке — процесс В→Г). Рабочее тело, имеющее к тому времени температуру , приводится в контакт с холодильником и начинает изотермически сжиматься, отдавая холодильнику количество теплоты .
Адиабатическое (изоэнтропическое) сжатие (на рисунке — процесс Г→А). Рабочее тело отсоединяется от холодильника и сжимается без теплообмена с окружающей средой. При этом его температура увеличивается до температуры нагревателя.
При изотермических процессах температура остаётся постоянной, при адиабатических отсутствует теплообмен, а значит, сохраняется энтропия:
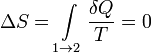 при
при ![]() .
.
Поэтому цикл Карно удобно представить в координатах T и S (температура и энтропия).
Количество теплоты, полученное рабочим телом от нагревателя при изотермическом расширении, равно
![]() .
.
Аналогично, при изотермическом сжатии рабочее тело отдало холодильнику
![]() .
.
Отсюда коэффициент полезного действия тепловой машины Карно равен
![]() .
.
Из последнего выражения видно, что КПД тепловой машины Карно зависит только от температур нагревателя и холодильника. Кроме того, из него следует, что КПД может составлять 100 % только в том случае, если температура холодильника равна абсолютному нулю. Это невозможно, но не из-за недостижимости абсолютного нуля (этот вопрос решается только третьим началом термодинамики, учитывать которое здесь нет необходимости), а из-за того, что такой цикл или нельзя замкнуть, или он вырождается в совокупность двух совпадающих адиабат и изотерм.
Поэтому максимальный КПД любой тепловой машины будет меньше или равен КПД тепловой машины Карно, работающей при тех же температурах нагревателя и холодильника. Например, КПД идеального цикла Стирлинга равен КПД цикла Карно.
Для того, чтобы цикл был обратимым, из него должна быть исключена передача теплоты при наличии разности температур (так как такие процессы необратимы в силу постулата Томсона). Значит, передача теплоты должна осуществляться либо в изотермическом процессе (как в цикле Карно), либо в эквидистантном процессе (обобщённый цикл Карно или, для примера, его частный случай Цикл Брайтона). Для того, чтобы менять температуру рабочего тела от температуры нагревателя до температуры холодильника и обратно, необходимо использовать либо адиабатические процессы (они идут без теплообмена и, значит, не влияют на энтропию), либо циклы с регенерацией тепла при которых нет передачи тепла при разности температур. Мы приходим к выводу, что любой обратимый цикл может быть сведён к циклу Карно.
Примером обратимого цикла, не являющегося циклом Карно, но интегрально совпадающим с ним, является идеальный цикл Стирлинга: вдвигателе Стирлинга добавлен регенератор, обеспечивающий полное приближение цикла к циклу Карно с достижением обратимости и тех же величин КПД.
Если же в цикле возникает передача теплоты при наличии разности температур, а таковыми являются все технические реализации термодинамических циклов, то цикл утрачивает свойство обратимости. Иначе говоря, посредством отведённой в цикле механической работы становится невозможным получить исходную теплоту. КПД такого цикла будет всегда меньше чем КПД цикла Карно.
ЭЛЕКТРИЧЕСКИЙ ПОТОК, величина ЭЛЕКТРИЧЕСКОГО ЗАРЯДА, которая прошла бы по ПРОВОДНИКУ, если его поместить в электрическое поле. Этим же термином обозначают величину заряда, который способен создать такое же электрическое поле. Эта величина пропорциональна силе поля и диэлектрической проницаемости среды, в которой поле создается. Величина электрического потока относительно единицы площади называется плотностью потока или электрической индукцией.
