
Пути обезвреживания аммиака
В результате процессов дезаминирования аминокислот, биогенных аминов, глютамина и аспарагина, пуриновых и пиримидиновых оснований в тканях и действия микрофлоры кишечника образуется аммиак. Аммиак - очень токсичное соединение, особенно для нервных клеток. При накоплении его возникает возбуждение нервной системы. Симптомами аммиачного отравления является своеобразный тремор, нечленораздельная речь, затуманенность зрения, в тяжёлых случаях - коматозное состояние и летальный исход. Поэтому чрезвычайно важным является его обезвреживание. В тканях существуют несколько механизмов, которые могут быть продемонстрированы схемой:
восстановительное образование
аминирование аммонийных солей
 1
2
1
2
NH3
 синтез аминогексаз
синтез аминогексаз
 3
3
 синтез
глутамин
синтез
глутамин
н

 уклеотидов
уклеотидов
4
синтез синтез
заменимых мочевины аммониогенез
аминокислот
из альфа-кетокислот
1. Восстановительное амминирование альфа-кетоглутарата - реакция обратная прямому окислительному дезаминированию глутимановой кислоты протекает по уравнению:

 СООН
СООН
СООН
СООН

 СН2 НАДФН2
НАДФ СН2
СН2 НАДФН2
НАДФ СН2



 CH2+NH3
CH2
CH2+NH3
CH2

 C-O
ГлДГ
CHNH2
C-O
ГлДГ
CHNH2
COOН COOH
альфа-кетоглутарат глу
2. Небольшое количество аммиака взаимодействует с кислотами с образованием аммонийных солей, которые затем выводятся с мочой.
3. Постоянно продуцируясь в тканях, аммиак содержится в крови в следовых количествах прежде всего благодаря образованию глютамина (аспарагина), которое протекает следующим образом:
COOH CONH2
(СН2)2 АТФ АДФ+Фн (СН2)2
C HNH2+NH3
CHNH2
HNH2+NH3
CHNH2
глутамин-
СООН синтетаза СООН
глу глн
Реакция активно протекает в нервной, мышечной тканях, в почках. Глютамин (аспарагин) - коллектор аммиака, своеобразная транспортная форма его. Все дальнейшие превращения аммиака связаны с глютамином, вернее, с NH2 - группой глютамина.
4.
Основной путь обезвреживания аммиака - синтез мочевины.
Синтез мочевины
Мочевина - главный конечный продукт обмена белков. Принято считать, что мочевина в 18 раз менее токсична, чем аммиак.
Ещё в прошлом веке русские учёные М.В. Ненцкий и С.С. Салазкин показали, что в печени происходит образование мочевины из аммиака и углекислоты. Г. Кребс и К. Гензенлейт установили, что синтез мочевины представляет собой циклический процесс, в котором каталитическую роль играет орнитин. Г. Коен и С. Ратнер выяснили, что начальной реакцией этого цикла является синтез карбомаил-фосфата. Главным местом образования мочевины является печень, где есть все ферменты мочевинообразования. В головном мозге имеются все ферменты синтеза мочевины, кроме первого, поэтому в нём мочевина не образуется. Считают, что автономный синтез мочевины имеет место в миокарде. Растворимость её безгранична, поэтому она может выводиться в большом количестве с мочой.
Как же синтезируется мочевина?
Начинается синтез с образования высокоэргическогосоединения - карбомаилфосфата. Реакция требует энергии АТФ, катализируется ферментом карбомаилфосфатсинтазой, аллостерическим регулятором которой является N-ацетилглутамат. Протекает реакция в митохондриях по уравнению:
карбомаил
1 .
NH3 + “СО2” + 2АТФ + Н2О
NH2-СО-О~Р + 2АДФ + ФН
.
NH3 + “СО2” + 2АТФ + Н2О
NH2-СО-О~Р + 2АДФ + ФН
фосфатсинтаза,
Mg+2
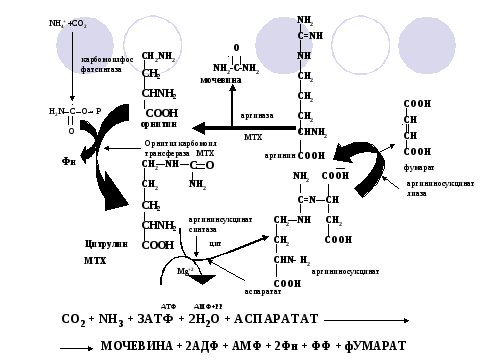
2. Карбомаилфосфат взаимодействует с орнитином и начинается орнитиновый цикл мочевинообразования.
3. Цитрулин выходит из митохондрий в цитоплазму, где вступает в реакцию конденсации с L-аспарагиновой кислотой. Эта реакция связана с затратой энергии АТФ.
4. Аргининосукцинат подвергается ферментативному расщиплению аргининосукцинат-лиазой на аргинин и фумаровую кислоту.
5. Аргинин далее гидролитически расщепляется аргиназой на мочевину и ортинин:
Орнитин снова вступает в реакции орнитинового цикла. Таким образом , образование мочевины представляет собой циклический процесс. Общая схема орнитинового цикла:
Суммарная реакция:
N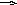 H3+СО2+3АТФ+2Н2О+аспартатмочевиа+2АДФ+АМФ+2Фн+РР+фумарат
H3+СО2+3АТФ+2Н2О+аспартатмочевиа+2АДФ+АМФ+2Фн+РР+фумарат
Фумаровая кислота, образовавшаяся в орнитиновом цикле, превращается в малат (яблочную кислоту) в цикле трикарбоновых кислот, затем окисляется в оксалоацетат под действием малатдегидрогеназы. Оксалоацетат, вступая в реакцию трансаминирования с глутаминовой кислотой, превращается в аспарагиновую кислоту, которая может включаться в орнитиновый цикл.
Два цикла: цикл трикарбоновых кислот и орнитиновый цикл тесно связаны не только именем учёного Г. Кребса, раскрывшего их механизмы - “двухколёсный велосипед” Кребса, но и общими метаболитами.
Такими метаболитами являются: углекислый газ, АТФ, которые, образуясь в цикле трикарбоновых кислот, используются в орнитиновом цикле; фумаровая кислота, которая с участием ферментов цикла трикарбоновых кислот и аспартатаминотрансферазы (см. выше) превращается в аспартат, необходимый в орнитиновом цикле.
