
- •Раздел I. Механика. Молекулярная физика. Термодинамика 16 глава 1. Законы динамики ньютона. Законы сохранения 16
- •Вопросы и задачи к главе I. 33 глава 2. Молекулярно-кинетическая теория газов
- •Глава 3. Применение первого начала термодинамики к процессам в идеальном газе 52
- •Глава 4. Реальные газы 74
- •Вопросы и задачи и вопросы к главе 4. 82 глава 5. Поверхностное натяжение жидкости 82
- •Вопросы и задачи к главе 5 102
- •Глава 6. Вязкость жидкости 103
- •Вопросы и задачи к главе 6 116
- •Глава 7. Твёрдые и жидкие кристаллы. Стеклообразное состояние вещества. Полимеры 117
- •Глава 8. Процессы переноса 127
- •Раздел II колебания и волны 135
- •Глава 1. Механические колебания 135
- •Вопросы и задачи к главе 1. 153
- •Глава 2. Механические волны 153
- •Вопросы задачи к главе 2. 158
- •Глава 3. Звук 159
- •Вопросы и задачи к главе 3. 167
- •Глава 4. Ультразвук. Его применение в медицине. Инфразвук
- •Вопросы задачи к главе 4 180
- •Глава 5. Электромагнитные колебания и волны 181
- •Вопросы задачи к главе 5 201 глава 6. Оптика 201
- •Вопросы задачи к главе 6 251
- •Раздел III. Атомная, ядерная и квантовая физика
- •Глава 1. Тепловое излучение тел 253
- •Глава 2. Рентгеновское излучение 261
- •Глава 3. Радиоактивность 272
- •Глава 4. Дозиметрия ионизирующих излучений 282
- •Раздел IV. Биофизика 337 глава1 молекулярная биофизика 337
- •Глава 2. Биологические мембраны. 358
- •Глава 3. Термодинамика биологических систем 386
- •Глава 4. Транспорт веществ через биологические мембраны
- •Глава 5. Биопотенциалы 416
- •Глава 6. Биофизика нервного импульса 427
- •Глава 7. Моделирование биологических процессов 446
- •Введение
- •Раздел I механика. Молекулярная физика. Термодинамика.
- •Глава 1 законы динамики ньютона. Законы сохранения.
- •1.1. Законы ньютона. Основные дифференциальные уравнения движения.
- •Здесь аx , аy , аz - проекции вектора ускорения на оси координат X , y и z;
- •1. 2. Законы сохранения импульса и энергии
- •. Задача о центральном ударе шаров: абсолютно упругом и абсолютно неупругом.
- •1.4 Физические основы центрифугирования
- •Глава 2. Молекулярно-кинетическая теория газов
- •2.1 Отличия молекулярной структуры газов, жидкостей и твёрдых тел. Характер молекулярного движения в различных состояниях вещества. Аморфные и кристаллические жидкости и твёрдые тела
- •Примечание 2
- •2.2 Основное уравнение молекулярно-кинетической теории газов. Средняя квадратическая скорость молекул газа.
- •2.3 Средняя кинетическая энергия поступательного движения молекул газа. Распределение энергии по степеням свободы. Внутренняя энергия идеального газа
- •2.4 Распределение Максвелла молекул идеального газа по абсолютным значениям их скоростей.
- •2.5 Распределение Больцмана по потенциальным энергиям молекул идеального газа. Барометрическая формула Больцмана.
- •Глава 3. Применение первого начала термодинамики к процессам в идеальном газе.
- •3.1. Особенности термодинамического метода. Первое начало термодинамики.
- •3.2. Применение первого начала термодинамики к равновесным изопроцессам идеального газа
- •Работа газа при его расширении
- •Теплоёмкость
- •Политропные процессы - процессы с постоянной теплоёмкостью.
- •Глава 4. Реальные газы
- •4.1.Уравнение состояния реального газа Ван - дер - Ваальса и изотермы Ван- дер - Ваальса.
- •4.2. Изотермы Эндрюса
- •Сжижение газов. Получение низких температур.
- •Глава 5. Поверхностное натяжение жидкости
- •5.3 Поверхностные явления на границе твёрдой, жидкой и газообразной фазы. Краевой угол смачивания. Смачивание и несмачивание твёрдой поверхности жидкостью.
- •5.4 Давление Лапласа. Капиллярные явления.
- •5.5 Методы определения коэффициента поверхностного натяжения
- •1. Метод отрыва капель
- •2. Метод отрыва кольца
- •Глава 6. Вязкость жидкости
- •6.1 Вязкость жидкости. Закон ньютона. Ньютоновские и неньютоновские жидкости. Реологические свойства биологических жидкостей в норме и при патологиях
- •6.2 Ламинарное течение жидкостей по цилиндрическим трубам с жёсткими стенками. Формула пуазейля. Закон гагена – пуазейля
- •1. Метод капиллярного вискозиметра (оствальда).
- •2. Метод падающего шарика (стокса)
- •Глава 7 твёрдые и жидкие кристаллы. Стеклообразное состояние вещества. Полимеры.
- •7.1. Фазовые переходы. Плавление, кристаллизация, сублимация.
- •7.2.Кинетические превращения. Стеклование и размягчение
- •7.3. Жидкие кристаллы
- •7.4. Кристаллические модификации твёрдых кристаллов.
- •7.5 Механические свойства твёрдых тел. Закон гука. Упругость и пластичность
- •7.6 Полимеры. Их кристаллическое, стеклообразное, высокоэластическое, вязкотекучее состояние.
- •Глава 8. Процессы переноса
- •8.1. Диффузия
- •8.2. Теплопроводность
- •8.3. Вязкость
- •8.5. Общий вид уравнений процессов переноса
- •Раздел II
- •Глава 1. Механические колебания
- •1.2. Свободные незатухающие механические колебания
- •1.3 Смещение, скорость и ускорение гармонически колеблющегося тела
- •1.4. Энергия гармонически колеблющегося тела
- •1.5. Свободные затухающие колебания
- •1.6 Вынужденные колебания. Резонанс
- •1.7. Автоколебания
- •1.8. Сложения гармонических колебаний, направленных по одной прямой. Теорема фурье. Гармонический спектр сложного колебания
- •Вопросы и задачи к главе 1
- •Глава 2. Механические волны
- •2.1 Механические волны, продольные и поперечные волны
- •2.2. Уравнение и график плоской незатухающей гармонической волны
- •2.3. Энергия волны. Поток энергии. Интенсивность.
- •Вопросы и задачи к главе 2
- •Глава 3. Звук
- •3.1. Субъективные (физиологические) характеритики восприятия звука и их связь с объективными, физическими характеристиками звуковой волны
- •3.2 Область слышимости
- •3.3. Закон вебера-фехнера
- •3.4. Уровень интенсивности
- •Уровень громкости, фон
- •Вопросы и задачи к главе 3
- •Глава 4. Ультразвук. Его применение в медицине инфразвук
- •4.1. Физические свойства ультразвука
- •1. Частотный диапазон ультразвука
- •2. Скорости распространения ультразвука
- •3. Особенности физических свойств ультразвука
- •4. Отражение ультразвука на границе раздела сред
- •5. Поглощение ультразвука
- •4.2 Действие ультразвука на вещество. Биологическое действие ультразвука
- •Механическое действие
- •2..Тепловое действие
- •3. Физико-химическое действие ультразвука
- •4. Биологическое действие ультразвука
- •1. Диагностика.
- •4.4.Источники и приёмники ультразвука
- •1. Пьезоэлектрические излучатели-приёмники
- •2. Магнитострикционные излучатели ультразвука
- •Инфразвук
- •Вопросы и задачи к главе 4
- •Глава 5. Электромагнитные колебания и волны
- •5.1. Некоторые необходимые сведения об основах электричества и магнетизма.
- •Электрические заряды
- •Закон кулона
- •Электроёмкость электрического конденсатора
- •6) Сила ампера -
- •8) Закон электромагнитной индукции фарадея
- •11)Энергия магнитного поля катушки индуктивности
- •5.3. Идеальный колебательный контур
- •5.4. Реальный колебательный контур
- •5.4. Получение незатухающих электромагнитных колебаний
- •5.5. Основные положения теории максвелла
- •Глава 6. Оптика
- •Корпускулярно – волновая природа света
- •6.2. Интерференция света
- •. Разрешающая способность оптических приборов-
- •. Голография
- •Поляризованный свет
- •Естественный и поляризованный свет.
- •2. Поляризатор и анализатор. Закон Малюса.
- •3. Поляризация света при отражении и преломлении. Закон Брюстера.
- •4. Двойное лучепреломление
- •Получение поляризованного света.
- •6. 11 Вращение плоскости поляризации. Оптическая активность. Поляриметрия.
- •Дисперсия света
- •Нормальная дисперсия
- •Качественное объяснение причины нормальной дисперсии
- •Аномальная дисперсия
- •Поглощение света
- •1.Закон Бугера - Ламберта
- •2. Закон Бера
- •Закон Бугера – Ламберта – Бера
- •Коэффициент пропускания и оптическая плотность. Колориметрия
- •2. Два вида рассеяния
- •3. Закон Рэлея
- •4.Турбидиметрия и нефелометрия.
- •6.14. Элементы геометрической оптики
- •Законы отражения и преломления света
- •Явления предельного преломления и полного внутреннего отражения
- •Волоконная оптика. Световоды
- •4.Линзы. Примеры построения изображений в тонких линзах
- •Микроскоп
- •Оптическая система глаза. Некоторые её недостатки, их исправление
- •Рефрактометр
- •Раздел III . Атомная, ядерная и квантовая физика
- •Глава 1. Тепловое излучение тел
- •Основные характеристики теплового излучения. Абсолютно чёрное тело
- •Закон кирхгофа
- •1.2 Спектр теплового излучения абсолютно чёрного тела.Закон вина. Закон стефана-больцмана.
- •1.3 Гипотеза планка. Формула планка
- •1.5. Примеры применения теплового излучения в фармации и медицине
- •Глава 2. Рентгеновское излучение
- •2.1 Простейшая рентгеновская трубка
- •2.2. Основные свойства рентгеновского излучения.
- •Рентгенодиагностика:
- •Рентгенотерапия.
- •Научные исследования.
- •2.4. Природа рентгеновского излучения
- •2.6 Характеристическое рентгеновское излучение
- •Глава 3. Радиоактивность
- •3.1. Радиоактивность. Виды радиоактивных излучений. Основные типы ядерных распадов.
- •3.2 Основной закон радиоактивного распада
- •3.3 Активность радиоактивных препаратов
- •3.4. Ядерные реакции. Меченые атомы
- •Глава 4. Дозиметрия ионизирующих излучений
- •2) Характеристическое рентгеновское излучение.
- •2) Характеристическое рентгеновское излучение.
- •Глава 5. Элементы квантовой механики.
- •5.1. Волновые свойства микрочастиц. Уравнение дё бройля
- •5.2. Электронный микроскоп
- •5.3. Основные положения квантовой механики
- •5.4. Решение уравнения шрёдингера для частицы в потенциальной яме с бесконечно высокими стенками
- •Глава 6. Люминесценция
- •6.1. Виды люминесценции
- •6.2. Фотолюминесценция. Флюоресценция. Фосфоресценция
- •6.3. Спектр фотолюминесценции. Правило стокса
- •6.4. Люминесцентный анализ. Применение в фармации и медицине
- •6.5. Хемилюминесценция
- •Глава 7. Лазер
- •7.1. Вынужденное излучение. Инверсная заселённость. Метастабильные уровни
- •7.3. Свойства лазерного излучения
- •7.4. Применение лазерного излучения в фармации и медицине
- •Глава 8. Оптическая спектроскопия. Ик- спектроскопия. Радиоспектроскопия.
- •8.1. Спектры испускания и спектры поглощения. Спектрографы. Спектрометры. Спектрофотометры
- •8.2. Атомарные спектры. Энергетические уровни атомов
- •8.3. Молекулярные спектры. Энергетические уровни молекул
- •8.4. Спектры комбинационного рассеяния
- •8.5. Радиоспектроскопия
- •Магнитные свойства вещества
- •Раздел IV. Биофизика
- •Глава 1. Молекулярная биофизика
- •Энтропийный характер упругости биополимеров в высокоэластическом состоянии.
- •1.4. Основные типы межатомных и межмолекулярных взаимодействий
- •1.Ионная связь
- •2.Ковалентная связь
- •3.Межатомное отталкивание
- •4. Донорно- акцепторная связь
- •5. Водородная связь
- •1. Ориентационная связь
- •3. Индукционная связь
- •3. Дисперсионная связь
- •4. Межмолекулярное отталкивание
- •5. Гидрофобные взаимодействия
- •Глава 2. Биологические мембраны
- •. Исследование структуры биологических мембран с помощью физических методов.
- •2.3. Жидкостно-мозаичная модель биомембран
- •2.4. Модельные липидные мембраны.
- •2.5. Физические свойства мембран и методы их исследования.
- •2.6. Физическое состояние и фазовые переходы фосфолипидного бислоя
- •Глава 3. Термодинамика биологических систем.
- •3.1 Применение первого начала термодинамики к биологическим системам. Прямая и непрямая калориметрия. Энергетический баланс организма.
- •3.2. Применение второго начала термодинамики к живым системам. Уравнение пригожина.
- •3.3 Сопряженные процессы. Сопряженные процессы созидания и разрушения
- •3.4 Стационарное состояние. Теорема пригожина. Аутостабилизация. Адаптация.
- •Глава 4. Транспорт веществ через биологические мембраны.
- •4.1 Пассивный и активный транспорт веществ
- •Глава 5. Биоэлектрические потенциалы
- •5.1Виды биопотенциалов. Их виды: покоя, действия. Природа биопотенциалов
- •5.2. Методы регистрации биопотенциалов. Микроэлектроды.
- •5.3 Биопотенциалы покоя. Уравнение Гольдмана, уравнение Нернста. Роль ионных насосов в создании биопотенциала покоя
- •Глава 6. Биофизика нервого импульса
- •6.1. Потенциал действия и его свойства
- •Уравнение Ходжкина-Хаксли
- •6.3.Метод фиксации мембранного потенциала. Ионные токи. Ионные каналы
- •Глава 7. Моделирование биофизических процессов
- •7.1 Моделирование биологических процессов. Моделирование физическое, аналоговое, математическое. Основные требования к моделям.
- •Математические модели роста популяции
- •7.3 Фармакокинетическая модель
5.3 Биопотенциалы покоя. Уравнение Гольдмана, уравнение Нернста. Роль ионных насосов в создании биопотенциала покоя
Потенциал покоя – стационарная разность электрических потенциалов, регистрируемая между внутренней и наружной поверхностями мембраны в невозбужденном состоянии.
Потенциал покоя определяется разной концентрацией ионов по разные стороны мембраны и диффузией ионов через мембрану (рис. 5.3)
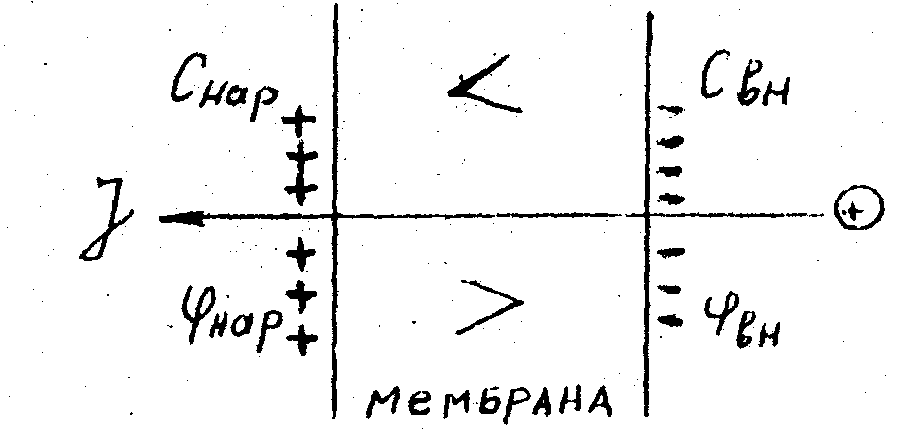
Рис. 5.2 Возникновение мембранного потенциала вследствие диффузии катионов (объяснение в тексте).
Если концентрация какого-либо иона
внутри клетки ![]() отлична от концентрации этого иона
снаружи
отлична от концентрации этого иона
снаружи ![]() ,
и мембрана проницаема для этого иона,
возникает поток заряженных частиц через
мембрану, вследствие чего нарушается
электрическая нейтральность системы,
образуется разность потенциалов внутри
и снаружи клетки
,
и мембрана проницаема для этого иона,
возникает поток заряженных частиц через
мембрану, вследствие чего нарушается
электрическая нейтральность системы,
образуется разность потенциалов внутри
и снаружи клетки
![]() =
= ![]() ,
которая будет препятствовать дальнейшему
перемещению ионов через мембрану. При
установлении равновесия выравниваются
значения электрохимических потенциалов
по разные стороны мембраны
,
которая будет препятствовать дальнейшему
перемещению ионов через мембрану. При
установлении равновесия выравниваются
значения электрохимических потенциалов
по разные стороны мембраны
![]() =
= ![]()

ln![]() + z
+ z![]() = RT
·ln
= RT
·ln![]() + z
+ z![]() ,
,
откуда легко получить формулу Нернста для равновесного мембранного потенциала
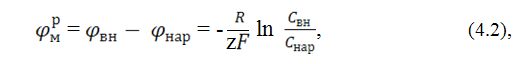
здесь R=8.3 Дж/К моль – универсальная газовая постоянная,
Т – температура в К, F=96500 Кл/моль – число Фарадея и
z - заряд иона (в единицах элементарного заряда).
Если мембранный потенциал обусловлен переносом ионов , для которых
![]() вн
>
нар
и z =+ 1,
вн
>
нар
и z =+ 1,
![]() =
-
=
- ![]() ln
ln
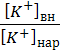
![]() 0 (4.3)
0 (4.3)
Для ионов
:
![]() , z = +1, и поэтому:
, z = +1, и поэтому:
![]() = -
ln
= -
ln

![]() (4.4)
(4.4)
Для ионов ![]() :
: ![]() , z = -1
, z = -1
и
![]() = -
ln
= -
ln
![]()
![]() (4.5)
(4.5)
Если в формуле Нернста перейти от натурального логарифма к десятичному, то для положительного одновалентного иона (z = +1)
![]() ≈
-
≈
-![]() 2.3 lg
2.3 lg
![]()
Примем температуру Т = 300 К, тогда
2.3 ≈ 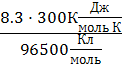 2.3 ≈ 0.06 В
2.3 ≈ 0.06 В
![]() ≈ - 0.06 В lg
(4.6)
≈ - 0.06 В lg
(4.6)
Согласно Бернштейну (1902 г.), причина мембранного потенциала покоя – диффузия ионов калия из клетки наружу.
Примем в формуле Нернста
![]() ≈ 100,
≈ 100,
что по порядку величины соответствует экспериментальным данным для калия (см. таблицу 5.1),
lg ![]() = lg 100 = 2
= lg 100 = 2
и мембранный потенциал ![]() = 0,06·2=0,12 В = 120 мВ, что несколько больше
экспериментально измеренных значений
потенциала покоя, и, пользуясь формулами
элементарной электростатики, оценим,
какое количество ионов должно перейти
из цитоплазмы во внеклеточную среду,
чтобы создать такую разность потенциалов.
= 0,06·2=0,12 В = 120 мВ, что несколько больше
экспериментально измеренных значений
потенциала покоя, и, пользуясь формулами
элементарной электростатики, оценим,
какое количество ионов должно перейти
из цитоплазмы во внеклеточную среду,
чтобы создать такую разность потенциалов.
Радиус клетки примем r =
10 мкм = ![]() м. Удельная электроёмкость мембраны
(электроемкость на единицу площади)
м. Удельная электроёмкость мембраны
(электроемкость на единицу площади)
![]() ≈
≈ ![]()
![]() .
.
Площадь мембраны
4π ![]() = 4π
= 4π ![]() ≈
≈ ![]() .
.
Тогда электроёмкость мембраны
C =
S ≈ ![]()
![]() =
= ![]() Ф
Ф
Абсолютная величина заряда каждого знака на поверхности мембраны, если ее представить себе как конденсатор,
![]() = ∆С φм ≈
ф·
= ∆С φм ≈
ф·
![]() В
=
Кл,
В
=
Кл,
что соответствует
![]() ≈
≈ 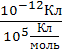 =
= ![]()
Объем клетки
V = ![]()
![]()
![]() ≈
≈
![]() ≈
5·
.
≈
5·
.
Изменение концентрации ионов в клетке
вследствие выхода из клетки ![]() моль ионов составит
моль ионов составит
∆С ≈ ![]() = 2·
= 2· ![]() = 2·
= 2· ![]()
Это ничтожное изменение концентрации по сравнению с концентрацией ионов калия внутри клетки (см. таблицу 5.1), изменение концентрации составляет всего ≈ 4 % от концентрации калия внутри клетки. Таким образом, для создания равновесного нернстовского мембранного потенциала, через мембрану должно пройти пренебрежимо малое количество ионов по сравнению с общим их количеством в клетке.
В таблице 5.1 приведены значения мембранного потенциала, рассчитанные по формуле Нернста для различных клеток и для различных ионов, и экспериментально полученные значения потенциала покоя для этих клеток.
ТАБЛИЦА 5.1 СОДЕРЖАНИЯ ИОНОВ РАВНОВЕСНЫХ ПОТЕНЦИАЛОВ И ПОТЕНЦИАЛОВ ПОКОЯ НЕКОТОРЫХ КЛЕТОК
объект |
концентрация ммоль/л |
мВ по формуле Нернста |
|
|||||||
[K+] |
[Na+] |
[Cl-] |
||||||||
вн |
нар |
вн |
нар |
вн |
нар |
K+ |
Na+ |
Cl- |
||
Гигантский аксон кальмара |
360 |
10 |
70 |
420 |
160 |
500 |
-90 |
50 |
-30 |
-60 |
Мышца лягушки |
125 |
2,5 |
15 |
125 |
11 |
120 |
-98 |
60 |
-87 |
-94 |
Из сравнения рассчитанных и экспериментальных значений мембранного потенциала видно, что потенциал покоя, на самом деле, ближе к потенциалу, рассчитанному по формуле Нернста для K+ в cоответствии с предположением Бернштейна, что потенциал покоя – калиевый потенциал.
Вместе с тем, обращают на себя внимание значительные расхождения экспериментальных и теоретических значений. Причины расхождений в том, что не учтена проницаемость мембраны для других ионов.
Одновременная диффузия через мембрану ионов K+, Na+, Cl- учитывается уравнением Гольдмана. При выводе уравнения Гольдмана, в отличие от уравнения Нернста, рассматривается не равновесный, а стационарный случай. Потоки ионов через мембрану не становятся равными нулю, а компенсируют друг друга, так что суммарный перенос заряда равен нулю. Суммарный поток ионов K+, Na+ и Cl- равен нулю:
Jk+ + JNa+ + Jcl- =0
Вывод уравнения Гольдана из уравнения Нернста – Планка сложен, и поэтому мы его не приводим. Уравнение Гольдмана имеет вид:
![]() (4.7)
(4.7)
Pk , PNa , PCl - проницаемости мембраны для ионов, K+, Na+ и Cl- .
В числителе выражения, стоящего под
знаком логарифма, стоят концентрации
![]() ,
,
![]() ,
но
,
но![]() ,
а в знаменателе
,
а в знаменателе ![]() ,
,
![]() , но
, но![]() так как
ионы хлора отрицательно заряжены.
так как
ионы хлора отрицательно заряжены.
В состоянии покоя проницаемость мембраны для ионов значительно больше, чем для и больше, чем для .
![]()
для аксона кальмара, например,
![]()
Переписав уравнение Гольдмана в виде:
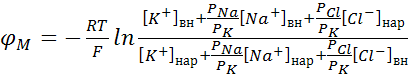 ,
,
в случае, когда проницаемость мембраны для натрия и хлора значительно меньше проницаемости для калия
![]() и
и ![]() ,
,
из уравнения Гольдмана получим уравнение Нернста:

Мембранный потенциал, рассчитанный по уравнению Гольдмана, оказался по абсолютной величине меньше мембранного потенциала, рассчитанного по формуле Нернста, и был ближе к экспериментальным его значениям в крупных клетках.
И формула Нернста и уравнение Гольдмана не учитывают активного транспорта ионов через мембрану, наличия в мембранах электрогенных (вызывающих разделение зарядов, а следовательно и возникновение разности потенциалов) ионных насосов, играющих важную роль в поддержании ионного равновесия в мелких клетках.
В цитоплазматической мембране работают
![]() - АТФ-азы, перекачивающие
калий внутрь клетки, а натрий из клетки.
С учетом работы электрогенных ионных
насосов для мембранного потенциала
было получено уравнение (Томас, 1972):
- АТФ-азы, перекачивающие
калий внутрь клетки, а натрий из клетки.
С учетом работы электрогенных ионных
насосов для мембранного потенциала
было получено уравнение (Томас, 1972):

где m - отношение количества
ионов натрия к количеству ионов калия,
перекачиваемых ионными насосами через
мембрану. Чаще всего
- АТФ-аза работает в режиме, когда m=
,
m всегда больше 1
(нет ионных насосов, перекачивающих
Cl-, поэтому в уравнении
Томаса отсутствуют члены ![]() ).
).
Коэффициент m > 1 усиливает вклад градиента концентрации калия в создание мембранного потенциала, поэтому мембранный потенциал, рассчитанный по Томасу, больше по абсолютной величине, чем мембранный потенциал, рассчитанный по Гольдману, и дает совпадение с экспериментальными значениями для мелких клеток.
Нарушение биоэнергетических процессов в клетке и работы АТФ-азы приводит к уменьшению , в этом случае мембранный потенциал лучше описывается уравнением Гольдмана.
Повреждение клеточной мембраны приводит
к повышению проницаемости клеточных
мембран для всех ионов: к повышению и
![]() ,
и
,
и ![]() ,
и
,
и ![]() .
Вследствие уменьшения различия
проницаемостей для различных ионов
абсолютное значение мембранного
потенциала
снижается.
.
Вследствие уменьшения различия
проницаемостей для различных ионов
абсолютное значение мембранного
потенциала
снижается.
Для сильно поврежденных клеток
еще меньше, но сохраняется отрицательный
мембранный потенциал ![]() за счет содержащихся в клетке
полианионов – отрицательно заряженных
белков, нуклеиновых кислот и других
крупных молекул, не могущих проникнуть
через мембрану (доннановский потенциал).
за счет содержащихся в клетке
полианионов – отрицательно заряженных
белков, нуклеиновых кислот и других
крупных молекул, не могущих проникнуть
через мембрану (доннановский потенциал).
ВОПРОСЫ И ЗАДАЧИ К ГЛАВЕ 5
1.Что такое биоэлектрические потенциалы? Какую роль они выполняют в организме? Какое значение имеет их исследование для фармации и медицины?
2. Что такое мембранный потенциал (трансмембранная разность электрических потенциалов)? За счёт каких процессов он образуется?
3. Что такое потенциал покоя, перенос каких ионов через цитоплазматическую мембрану его поддерживает?
4. В чём различия условий при которых выводятся уравнения Нернста и Гольдмана?
5. Как влияет на величину мембранного потенциала покоя нарушение работы ионных насосов в мембране? Нарушение барьерной функции мембраны?
6.Концентрация калия внутри клетки 400 ммоль/л, а во внеклеточной среде 10 ммоль/л. Толщина мембраны 10 нм. Оцените разность электрических потенциалов на мембране в состоянии покоя и напряжённость электрического поля в мембране.
