
- •Раздел I. Механика. Молекулярная физика. Термодинамика 16 глава 1. Законы динамики ньютона. Законы сохранения 16
- •Вопросы и задачи к главе I. 33 глава 2. Молекулярно-кинетическая теория газов
- •Глава 3. Применение первого начала термодинамики к процессам в идеальном газе 52
- •Глава 4. Реальные газы 74
- •Вопросы и задачи и вопросы к главе 4. 82 глава 5. Поверхностное натяжение жидкости 82
- •Вопросы и задачи к главе 5 102
- •Глава 6. Вязкость жидкости 103
- •Вопросы и задачи к главе 6 116
- •Глава 7. Твёрдые и жидкие кристаллы. Стеклообразное состояние вещества. Полимеры 117
- •Глава 8. Процессы переноса 127
- •Раздел II колебания и волны 135
- •Глава 1. Механические колебания 135
- •Вопросы и задачи к главе 1. 153
- •Глава 2. Механические волны 153
- •Вопросы задачи к главе 2. 158
- •Глава 3. Звук 159
- •Вопросы и задачи к главе 3. 167
- •Глава 4. Ультразвук. Его применение в медицине. Инфразвук
- •Вопросы задачи к главе 4 180
- •Глава 5. Электромагнитные колебания и волны 181
- •Вопросы задачи к главе 5 201 глава 6. Оптика 201
- •Вопросы задачи к главе 6 251
- •Раздел III. Атомная, ядерная и квантовая физика
- •Глава 1. Тепловое излучение тел 253
- •Глава 2. Рентгеновское излучение 261
- •Глава 3. Радиоактивность 272
- •Глава 4. Дозиметрия ионизирующих излучений 282
- •Раздел IV. Биофизика 337 глава1 молекулярная биофизика 337
- •Глава 2. Биологические мембраны. 358
- •Глава 3. Термодинамика биологических систем 386
- •Глава 4. Транспорт веществ через биологические мембраны
- •Глава 5. Биопотенциалы 416
- •Глава 6. Биофизика нервного импульса 427
- •Глава 7. Моделирование биологических процессов 446
- •Введение
- •Раздел I механика. Молекулярная физика. Термодинамика.
- •Глава 1 законы динамики ньютона. Законы сохранения.
- •1.1. Законы ньютона. Основные дифференциальные уравнения движения.
- •Здесь аx , аy , аz - проекции вектора ускорения на оси координат X , y и z;
- •1. 2. Законы сохранения импульса и энергии
- •. Задача о центральном ударе шаров: абсолютно упругом и абсолютно неупругом.
- •1.4 Физические основы центрифугирования
- •Глава 2. Молекулярно-кинетическая теория газов
- •2.1 Отличия молекулярной структуры газов, жидкостей и твёрдых тел. Характер молекулярного движения в различных состояниях вещества. Аморфные и кристаллические жидкости и твёрдые тела
- •Примечание 2
- •2.2 Основное уравнение молекулярно-кинетической теории газов. Средняя квадратическая скорость молекул газа.
- •2.3 Средняя кинетическая энергия поступательного движения молекул газа. Распределение энергии по степеням свободы. Внутренняя энергия идеального газа
- •2.4 Распределение Максвелла молекул идеального газа по абсолютным значениям их скоростей.
- •2.5 Распределение Больцмана по потенциальным энергиям молекул идеального газа. Барометрическая формула Больцмана.
- •Глава 3. Применение первого начала термодинамики к процессам в идеальном газе.
- •3.1. Особенности термодинамического метода. Первое начало термодинамики.
- •3.2. Применение первого начала термодинамики к равновесным изопроцессам идеального газа
- •Работа газа при его расширении
- •Теплоёмкость
- •Политропные процессы - процессы с постоянной теплоёмкостью.
- •Глава 4. Реальные газы
- •4.1.Уравнение состояния реального газа Ван - дер - Ваальса и изотермы Ван- дер - Ваальса.
- •4.2. Изотермы Эндрюса
- •Сжижение газов. Получение низких температур.
- •Глава 5. Поверхностное натяжение жидкости
- •5.3 Поверхностные явления на границе твёрдой, жидкой и газообразной фазы. Краевой угол смачивания. Смачивание и несмачивание твёрдой поверхности жидкостью.
- •5.4 Давление Лапласа. Капиллярные явления.
- •5.5 Методы определения коэффициента поверхностного натяжения
- •1. Метод отрыва капель
- •2. Метод отрыва кольца
- •Глава 6. Вязкость жидкости
- •6.1 Вязкость жидкости. Закон ньютона. Ньютоновские и неньютоновские жидкости. Реологические свойства биологических жидкостей в норме и при патологиях
- •6.2 Ламинарное течение жидкостей по цилиндрическим трубам с жёсткими стенками. Формула пуазейля. Закон гагена – пуазейля
- •1. Метод капиллярного вискозиметра (оствальда).
- •2. Метод падающего шарика (стокса)
- •Глава 7 твёрдые и жидкие кристаллы. Стеклообразное состояние вещества. Полимеры.
- •7.1. Фазовые переходы. Плавление, кристаллизация, сублимация.
- •7.2.Кинетические превращения. Стеклование и размягчение
- •7.3. Жидкие кристаллы
- •7.4. Кристаллические модификации твёрдых кристаллов.
- •7.5 Механические свойства твёрдых тел. Закон гука. Упругость и пластичность
- •7.6 Полимеры. Их кристаллическое, стеклообразное, высокоэластическое, вязкотекучее состояние.
- •Глава 8. Процессы переноса
- •8.1. Диффузия
- •8.2. Теплопроводность
- •8.3. Вязкость
- •8.5. Общий вид уравнений процессов переноса
- •Раздел II
- •Глава 1. Механические колебания
- •1.2. Свободные незатухающие механические колебания
- •1.3 Смещение, скорость и ускорение гармонически колеблющегося тела
- •1.4. Энергия гармонически колеблющегося тела
- •1.5. Свободные затухающие колебания
- •1.6 Вынужденные колебания. Резонанс
- •1.7. Автоколебания
- •1.8. Сложения гармонических колебаний, направленных по одной прямой. Теорема фурье. Гармонический спектр сложного колебания
- •Вопросы и задачи к главе 1
- •Глава 2. Механические волны
- •2.1 Механические волны, продольные и поперечные волны
- •2.2. Уравнение и график плоской незатухающей гармонической волны
- •2.3. Энергия волны. Поток энергии. Интенсивность.
- •Вопросы и задачи к главе 2
- •Глава 3. Звук
- •3.1. Субъективные (физиологические) характеритики восприятия звука и их связь с объективными, физическими характеристиками звуковой волны
- •3.2 Область слышимости
- •3.3. Закон вебера-фехнера
- •3.4. Уровень интенсивности
- •Уровень громкости, фон
- •Вопросы и задачи к главе 3
- •Глава 4. Ультразвук. Его применение в медицине инфразвук
- •4.1. Физические свойства ультразвука
- •1. Частотный диапазон ультразвука
- •2. Скорости распространения ультразвука
- •3. Особенности физических свойств ультразвука
- •4. Отражение ультразвука на границе раздела сред
- •5. Поглощение ультразвука
- •4.2 Действие ультразвука на вещество. Биологическое действие ультразвука
- •Механическое действие
- •2..Тепловое действие
- •3. Физико-химическое действие ультразвука
- •4. Биологическое действие ультразвука
- •1. Диагностика.
- •4.4.Источники и приёмники ультразвука
- •1. Пьезоэлектрические излучатели-приёмники
- •2. Магнитострикционные излучатели ультразвука
- •Инфразвук
- •Вопросы и задачи к главе 4
- •Глава 5. Электромагнитные колебания и волны
- •5.1. Некоторые необходимые сведения об основах электричества и магнетизма.
- •Электрические заряды
- •Закон кулона
- •Электроёмкость электрического конденсатора
- •6) Сила ампера -
- •8) Закон электромагнитной индукции фарадея
- •11)Энергия магнитного поля катушки индуктивности
- •5.3. Идеальный колебательный контур
- •5.4. Реальный колебательный контур
- •5.4. Получение незатухающих электромагнитных колебаний
- •5.5. Основные положения теории максвелла
- •Глава 6. Оптика
- •Корпускулярно – волновая природа света
- •6.2. Интерференция света
- •. Разрешающая способность оптических приборов-
- •. Голография
- •Поляризованный свет
- •Естественный и поляризованный свет.
- •2. Поляризатор и анализатор. Закон Малюса.
- •3. Поляризация света при отражении и преломлении. Закон Брюстера.
- •4. Двойное лучепреломление
- •Получение поляризованного света.
- •6. 11 Вращение плоскости поляризации. Оптическая активность. Поляриметрия.
- •Дисперсия света
- •Нормальная дисперсия
- •Качественное объяснение причины нормальной дисперсии
- •Аномальная дисперсия
- •Поглощение света
- •1.Закон Бугера - Ламберта
- •2. Закон Бера
- •Закон Бугера – Ламберта – Бера
- •Коэффициент пропускания и оптическая плотность. Колориметрия
- •2. Два вида рассеяния
- •3. Закон Рэлея
- •4.Турбидиметрия и нефелометрия.
- •6.14. Элементы геометрической оптики
- •Законы отражения и преломления света
- •Явления предельного преломления и полного внутреннего отражения
- •Волоконная оптика. Световоды
- •4.Линзы. Примеры построения изображений в тонких линзах
- •Микроскоп
- •Оптическая система глаза. Некоторые её недостатки, их исправление
- •Рефрактометр
- •Раздел III . Атомная, ядерная и квантовая физика
- •Глава 1. Тепловое излучение тел
- •Основные характеристики теплового излучения. Абсолютно чёрное тело
- •Закон кирхгофа
- •1.2 Спектр теплового излучения абсолютно чёрного тела.Закон вина. Закон стефана-больцмана.
- •1.3 Гипотеза планка. Формула планка
- •1.5. Примеры применения теплового излучения в фармации и медицине
- •Глава 2. Рентгеновское излучение
- •2.1 Простейшая рентгеновская трубка
- •2.2. Основные свойства рентгеновского излучения.
- •Рентгенодиагностика:
- •Рентгенотерапия.
- •Научные исследования.
- •2.4. Природа рентгеновского излучения
- •2.6 Характеристическое рентгеновское излучение
- •Глава 3. Радиоактивность
- •3.1. Радиоактивность. Виды радиоактивных излучений. Основные типы ядерных распадов.
- •3.2 Основной закон радиоактивного распада
- •3.3 Активность радиоактивных препаратов
- •3.4. Ядерные реакции. Меченые атомы
- •Глава 4. Дозиметрия ионизирующих излучений
- •2) Характеристическое рентгеновское излучение.
- •2) Характеристическое рентгеновское излучение.
- •Глава 5. Элементы квантовой механики.
- •5.1. Волновые свойства микрочастиц. Уравнение дё бройля
- •5.2. Электронный микроскоп
- •5.3. Основные положения квантовой механики
- •5.4. Решение уравнения шрёдингера для частицы в потенциальной яме с бесконечно высокими стенками
- •Глава 6. Люминесценция
- •6.1. Виды люминесценции
- •6.2. Фотолюминесценция. Флюоресценция. Фосфоресценция
- •6.3. Спектр фотолюминесценции. Правило стокса
- •6.4. Люминесцентный анализ. Применение в фармации и медицине
- •6.5. Хемилюминесценция
- •Глава 7. Лазер
- •7.1. Вынужденное излучение. Инверсная заселённость. Метастабильные уровни
- •7.3. Свойства лазерного излучения
- •7.4. Применение лазерного излучения в фармации и медицине
- •Глава 8. Оптическая спектроскопия. Ик- спектроскопия. Радиоспектроскопия.
- •8.1. Спектры испускания и спектры поглощения. Спектрографы. Спектрометры. Спектрофотометры
- •8.2. Атомарные спектры. Энергетические уровни атомов
- •8.3. Молекулярные спектры. Энергетические уровни молекул
- •8.4. Спектры комбинационного рассеяния
- •8.5. Радиоспектроскопия
- •Магнитные свойства вещества
- •Раздел IV. Биофизика
- •Глава 1. Молекулярная биофизика
- •Энтропийный характер упругости биополимеров в высокоэластическом состоянии.
- •1.4. Основные типы межатомных и межмолекулярных взаимодействий
- •1.Ионная связь
- •2.Ковалентная связь
- •3.Межатомное отталкивание
- •4. Донорно- акцепторная связь
- •5. Водородная связь
- •1. Ориентационная связь
- •3. Индукционная связь
- •3. Дисперсионная связь
- •4. Межмолекулярное отталкивание
- •5. Гидрофобные взаимодействия
- •Глава 2. Биологические мембраны
- •. Исследование структуры биологических мембран с помощью физических методов.
- •2.3. Жидкостно-мозаичная модель биомембран
- •2.4. Модельные липидные мембраны.
- •2.5. Физические свойства мембран и методы их исследования.
- •2.6. Физическое состояние и фазовые переходы фосфолипидного бислоя
- •Глава 3. Термодинамика биологических систем.
- •3.1 Применение первого начала термодинамики к биологическим системам. Прямая и непрямая калориметрия. Энергетический баланс организма.
- •3.2. Применение второго начала термодинамики к живым системам. Уравнение пригожина.
- •3.3 Сопряженные процессы. Сопряженные процессы созидания и разрушения
- •3.4 Стационарное состояние. Теорема пригожина. Аутостабилизация. Адаптация.
- •Глава 4. Транспорт веществ через биологические мембраны.
- •4.1 Пассивный и активный транспорт веществ
- •Глава 5. Биоэлектрические потенциалы
- •5.1Виды биопотенциалов. Их виды: покоя, действия. Природа биопотенциалов
- •5.2. Методы регистрации биопотенциалов. Микроэлектроды.
- •5.3 Биопотенциалы покоя. Уравнение Гольдмана, уравнение Нернста. Роль ионных насосов в создании биопотенциала покоя
- •Глава 6. Биофизика нервого импульса
- •6.1. Потенциал действия и его свойства
- •Уравнение Ходжкина-Хаксли
- •6.3.Метод фиксации мембранного потенциала. Ионные токи. Ионные каналы
- •Глава 7. Моделирование биофизических процессов
- •7.1 Моделирование биологических процессов. Моделирование физическое, аналоговое, математическое. Основные требования к моделям.
- •Математические модели роста популяции
- •7.3 Фармакокинетическая модель
3.2. Применение первого начала термодинамики к равновесным изопроцессам идеального газа
Работа газа при его расширении

Рис.3.3.
На рис.3.3 газ,
заключённый в цилиндре под поршнем с
площадью S
,совершает работу, перемещая поршень
вверх на dx.
Изменение объёма газа при этом dV=S![]() dx
считаем столь малым что изменением
давления газа p
можно пренебречь и можно считать его
постоянным
dx
считаем столь малым что изменением
давления газа p
можно пренебречь и можно считать его
постоянным
р = const
Тогда элементарное количество работы, произведённой газом при его расширении:
![]()
потому что силу давления газа на поршень при таком его малом расширении F=pS можно считать постоянной.
Так как Sdx=dV, элементарное количество работы при изменении объёма газа на dV равно давлению газа, помноженному на элементарное изменение объёма dV:
![]() (3.4)
(3.4)
При больших изменениях объёма работу можно вычислить по формуле:
![]() (3.5)
(3.5)
где ![]() -
начальный объём
-
начальный объём ![]() -
конечный объёмы газа ,а давление p-
функция объёма, вид которой определяется
типом процесса перехода газа из первого
состояния во второе.
-
конечный объёмы газа ,а давление p-
функция объёма, вид которой определяется
типом процесса перехода газа из первого
состояния во второе.
На графиках, изображающих процесс в координатах p иV, работа газа равна площади под графиком. (рис.3.4)
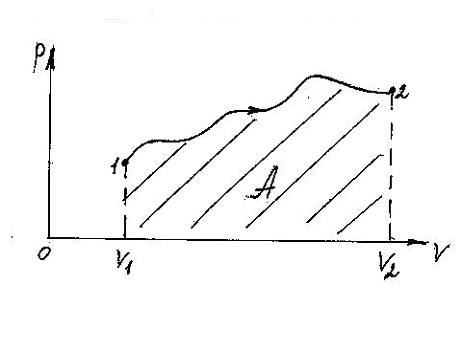
Рис. 3.4. Нахождение работы газа при его расширении по площади под графиком зависимости его давления р от объема V
Теплоёмкость
Теплоёмкость тела численно равна количеству теплоты, которое нужно подвести к телу для его нагревания на единицу температуры.
![]() (3.6)
(3.6)
Удельная теплоёмкость численно равна количеству теплоты, нужного для нагревания единицы массы тела на единицу температуры
Cуд = бQ /m dT (Дж/кг К) (3.7)
Молярная теплоёмкость вещества численно равна количеству теплоты, необходимому для нагревания одного моля вещества на единицу температуры
Cуд = бQ /(m/М) dT (Дж/моль К) (3.8)
Из 3.7 и 3.8 видно, что

Так как теплота - функционал процесса, то и теплоёмкость зависит от условий, при которых протекает процесс. Теплоёмкость данного вещества в разных процессах разная.
В дальнейшем будем оперировать только молярными теплоёмкостями и будем их обозначать строчной буквой c.
Изопроцессы в идеальных газах
Изопроцессы– процессы, протекающие при постоянстве какого-нибудь параметра.
Для простоты будем рассматривать один моль идеального газа. Для этого случая уравнение состояния идеального газа - уравнение Клапейрона- Менделеева
![]()
примет вид:
![]()
так как
![]()
(Здесь и дальше V- объём одного моля газа при температуре T и давлении p).
А. Изохорный процесс- при котором объём постоянен:
(рис.3.5)

Рис.3.5 Изохорный процесс
Так как V=const, dV=0,то, согласно 3.4 и 3.5, газ при этом процессе работы не совершает
![]()
и вся теплота, подводимая к газу, идёт на увеличение его внутренней энергии
![]() (3.9)
(3.9)
Молярная теплоёмкость при постоянном объёме:
![]() (3.10)
(3.10)
Отсюда элементарное изменение внутренней энергии:
![]() (3.11)
(3.11)
Изменение внутренней энергии:
![]() (3.12)
(3.12)
а количество теплоты
![]()
Согласно молекулярной физике внутренняя энергия одного моля идеального газа U определяется температурой T и числом степеней свободы молекулы i:
![]()
и поэтому молярная теплоёмкость при постоянном объёме идеального газа:
![]() (3.13)
(3.13)
Б.Изобарный процесс -при постоянном давлении (рис.3.6):
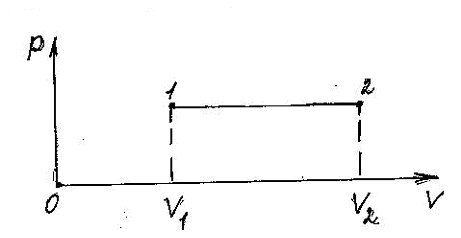
Рис.3.6 Изобарный процесс
В этом случае элементарное количество работы
![]()
Количество работы

Поэтому первое начало термодинамики записывается для этого случая так:
и , подставив сюда выражение для , запишем
![]() (3.14)
(3.14)
Так
как согласно (3.11),dU=![]() ,
,
![]() (3.15)
(3.15)
Из уравнения Клапейрона-Менделеева для одного моля
pV=RT
Продифференцировав обе части этого равенства при p=const, получим:
pdV=RdT
И тогда первое начало термодинамики для идеальных газов при постоянном давлении запишется так:
![]()
А молярная теплоёмкость идеального газа при постоянном давлении будет
![]()
Это уравнение
![]() (3.16)
(3.16)
носит название уравнения Майера. Оно получило блестящее подтверждение опытными данными ,что в своё время сыграло большую роль в утверждении первого начала термодинамики.
Теплоёмкость при изобарическом нагревании газа больше его теплоёмкости при постоянном объёме, потому что при постоянном давлении газ расширяется, и теплота идёт не только на увеличение внутренней энергии газа, но и ещё на совершение работы против сил внешнего давления.
Согласно 3.13 и 3.16
![]() (3.17)
(3.17)
а отношения
теплоёмкостей ![]() и
и ![]()
![]() (3.18)
(3.18)
В.Изотермический процесс - процесс при постоянной температуре:
T=const,dT=0 (рис. 3.7)
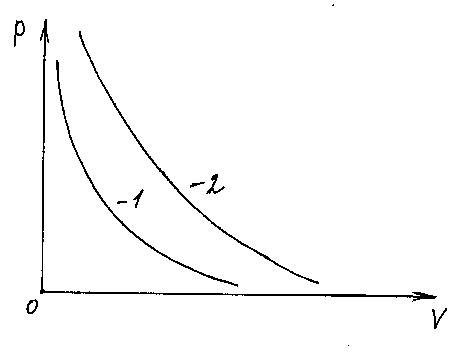
Рис 3.7 Изотермический
процесс 1- T
1 , 2- T2
![]() T1
.
T1
.
Внутренняя энергия идеального газа при постоянной температуре не меняется
![]() ,
U=const
,
U=const
И вся теплота идёт на совершение работы:
![]()
Q=A=![]()
Учитывая, что для одного моля идеального газа
,
![]() (3.19)
(3.19)
При расширении газа:
![]() ,
,![]()
Газ совершает работу и для сохранения постоянной температуры и, следовательно, внутренней энергии к нему надо подводить энергию извне в процессе теплопередачи.
При сжатии газа работа совершается над газом и полученную при этом энергию он отдаёт назад в окружающую среду в процессе теплопередачи.
![]()
Теплоёмкость при изотермическом процессе
![]()
При расширении
газа (dT![]() )
)
![]()
При сжатии газа
(![]() )
)
![]()
Г. Адиабатический процесс - когда отсутствует теплообмен системы с окружающей средой:
![]()
Следовательно, теплоёмкость при адиабатическом процессе
![]()
Равновесный адиабатический процесс тоже относится к изопроцессам и вот почему.
Согласно второму началу термодинамики, элементарное изменение функции состояния - энтропии при равновесных процессах равно элементарному количеству теплоты, обмененному системой с окружающей средой, делённой на температуру системы.
![]()
Так как в равновесных
адиабатических процессах система не
обменивается теплотой с окружающей
средой, ![]() ,
также и dS=0
, а S=const
,
также и dS=0
, а S=const
Таким образом, равновесный адиабатический процесс протекает при неизменной энтропии, это изоэнтропийный процесс.
Первое начало термодинамики для этого изопроцесса записывается так:
![]()
Или
![]()
Вся работа совершается системой только за счёт расхода её внутренней энергии.
Первое начало для идеального газа в дифференциальном виде для этого случая имеет вид:
![]()
так как
и ![]() ,
,
Откуда для элементарного изменения температуры получим:
![]() (3.20)
(3.20)
При адиабатическом
расширении газа, когда ![]() ,
газ охлаждается
,
газ охлаждается ![]() Это
применяется, например, для получения
низких температур.
Это
применяется, например, для получения
низких температур.
При адиабатическом
сжатии, когда ![]() , газ нагревается
, газ нагревается![]() .
.
Это используется, в частности, в двигателях Дизеля, где в длинном толстостенном цилиндре рабочей камеры двигателя сильно сжимается воздух. Так как это происходит быстро, газ не успевает отдать энергию в окружающую среду в процессе теплообмена и нагревается до высокой температуры. Затем в раскалённый воздух впрыскивается топливо, возгорающееся от соприкосновения с горячим воздухом. Освобождённая при химической реакции внутренняя энергия топлива резко повышает температуру и давление в рабочей камере и толкает поршень - совершается рабочий ход.
А теперь, проведя ряд несложных математических преобразований, выведем уравнение адиабаты - связывающее параметры p и V идеального газа при равновесном адиабатическом процессе.
Согласно уравнению Клапейрона-Менделеева для одного моля идеального газа:
RT= pV
Продифференцируем обе части уравнения:
RdT = pdV + Vdp
Откуда:
![]() (3.21)
(3.21)
Приравняв правые части уравнений 3.20и 3.21, получим:
![]()
или
![]()
и
![]()
![]()
![]()
Так как согласно уравнению Майера
![]()
получим
![]()
где
![]()
Продолжим математические преобразования. Разделив переменные в полученном дифференциальном уравнении, запишем
![]()
А теперь обе части уравнения проинтегрируем в пределах: от параметров начального состояния
![]()
до параметров конечного состояния
![]()
Получаем
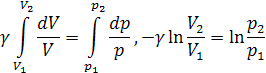
-
и отсюда
![]()
После потенцирования:
![]()
или
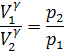
И наконец
![]()
Или (в силу произвольно выбора состояний 1 и 2)
![]() (3.22)
(3.22)
и
![]() (3.23)
(3.23)
Давление при адиабатическом расширении уменьшается, а при сжатии увеличивается быстрее, чем при изотермических условиях, так как газ при адиабатическом расширении охлаждается, а при сжатии нагревается, что приводит к большему, нежели при изотермических процессах изменению давления. Адиабата идёт круче, чем изотерма (см. рис.3.8)

Рис. 3.8, Изотерма – 1 и адиабата – 2.
Показатель
адиабаты ![]() определяется числом степеней свободы
молекулы
определяется числом степеней свободы
молекулы
![]() (3.24)
(3.24)
Определяя экспериментально показатель адиабаты и число степеней свободы молекулы, можно установить к каким газам: одноатомным, двухатомным, или многоатомным относится исследуемый образец - один из методов качественного химического анализа.
