
- •Определение отношения теплоемкости газа при постоянном давлении к теплоемкости при постоянном объеме
- •Составители Валишев м.Г., Гребенкина о.Г., Повзнер а.А., Саввин в.С.
- •1. Некоторые сведения из теории
- •2. Метод клемана - дезорма
- •3. Работа при адиабатическом процессе
- •4. Усовершенствованный вариант метода
- •5. Описание установки. Порядок выполнения работы
- •Контрольные вопросы
- •Определение отношения теплоемкости газа при постоянном давлении к теплоемкости при постоянном объеме
- •Определение отношения теплоемкости газа при постоянном давлении к теплоемкости при постоянном объеме
- •620002, Екатеринбург, Мира, 19
- •620002, Екатеринбург, Мира, 19
2. Метод клемана - дезорма
Метод Клемана-Дезорма определения величины γ базируется на измерении давления газа, заключенного в одном и том же сосуде и последовательно проходящего через три состояния: из первого во второе газ переходит адиабатически, из второго в третье – изохорически. Рассмотрим это более подробно.
В
стеклянный баллон нагнетается воздух
до давления
p1,
которое превышает атмосферное давление
p0
на небольшую величину p,
т.е.
![]() и
и
![]() .
После установления термодинамического
равновесия с окружающей средой температура
в баллоне будет T1.
.
После установления термодинамического
равновесия с окружающей средой температура
в баллоне будет T1.
Таким образом, начальное состояние газа (состояние 1 на рис. 3) определяется параметрами V1, p1, T1.
Рис. 3. Схема
термодинамических процессов
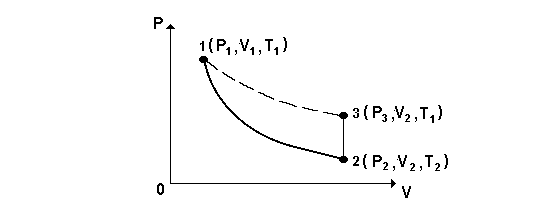
Этот процесс расширения газа происходит достаточно быстро, поэтому теплообменом с окружающей средой через стенки баллона можно пренебречь и считать процесс адиабатическим. Воздух в баллоне перейдет (рис. 3) в состояние 2 с параметрами: p2, V2, T2, причем V2 >V1, а Т2 < T1. Будем считать, что V2 – это объем баллона. При адиабатическом расширении часть воздуха выходит в атмосферу, поэтому необходимо иметь в виду, что V1 – это объем воздуха в состоянии 1, несколько меньший объема баллона (на величину, которую занимает воздух при давлении p1, вышедший в атмосферу при открывании крана).
Связь между состояниями 1 и 2 определяется уравнением Пуассона
![]() ,
,
с другой стороны,
![]()
![]()
Отсюда легко получается зависимость между давлением и температурой газа в этих состояниях
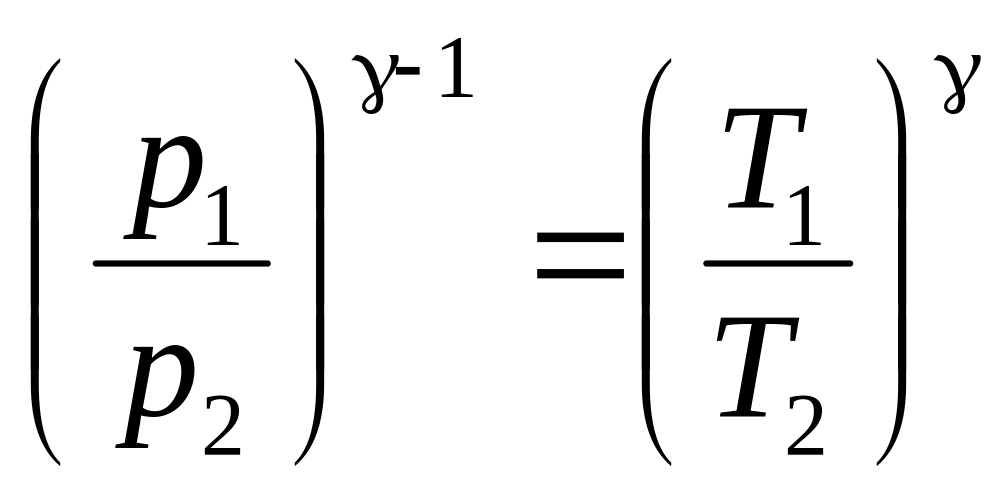 . (6)
. (6)
В дальнейшем (после закрытия клапана) воздух в баллоне изохорически нагревается до температуры окружающей среды T1, а давление повысится до значения p3, которое превысит атмосферное p0 на небольшую величину p, т.е. воздух переходит (рис. 3) в состояние 3 с параметрами: p3, V2 , T1, при этом p3 = p0 + p’’ и p p0.
Связь между состояниями 2 и 3 находится из уравнения изохорического процесса
![]() (7)
(7)
Из формул (6) и (7) с учетом того, что p1 = p0 + p’, а p3 = p0 + p’’, получается

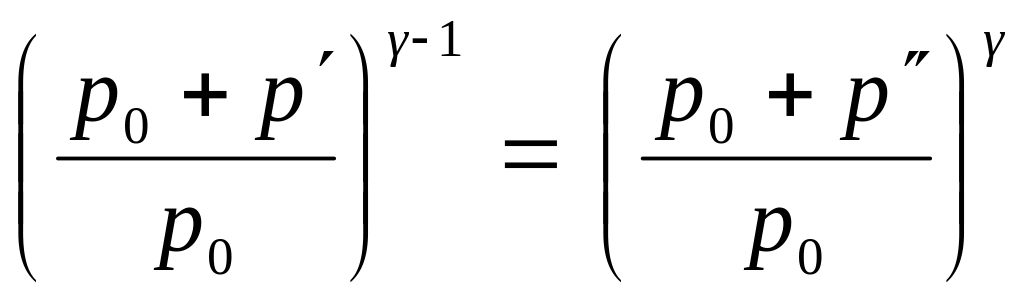 ;
;
![]() .
.
Так как p’ << p0 и p’’ << p0, то, разлагая оба двучлена в ряд и ограничиваясь членами первого порядка, получаем
![]()
откуда
![]() (8)
(8)
Давления p и p измеряются с помощью жидкостного манометра.
Учитывая,
что давление столба жидкости пропорционально
плотности жидкости
![]() и высоте столба
h,
величины p
и p
можно выразить следующим образом:
и высоте столба
h,
величины p
и p
можно выразить следующим образом:
![]() ;
;
![]() (9)
(9)
где g – ускорение свободного падения.
Подставляя (9) в (8), получим расчетную формулу для определения γ
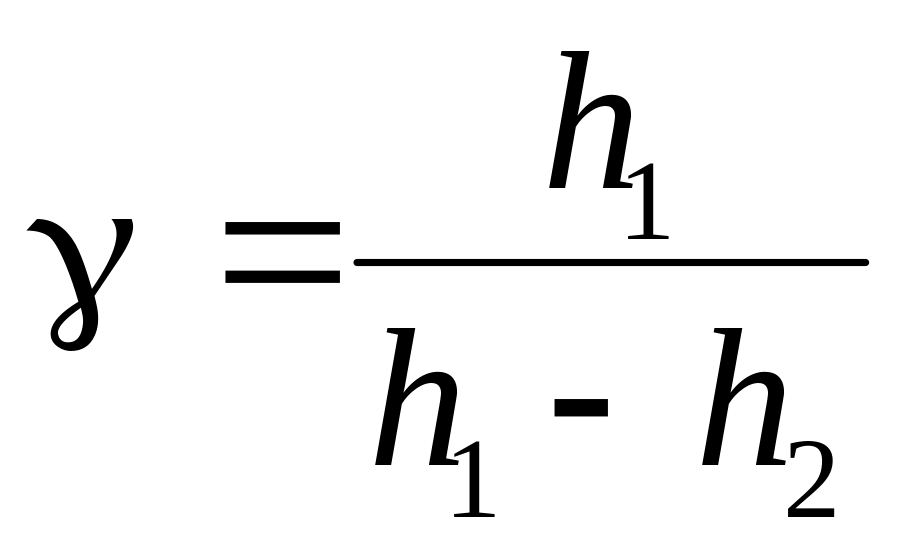 .
(10)
.
(10)
3. Работа при адиабатическом процессе
В данной работе также определяется работа при адиабатическом расширении газа на участке кривой 1–2 (рис. 3).
Адиабатическим называется процесс, происходящий без теплообмена с окружающей средой (Q = 0).
Из первого начала термодинамики для адиабатического процесса следует, что
![]() (11)
(11)
т.е. газ, адаиабатически расширяясь, совершает работу против внешних сил за счет уменьшения своей внутренней энергии, при этом его температура уменьшается, что видно из формулы (11) (A > 0, поэтому T2 < T1).
В формуле (11) работа адиабатического расширения газа определена через изменение температуры. Однако в этом процессе меняется не только температура, но и давление, и объем. Выразим работу через изменение этих параметров.
Учитывая
формулу (6), а также
![]() получим
получим
![]()
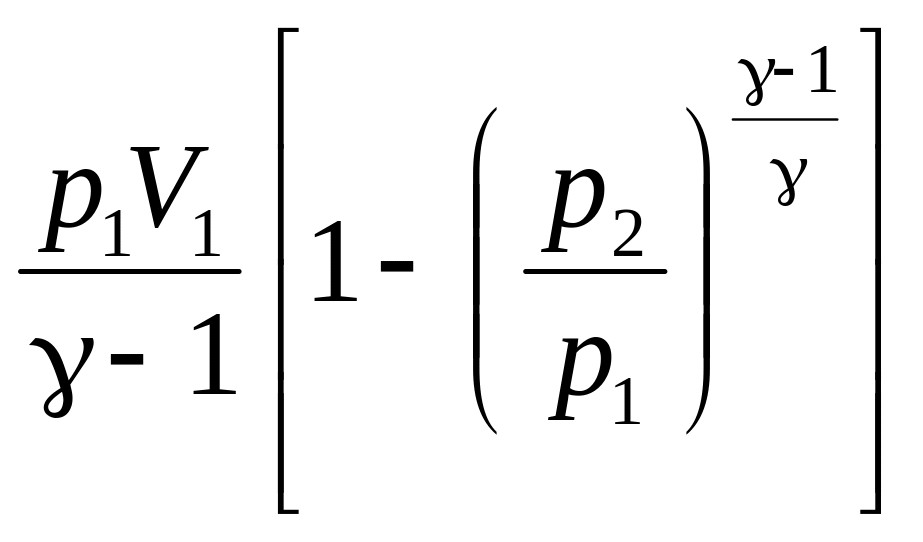 (12)
(12)
или, заменяя p1 = p0 + p и p2 = p0 , находим
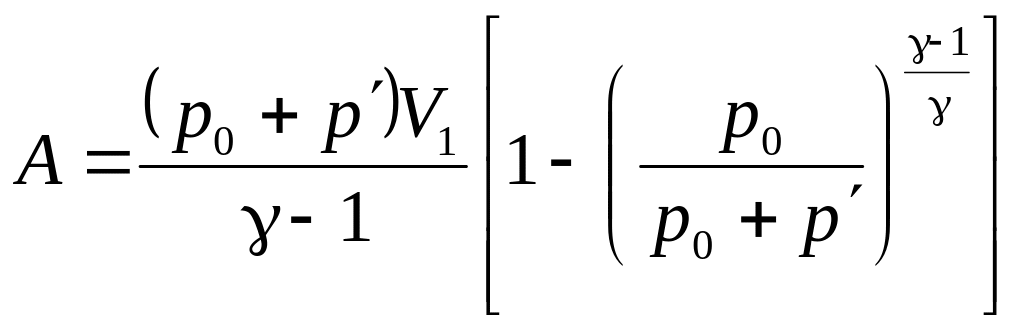 .
(13)
.
(13)
Принимая во внимание, что p p0, разложим выражение, стоящее в скобках, в ряд и, ограничиваясь первыми слагаемыми ряда, получим
 .
.
Тогда формула (13) примет вид

Учитывая,
что
![]() и p
<< p0,
можно пренебречь членом
(p’)2
V1
в числителе и
и p
<< p0,
можно пренебречь членом
(p’)2
V1
в числителе и
![]() – в знаменателе последнего выражения,
окончательно получим расчетную
формулу для работы при адиабатическом
расширении газа в рассматриваемом
случае
– в знаменателе последнего выражения,
окончательно получим расчетную
формулу для работы при адиабатическом
расширении газа в рассматриваемом
случае
![]() , (14)
, (14)
где V1 первоначальный объем газа, который хотя и меньше объема баллона V2 , но на небольшую величину. Поэтому при расчете работы за величину V1 принимаем объем баллона. Величина ρ плотность жидкости (воды) в манометре.
