
Белозеров В.И. Учебное пособие по курсу Техническая термодинамика (исправлено)
.pdf
Для любого термодинамического процесса представляет интерес отношение изменения внутренней энергии u к количеству подведенного или отведенного тепла q
|
|
u |
||
|
|
|
|
. |
|
|
|
||
|
|
q |
||
Для изохорного процесса |
u |
1. |
||
|
||||
|
q |
|||
6.2. Изобарный процесс
Изобарным называется такой процесс изменения состояния рабочего тела, при котором давление его остается постоянным. Линия, изображающая этот процесс графически, называется изобарой.
|
P |
|
|
a) |
Ò |
|
|
v = const |
á) |
|
|
|
|
|
|
|
|
||
|
|
-q |
+q |
|
|
|
|
|
|
|
|
|
|
|
|
|
T |
2 |
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
2χ |
|
|
|
|
|
|
|
p = const |
|
1 |
2 |
|
2χ |
T |
1 |
|
|
|
1 |
2 |
|
|
|
1 |
|
|
|
|
P |
= P |
|
|
|
|
|
|
|
|
|
|
-l |
+l |
|
|
|
|
+q |
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
-q |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
v χ |
v |
v |
v |
|
|
S |
S |
S |
|
2 |
1 |
|
2 |
|
|
1 |
2 |
|
|
|
|
|
|
Ðèñ. 6.2.1 |
|
|
|
|
Связь между термическими параметрами начального и конечного состояний может быть получена из уравнения состояния идеального газа при P = const
v1 |
|
T1 |
, |
(6.2.1) |
|
|
v2 T2
откуда видно, что изобара нагревания направлена слева направо, изобара охлаждения – справа налево (рис. 6.2.1, а).
81

Аналитическое выражение первого закона термодинамики
|
v2 |
q |
u2 u1 ³Pdv |
|
v1 |
для изобарного процесса принимает вид |
|
q u2 u1 P v2 v1 |
u2 Pv2 u1 Pv1 h2 h1. (6.2.2) |
Таким образом, в изобарном процессе все подводимое тепло рас-
ходуется на изменение энтальпии газа.
Согласно определению теплоемкости
dq CP dT CP dt è q |
|
|
P T2 |
T1 |
CP t2 t1 , |
|
C |
(6.2.3) |
|||||
поэтому |
|
|
|
|
|
|
dh CP dt è h2 h1 |
CP T2 |
T1 |
CP t2 t1 . |
(6.2.4) |
||
Энтальпия является функцией состояния, и ее изменение не зависит от характера процесса, поэтому приведенные формулы справедливы для любого процесса.
В теплотехнических расчетах, учитывая изменение теплоемкости от температуры, для изобарного процесса можно записать
|
t2 |
t1 |
|
||
|
|
|
|
|
|
q C |
P t2 CP t1 . |
(6.2.5) |
|||
0 |
0 |
|
|||
Величина работы в изобарном процессе выразится по формуле
l |
P v2 v1 , |
(6.2.6) |
с учетом уравнения состояния идеального газа |
|
|
l |
R T2 T1 . |
(6.2.7) |
Уравнение (6.2.7) позволяет выяснить физический смысл газовой постоянной R: это работа расширения 1 кг идеального газа при изобарном нагревании его на один градус.
Если считать теплоемкость постоянной, то изменение энтропии определяется формулой
T2 |
dq |
T2 |
dT |
|
|
|
T |
|
|
S2 S1 ³ |
³CP |
|
|
|
|
|
|||
|
|
CP ln |
2 |
, |
(6.2.8) |
||||
T |
T |
T |
|||||||
T |
|
T |
|
|
|
|
1 |
|
|
1 |
|
1 |
|
|
|
|
|
|
|
82
с учетом (6.2.1)
S |
|
S |
|
|
|
ln |
v2 |
. |
|
|
2 |
C |
P |
(6.2.9) |
|||||||
|
||||||||||
|
1 |
|
|
|
v1 |
|
||||
|
|
|
|
|
|
|
|
|||
Поскольку C > C , то, сравнивая формулы (6.2.8) и (6.1.5), видим,
Pv
что изобара идет более полого, чем изохора. Для изобарного процесса
u Cv T2 T1 Cv |
1 |
. |
|||||
|
|
|
|
|
|
|
|
q CP T2 T1 CP |
|
||||||
|
k |
||||||
6.3. Изотермический процесс
Изотермическим процессом называется такое изменение состояния рабочего тела, при котором температура остается постоянной.
Связь между термическими параметрами может быть получена из уравнения состояния идеального газа, если принять T = const:
Pv const. |
(6.3.1) |
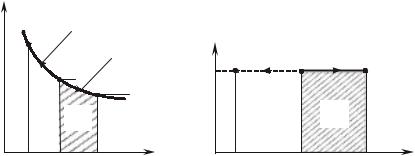
Линия, которая изображает изотермический процесс на Pv-диаг- рамме, называется изотермой (рис. 6.3.1, а).
Поскольку в изотермическом процессе
u2 u1 Cv T2 T1 0, |
(6.3.2) |
т.е. внутренняя энергия не изменяется, аналитическое выражение
P |
|
|
a) |
|
|
|
|
|
|
|
|
|
|
|
|
2χ |
|
-q |
|
|
|
|
|
|
|
|
T |
|
|
á) |
|
|
|
|
|
|
|
|
|
|
|
|
+q |
2χ |
1 |
2 |
|
|
|
|
|
|
|||
|
1 |
P |
v |
= v |
|
|
|
|
|
1 |
|
|
|
||
|
|
1 |
2 |
|
|
|
|
|
|
|
|
|
|
||
|
|
2 |
P |
|
|
|
|
|
|
|
2 |
|
|
|
|
-l |
|
+l |
|
|
-q |
+q |
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
v χ |
v |
v |
v |
S χ |
S |
S |
S |
2 |
1 |
2 |
|
2 |
1 |
|
2 |
|
|
|
Ðèñ. 6.3.1 |
|
|
|
|
83

первого закона термодинамики принимает вид
v2 |
|
q ³Pdv l, |
(6.3.3) |
v1 |
|
т.е. все тепло, затраченное на процесс, расходуется на совершение работы изменения объема газа. Для идеального газа
PRT , v
следовательно,
v2 |
RT |
|
v |
(6.3.4) |
||
q l ³ |
|
dv |
RT ln |
2 |
. |
|
v |
v |
|
||||
v |
|
|
|
1 |
|
|
1 |
|
|
|
|
|
|
Полученное выражение показывает, что если v |
> v , òî q > 0 è |
|||||
|
|
|
|
2 |
1 |
|
l > 0. Это означает, что при подводе тепла газ расширяется, изотер-
ма направлена слева направо и работа его положительна. Если v < v ,
2 1
то q < 0 и l < 0, т.е. при отводе тепла газ сжимается, изотерма направлена справа налево и работа отрицательна.
Если в изотермическом процессе |
v2 |
|
|
P1 |
, òî |
|
|
|
|||||||||||||
v1 |
P2 |
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
q |
l |
RT ln |
P1 |
. |
|
|
|
(6.3.5) |
||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
P2 |
|
|
|
|
|
|
|||
Из рис. 6.3.1,б видно, что |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
q |
T S2 S1 |
|
|
|
|
|
(6.3.6) |
|||||||||
èëè S2 S1 |
q |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
, ò.ê. q = l, |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
T |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
тогда |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
RT ln |
v2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
S |
|
S |
v1 |
|
R ln |
v2 |
|
|
R ln |
P1 |
. |
(6.3.7) |
|||||||
|
|
|
|
|
|
|
|
||||||||||||||
|
|
2 |
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
1 |
T |
|
|
|
|
|
|
|
|
v1 |
|
|
|
P2 |
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
Для изотермического процесса |
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
u |
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
0. |
|
|
|
|
|
|
|
|
(6.3.8) |
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
q
84
|
|
6.4. Адиабатный процесс |
|
|
||||||||
Адиабатным называется процесс изменения состояния рабоче- |
||||||||||||
го тела, протекающего без теплообмена с окружающей средой. |
||||||||||||
Уравнение адиабаты может быть получено из аналитических |
||||||||||||
выражений первого закона термодинамики, которые в данном слу- |
||||||||||||
чае принимают вид |
|
|
|
|
|
|
|
|
|
|
||
dq |
du Pdv |
Cv dT Pdv |
0, |
|
dq |
|
dh vdP |
CP dT vdP |
0, |
|||
откуда |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Cv dT Pdv, |
|
|
|||||
|
|
|
|
|
CP dT vdP. |
|
|
|||||
Разделив первое уравнение на второе, получаем |
|
|||||||||||
|
|
|
|
|
CP |
|
vdP |
, |
|
|
||
|
|
|
|
|
Cv |
|
Pdv |
|
|
|||
|
|
|
|
|
|
|
|
|
|
|||
CP |
k, ò.å. k |
|
|
vdP |
|
dP |
k |
dv |
|
|
||
ãäå |
|
Pdv |
èëè |
|
|
|
0. |
|
|
|||
Cv |
|
|
|
|
P |
|
|
v |
|
|
||
Интегрируя это уравнение, получаем |
|
|
|
|
||||||||
|
|
|
|
ln P k ln v |
const |
|
|
|||||
èëè |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Pvk |
|
const. |
|
(6.4.1) |
|||
|
P |
|
|
|
|
a) |
|
T |
|
á) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2χ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Изотерма |
|
|
|
|
2χ |
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
P |
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
T |
1 |
|
|
|
|
|
|
P |
|
|
|
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
1 |
|
|
|
|
|
|
|
-l |
+l |
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
T |
|
|
|
|
|
|
|
|
|
|
|
|
2 |
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
v χ |
v |
|
v |
|
v |
|
|
|
|
|
S |
|
|
|
|
|
|
|
|
|
||||
|
2 |
1 |
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
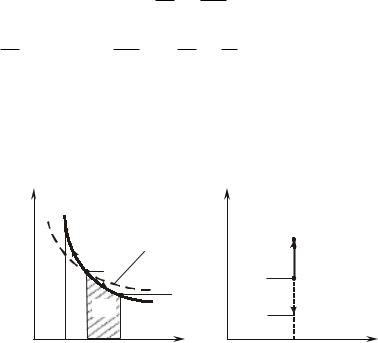
Ðèñ. 6.4.1 |
|
|
|
|||
85
Полученное соотношение называют уравнением Пуассона или уравнением адиабаты.
Графически адиабата, изображаемая линией 1-2, несколько кру- че изотермы, т.к. k > 1 (рис. 6.4.1,а).
В адиабатном процессе все три термических параметра (P, v, T) переменны, поэтому связь между их значениями для начального и конечного состояний газа выражается тремя уравнениями:
• между P и v из уравнения адиабаты (6.4.1)
P |
§ v |
·k |
|
||
1 |
¨ |
2 |
¸ |
; |
(6.4.2) |
P2 |
|
||||
© v1 |
¹ |
|
|
||
• между T и v: сопоставляя формулы (6.4.1) и уравнение состояния идеального газа Pv = RT, получаем
|
RT1 |
vk |
RT2 |
vk |
èëè T vk 1 |
T vk 1 |
||||||||||||||||
|
|
|
|
|||||||||||||||||||
1 |
|
|
v2 |
2 |
|
|
|
|
|
|
1 |
1 |
|
|
2 |
2 |
||||||
|
v1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
и окончательно |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
T |
|
§ v |
·k 1 |
|
|
||||||||||
|
|
|
|
|
|
|
1 |
|
|
¨ |
|
2 |
|
¸ |
|
; |
|
(6.4.3) |
||||
|
|
|
|
|
|
|
T2 |
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
© v1 ¹ |
|
|
|
|
|
|||||||||
• между P и T: из формул (6.4.2) и (6.4.3) получаем |
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|
|
|
|
|
1 |
|
|
||
|
|
|
v |
§ P · |
|
|
|
§ T |
· |
|
|
|
|
|||||||||
|
|
|
k |
|
|
k 1 |
|
|
||||||||||||||
|
2 |
|
¨ |
1 |
¸ |
|
|
|
¨ |
|
1 |
¸ |
|
|
, |
|
||||||
|
|
|
v1 |
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
© |
P2 ¹ |
|
|
|
©T2 ¹ |
|
|
||||||||||||
откуда окончательно находим |
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
§ P · |
k 1 |
|
|
|||||||
|
|
|
|
|
|
|
T |
|
k |
|
|
|
||||||||||
|
|
|
|
|
|
1 |
|
|
|
¨ |
|
1 |
|
¸ . |
|
(6.4.4) |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
T2 |
|
© P2 ¹ |
|
|
|
|
|
|||||||||
Аналитическое выражение первого закона термодинамики для адиабатного процесса q = u – u + l = 0 или
21
u1 u2 l. |
(6.4.5) |
Это означает, что работа изменения объема в адиабатном процессе совершается за счет изменения внутренней энергии. Если газ
86

расширяется и работа положительна, то внутренняя энергия уменьшается; если происходит сжатие и работа газа отрицательна, то внутренняя энергия увеличивается, поэтому адиабатное расширение сопровождается уменьшением температуры газа, а адиабатное сжатие – ее увеличением.
Поскольку для любого процесса
u1 u2 Cv T1 T2 ,
то работа адиабатного процесса может быть найдена по формуле
|
|
l |
|
Cv T1 T2 , |
|
(6.4.6) |
|||||||
à ò.ê. C |
R |
, òî |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
v |
k 1 |
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
l |
|
R |
|
T |
T |
|
|
(6.4.7) |
|||
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
k 1 |
1 |
2 |
|
|
|
|||
èëè |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
l |
|
1 |
|
Pv |
P v |
. |
(6.4.8) |
||||
|
|
k 1 |
|||||||||||
|
|
|
1 |
1 |
2 |
2 |
|
|
|||||
Изменение энтропии в адиабатном процессе равно нулю, так как
dq TdS 0,
следовательно, S – S = 0 и S = S = S = const. В TS-координатах (рис. 6.4.1,б) адиабата изображается прямой 1-2 (адиабата расширения) и 1-2χ – (сжатия).
Для адиабатного процесса
u u
ρφ . (6.4.9)
q0
6.5.Политропный процесс
Кроме рассмотренных существуют процессы, у которых хотя и
нет вышеуказанных ограничений, но величина |
u |
|
|
в течение |
|
|
||
|
q |
|
данного процесса остается неизменной. Такие процессы называются политропными.
87

Уравнение политропного процесса
Pvn const , |
(6.5.1) |
где п – показатель политропы, изменяющийся для различных процессов от 0 до ±φ.
Для одного и того же процесса показатель политропы n – величи- на постоянная.
Рассмотрим уравнение (6.5.1) при некоторых значениях п:
•при n = 0 получаем Pv0 = P = const – изобарный процесс;
•при n = 1 получаем Pv = const – изотермический процесс;
•при n = k получаем Pvk = const – адиабатный процесс;
ρ |
1 |
|
ρ |
1 |
|
• ïðè n ρφ P φ v |
const (ò.ê. P φ 1, то v = const) – изохорный |
||||
процесс. |
|
|
|
|
|
Таким образом, рассмотренные основные термодинамические процессы являются частными случаями политропных процессов (при условии, что теплоемкость в этих процессах принимается постоянной).
Изобразим политропные процессы в Pv-координатах при различ- ных показателях политропы n (рис. 6.5.1).
Адиабата делит все процессы в Pv-координатах на две группы:
•процессы, распложенные выше адиабаты; в этой группе процессов тепло подводится;
•процессы, расположенные ниже адиабаты; в этой группе процессов тепло отводится.
Уравнения политропы Pvn = const и адиабаты Pvk = const одинаковы по форме и отличаются только показателем, поэтому зависи-
P |
|
n = φ |
|
|
U > 0, n < 1 |
|
q > 0, n < k |
|
n = 0 |
q < 0, n > k |
1 > n > 0 |
|
|
|
n = 1 |
U < 0, n > 1 |
n = k |
n =+φ φ> n > k |
|
|
v |
Ðèñ. 6.5.1 |
|
88
|
|
Таблица 6.5.1 |
|
|
|
Изменение внутренней энергии |
Расширение газа |
Сжатие газа |
|
|
|
U > 0 |
n < 1 |
n > 1 |
|
|
|
U = 0 |
n = 0 |
n = 0 |
|
|
|
U < 0 |
n > 1 |
n < 1 |
|
|
|
Знак теплоты |
Расширение газа |
Сжатие газа |
|
|
|
q > 0 |
n < k |
n > k |
|
|
|
q = 0 |
n = k |
n = k |
|
|
|
q < 0 |
n > k |
n < k |
|
|
|
мости, выведенные для адиабатного процесса, остаются справедливыми и для политропного процесса при замене показателя k показателем n. Таким образом, зависимости между основными терми- ческими параметрами имеют вид
|
§ v ·n1 |
|
§ v |
|
·n |
|
§ P · |
n1 |
|
||||||||
T |
P |
|
T |
n |
|
|
|||||||||||
1 |
¨ |
2 |
¸ |
; |
1 |
¨ |
|
2 |
¸ |
; |
1 |
¨ |
1 |
¸ . |
(6.5.2) |
||
|
|
|
|
||||||||||||||
|
|
|
|
|
|
||||||||||||
T2 |
© v1 ¹ |
|
P2 |
© v1 ¹ |
|
T2 |
© |
P2 ¹ |
|
||||||||
Величина работы вычисляется по формулам
l |
R |
T |
T |
, l |
1 |
Pv |
P v |
. |
(6.5.3) |
|
|
||||||||
|
n 1 1 |
2 |
|
n 1 1 1 |
2 2 |
|
|
||
Согласно первому закону термодинамики для политропного процесса
q u |
|
u |
l Cv T |
T |
|
R |
|
T |
T |
|
§C |
|
|
R |
· |
T |
T |
. |
|
2 |
|
v |
|
|
¸ |
||||||||||||||
|
1 |
2 |
1 |
|
n 1 |
1 |
2 |
|
¨ |
|
n 1 |
2 |
1 |
|
|||||
|
|
|
|
|
|
|
|
|
© |
|
|
¹ |
|
|
|
||||
Сравнивая полученное выражение с формулой q = C(T – T ), на-
2 1
ходим зависимость
C Cv |
|
|
R nCv Cv R nCv CP |
|||||
|
|
|
|
|
|
|||
n 1 |
n 1 |
|
n 1 |
|||||
|
|
|
|
|
||||
или, учитывая, что |
CP |
k, |
|
|
|
|||
|
|
|
|
|
|
|||
Cv
89
C |
n k |
C . |
(6.5.4) |
|
|||
|
n 1 v |
|
|
Формулой (6.5.4) определяется теплоемкость политропного про-
цесса.
Логарифмируя уравнение политропы Pvn = const, получаем
|
|
lnP = nlnv = const |
|
|||||||||||
– прямая линия в логарифмических координатах или |
|
|||||||||||||
|
|
|
|
|
§ P · |
|
|
|
|
|
|
|||
|
|
|
|
|
ln ¨ |
1 |
¸ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
n |
© |
|
P2 ¹ |
. |
|
|
|
|
(6.5.5) |
||
|
|
|
|
§ v |
· |
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
ln ¨ |
|
2 |
¸ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
© v1 ¹ |
|
|
|
|
|
|
|||
Для политропного процесса величина |
|
|
|
|
|
|||||||||
D |
'u |
|
|
Cv T2 T1 |
|
|
n 1 |
. |
(6.5.6) |
|||||
|
|
|
n k |
|
|
|
|
|
|
|||||
|
q |
|
C |
|
T |
|
T |
n k |
|
|||||
|
|
|
|
|
|
|
||||||||
|
|
|
v n 1 |
2 |
1 |
|
|
|
|
|
||||
Изменение энтропии политропного процесса определяется по
формуле
S2 S1 |
C ln |
|
|
|
|
|
|
|
T2 |
, |
|
(6.5.7) |
|
|
|
T1 |
|
|||
|
|
|
|
|
|
|
где C – теплоемкость политропного процесса C |
C |
n k |
. |
|||
|
||||||
|
|
|
|
v n 1 |
||
6.6. Дросселирование. Эффект Джоуля–Томсона
Из опыта известно, если в трубе или в другом канале имеется сужение, а затем сечение увеличивается, то давление газа или жидкости за сужением будет всегда меньше, чем перед ним (рис. 6.6.1). Такое сужение называют местным сопротивлением.
Эффект падения давления струи рабочего тела в процессе протекания через сужение в канале называется дросселированием или
90
