
- •Обработка воды методом ионного обмена Физико-химические основы ионного обмена
- •Свойства ионитов
- •Натрий-катионирование
- •Водород-катионирование.
- •Анионирование воды
- •Фильтры смешанного действия
- •Технологические схемы ионитных установок
- •Очистка воды от растворенных газов
- •Удаление свободной углекислоты
Водород-катионирование.
При Н-катионировании обменными ионами являются катионы водорода. В процессе фильтрования из воды поглощаются все содержащиеся в ней катионы согласно ряду селективности, то есть Са2+, Mg2+, Na+ и другие, а в воду переходит эквивалентное количество Н+ ионов. Кроме того, происходит разрушение ионами водорода бикарбонатной щелочности воды с образованием свободной углекислоты. Протекают следующие реакции:
2HR + Ca(HCO3)2 CaR2 + 2H2O + 2CO2;
2HR + Mg(HCO3)2 MgR2 + 2H2O + 2CO2;
2HR + CaCl2 CaR2 + 2HCl;
2HR + MgSO4 MgR2 + H2SO4;
HR + NaCl NaR + HCl;
2HR + Na2SO4 2NaR + H2SO4.
В результате этих реакций общая жесткость снижается до 0,01 мг-экв/кг, а карбонатная жесткость [Са(НСО3)2 и Mg(НСО3)2] полностью удаляется, вследствие чего происходит устранение щелочности воды и снижение солесодержания. В процессе Н-катионирования все катионы заменяются катионами водорода Н+, а присутствующие в исходной воде соли: сульфаты, хлориды и нитраты кальция, натрия и другие, преобразуются в свободные кислоты: серную, соляную, азотную, кремниевую… Общая кислотность фильтрата равна сумме содержащихся в воде анионов минеральных кислот SO42–, Cl–, NO3– и др. Н-катионированная вода является кислой, непригодной для питания паровых котлов, поэтому этот метод всегда сочетают с Na- катионированием или анионированием, что дает возможность нейтрализовать кислотность и снизить щелочность обработанной воды.
Вследствие селективности удержания ионов катионитом, весь слой условно можно разбить на зоны по поглощаемым катионам. Ближе к нижней границе слоя располагается зона поглощения ионов Na+, над ней - смешанная зона поглощения Mg2+ и Na+, а еще выше - зона поглощения Са2+, Mg2+. Суммарная высота этих зон определяет величину рабочей зоны катионита. Над ней располагается слой истощенного катионита, а под ней - свежего.
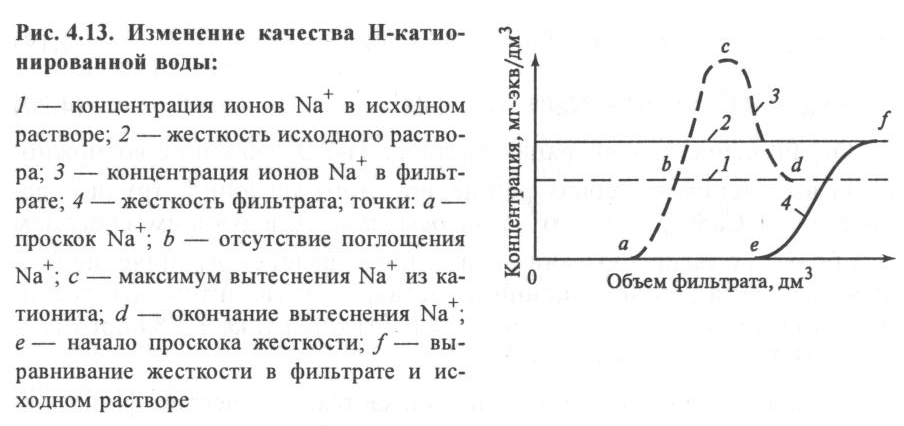
При работе Н-катионитного фильтра наблюдаются два периода. В первом происходит полное поглощение всех катионов до момента достижения зоной поглощения ионов Na+ нижней границы слоя катионита (работа до проскока Na+). В этот период кислотность фильтрата остается постоянной. Второй период начинается с проскока ионов Na+ в воду. С этого момента содержание Na+ в обработанной воде начинает возрастать, так как этот ион не может полностью улавливаться катионитом, пока не достигнет концентрации Na+ как в исходной воде. К этому моменту Н-катионит совсем прекращает поглощать Na+ из обрабатываемой воды и происходит только улавливание ионов Са2+ и Mg2+. Эти ионы Са2+ и Mg2+. наряду с обменом на ионы Н+ начинают вытеснять ранее поглощенные ионы Na+ из катионита, поэтому содержание Na+ в фильтрате становится больше его концентрации в исходной воде. Происходят одновременно процессы водород- и натрий-катионирования с постепенным переходом в Na-катионирование, так как ионы Н+ в катионите уже полностью заменены на ионы Na+, Са2+, Mg2+(точка О). Содержание натрия в фильтрате снижается по мере истощения катионита и возвращается к его концентрации в исходной воде по мере приближения проскока ионов жесткости Мg2+ (точка Р). Во втором периоде снижается кислотность фильтрата и начинает возрастать щелочность. При переходе в режим Na-катионирования щелочность восстанавливается полностью.
При умягчении воды Н-катионитные фильтры отключаются на регенерацию по проскоку ионов жесткости Са2+ и Mg2+ в фильтрат, а при химическом обессоливании - по проскоку катионов Na+, то есть при снижении кислотности фильтрата.
Эффект умягчения воды при Н-катионировании обычно столь же полный, как и при Na-катионировании. Он зависит от качества регенерации ионита, его природы и состава исходной воды. Регенерация производится 1...1,5 % раствором серной кислоты, как более дешевой и удобной по сравнению с соляной. Последняя также может применяться для регенерации (например, для вод с высоким содержанием Na+). Реакции регенерации описываются следующими уравнениями:
СаR2 + H2SO4 2HR + CaSO4;
MgR2 + H2SO4 2HR + MgSO4;
2NaR + H2SO4 2HR + Na2SO4.
При регенерации катионита соляной кислотой продуктами регенерации являются хлориды кальция, магния, натрия, хорошо растворимые в воде. При использовании серной кислоты один из продуктов регенерации сульфат кальция (СаSO4) обладает ограниченной растворимостью и способен «загипсовывать» катионит. Это обстоятельство заставляет ограничивать крепость регенерационного раствора до 1...1,5 % или осуществлять ступенчатую регенерацию: сначала 1% раствором Н2SO4, а затем, когда основная масса Са2+ и Mg2+ вытеснена и опасности гипсования уже нет, более крепким 5...6 % раствором кислоты для более полного вытеснения поглощенных катионитом ионов. Скорость пропуска регенерационного раствора выбирают также исходя из условий предотвращения кристаллизации гипса, а не диффузии при обмене ионов, как при Na-катионировании. Для сокращения времени контакта раствора кислоты с катионитом скорость фильтрования принимают 10...15 м/ч. По этой же причине, а также во избежание усиления коррозии оборудования, не допускается повышение температуры обрабатываемой воды и регенерационного раствора.
Кислотность
Н-катионированной
воды, то есть концентрация в ней
противоиона Н+,
определяется разностью между суммой
всех анионов и щелочностью воды и зависит
от суммарной концентрации хлоридов и
сульфатов. Противоионный эффект заметно
проявляется в Н-катионированной
воде, которая содержит значительное
количество ионов SO![]() и Cl-.
Чем больше некарбонатная жесткость,
тем ниже рН фильтрата, тем сильнее
противоионный эффект. В этом случае
сильно подавляется диссоциация особенно
слабокислотного катионита и уменьшается
рабочая обменная емкость Н-катионита.
Обменная емкость и эффект умягчения
воды зависят лишь от концентрации
нейтральных солей, так как бикарбонаты
кальция, магния и натрия не повышают
концентрацию противоиона в фильтрате.
Чем больше противоионный эффект, тем
больший требуется удельный расход
кислоты на регенерацию для достижения
заданной остаточной жесткости фильтрата.
Существенно снижается расход реагента
при применении противоточной регенерации
или двухступенчатого Н-катионирования.
и Cl-.
Чем больше некарбонатная жесткость,
тем ниже рН фильтрата, тем сильнее
противоионный эффект. В этом случае
сильно подавляется диссоциация особенно
слабокислотного катионита и уменьшается
рабочая обменная емкость Н-катионита.
Обменная емкость и эффект умягчения
воды зависят лишь от концентрации
нейтральных солей, так как бикарбонаты
кальция, магния и натрия не повышают
концентрацию противоиона в фильтрате.
Чем больше противоионный эффект, тем
больший требуется удельный расход
кислоты на регенерацию для достижения
заданной остаточной жесткости фильтрата.
Существенно снижается расход реагента
при применении противоточной регенерации
или двухступенчатого Н-катионирования.
Иногда применяется
«голодная
регенерация»
Н-катионитных
фильтров. В этом случае при катионировании
происходит не глубокое умягчение
исходной воды, а разрушение её карбонатной
щелочности без образования кислого
фильтрата. Это достигается тем, что
фильтры регенерируются таким количеством
кислоты, которого недостаточно для
вытеснения всех катионов, ранее
поглощенных из воды. Это приводит к
расположению в верхних частях фильтрующего
слоя обменного иона Н+
водорода (отрегенерированный слой), а
в нижних слоях- обменных катионов кальция
и магния. В слоях, находящихся в Н+-форме
протекают реакции обмена улавливаемых
из воды ионов на ионы водорода, который
переходит в воду с образованием сильных
кислот и угольной кислоты. В ниже
расположенных слоях ионы водорода
сильных кислот обмениваются на ионы
кальция, магния, натрия. Слабая угольная
кислота, диссоциация которой подавлена
в присутствии сильных кислот, значительную
часть слоя проходит «транзитом» и
обменивает некоторое количество ионов
водорода уже в нижних слоях, обусловливая
появление щелочности. С течением времени
количество обменных ионов Н+
уменьшается и одновременно происходит
их перемещение из вышележащих слоев в
нижележащие. К моменту окончания рабочего
цикла все количество введенных при
регенерации ионов +
Н
Режим «голодной регенерации» отличается от других режимов регенерации с недостатком кислоты тем, что на протяжении всего рабочего цикла обеспечивается нулевая кислотность фильтрата и минимальная щелочность. Любые другие модификации регенерации с недостатком кислоты не обеспечивают этого требования.
Такой режим применяется в схемах подготовки подпиточной воды для тепловых сетей.
