
- •Экология
- •Часть 1 Элементы общей и социальной экологии
- •Введение
- •Автор лекция 1 возникновение и развитие экологии как науки
- •Источники и слагаемые современной экологии
- •Гигиена Экология человека
- •Сельское хозяйство и окружающей среды
- •Методы экологии
- •Иерархия понятий
- •Лекция 2 биосфера
- •Физиологические свойства живого
- •Механизмы стабилизации живых систем
- •Химические особенности живых организмов
- •Термодинамика биологических систем
- •Строение биосферы
- •Основные функции биосферы
- •Действие принципа Ле Шателье в биосфере
- •Лекция 3 экосистемы
- •Пищевые цепи и сети
- •Развитие экосистем и проблема устойчивости
- •Лекция 4 взаимоотношения организма и среды
- •Общие закономерности действия экологических факторов на живые организмы Действие абиотических факторов
- •Совместное действие абиотических факторов
- •Экологическая ниша
- •Общие закономерности действия биологических факторов
- •Лекция 5 элементы экологии человека и социальной экологии
- •Среда жизни современного человека
- •Адаптации человека
- •Потребности человека
- •Влияние типа экологического сознания человека на природопользование
- •Лекция 6 антропогенное воздействие на биосферу
- •Загрязнение атмосферы
- •Кислотные осадки
- •Изменение концентрации озона в стратосфере и образование озоновых дыр
- •Парниковый эффект
- •Лекция 7 антропогенное воздействие на гидросферу
- •Классификация загрязнений
- •Характеристика основных гидрополлютантов
- •Самоочищение и эвтрофикация водоёмов
- •Лекция 8 антропогенное воздействие на литосферу, педосферу и биологические ресурсы
- •Ресурсный аспект взаимодействия человека и природы
- •Минеральные ресурсы
- •Воздействие человека на биологические ресурсы
- •Лекция 9 особенности современной экологической ситуации. Причины и перспективы возникновения глобального экологического кризиса
- •Известны три места, славящиеся своими долгожителями: Кавказ, Вилькабамба (Южный Эквадор), Хунза (северо-восточный Пакистан). Некоторые долгожители умирают в возрасте 160–168 лет.
- •Особенности роста народонаселения
- •Особенности современной экологической ситуации. Причины и перспективы возникновения глобального экологического кризиса
- •Особенности современной экологической ситуации
- •Библиографический список
- •Экология
Кислотные осадки
Постоянное поступление в атмосферу больших количеств оксидов серы и оксидов азота, а также изредка в результате аварийных выбросов хлористого водорода (HCl), приводит к кислотным осадкам. Основные источники таких выбросов – это продукты сгорания топлива (угля, мазута, бензина и т. д), выбросы химических и металлургических предприятий. Известно, что в нейтральной среде содержание ионов водорода pH = 7 (pH = - lg [H+]). Кислотными осадками называются дожди, туманы, снег, которые имеют pH < 7.
Оксиды серы и азота находятся в атмосфере достаточно длительное время, претерпевают ряд химических превращений и из них образуются серная и азотная кислоты. В атмосфере происходит много химических превращений, запишем только суммарные (брутто) реакции:
2SO2 + 2H2O + O2 → 2H2SO4
4NO2 + 2H2O + O2 → 4HNO3
4NO + 2H2O + 3O2 → 4HNO3
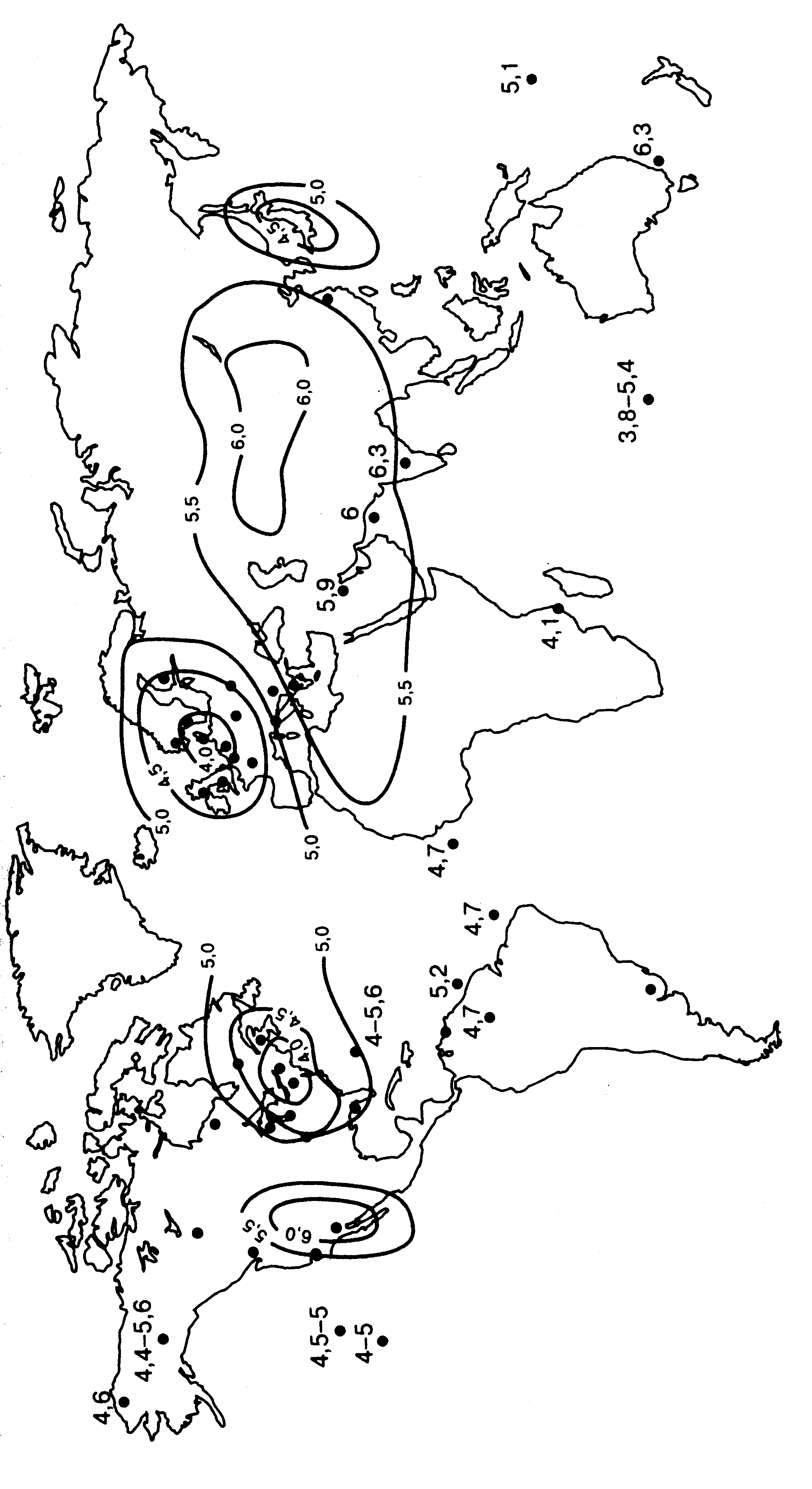
Самоочищение атмосферы происходит за счёт влажной и сухой седиментации (выпадения). Условия образования облаков – пересыщенность. Воздух содержит больше водяного пара, чем может при данной температуре. При подъёме воздушных масс вверх они остывают, и способность накапливать воду снижается. Начинается конденсация водяного пара. Капельки возникают только на частицах аэрозоля – ядрах конденсации. Ядрами конденсации выступают оксиды серы и азота. Таким образом, вода облаков – это ни в коем случае не чистая вода, а раствор атмосферных микроэлементов. Кислотные осадки антропогенного происхождения заметно изменили значение pH окружающей среды. Около 150 тыс. лет назад при образовании ледяного покрова Гренландии величина pH осадков составляла 6,0÷7,6 (по результатам анализов полярных льдов). Во второй трети XX века pH атмосферных осадков составляет 4,0-4,5 в Германии; 2,5÷2,7 в Шотландии и Норвегии; 4,0÷4,5 в США и Японии [3]. На рис. 7 приведена кислотность осадков на земном шаре [17]. Из рис. 9 видно, что разброс значений рН в основном заключён в интервале 4÷6,3. Тем не менее наблюдаются осадки как с более низким, так и с более высоким значением рН. Например, в Китае в 1981 г. зафиксированы осадки pH = 2,25. Специалисты считают, что это результат техногенной деятельности человека, так как за последние несколько сотен лет заметных изменений во вкладе в кислотные осадки со стороны природных процессов не происходило.
Сухие выпадения происходят под действием турбулентной диффузии, в осадок выпадают вещества, находящиеся в газообразном состоянии или адсорбированные на пылевидных частицах. Количество соединений серы, выпавших в сухой седиментации, в 2 раза больше, чем азота.

Скорость осаждения зависит от характера подстилающей поверхности. Больше всего она для влажной травы и кустарника до 30 мм/с. Средняя высота распределения диоксида серы и сульфатов для условий Европы составляет 1200–1500 м (не более 2000 м). Отдельные молекулы и частицы размером единиц мкм практически неоседаемы и могут поглощаться земной поверхностью.
Значение pH окружающей среды чрезвычайно важно с экологической точки зрения.
Это прежде всего процессы в живых организмах, связанные с действием ферментов, гормонов, регулирующих обмен веществ, рост и развитие. Особенно низкое значение рН сказывается на обитателях водоёмов и рек, где организмы адаптировались к pH = 6–7. В подкислённой среде гибнут яйцеклетки, молодь водных обитателей. Изменения затрагивают пищевые цепи, сокращая сначала популяции птиц и животных, питающихся обитателями вод, а затем и хищников.
Кислотные осадки вызывают деградацию лесов, особенно хвойных. Попадая на листья и хвою деревьев, кислоты разрушают защитный восковой налёт, что делает растения более уязвимыми для патогенных организмов, снижает их сопротивляемость болезням, способствует большему испарению влаги.
Под действием кислотных осадков существенно ускоряется коррозия металлов, нарушается целостность лакокрасочных покрытий, стёкол, разрушаются здания и памятники архитектуры. Из минеральных строительных конструкций и стёкол выщелачиваются карбонаты и силикаты.
При взаимодействии с почвенным покровом усиливается процесс выщелачивания биогенов. При pH < 4 снижается активность редуцентов и азотфиксаторов, обостряется дефицит питательных веществ и почвы теряют плодородие.
Выщелачиваются тяжёлые металлы из почв и горных пород, ранее находившиеся в нерастворимых соединениях. Повышается токсичность металлов, попадающих в реки и озёра. Например, в кислой среде возрастает растворимость Al(OH)3. При концентрации Al3+ > 0,3 мг/л среда становится токсичной для рыб.
