
Фармакология (Пособие для резидентуры)
.pdf
ЧАСТНАЯ ФАРМАКОЛОГИЯ
6.5.10.Разные препараты, применяющиеся для лечения припадков и эпилепсии
Выше рассматривались представители группы бензодиазепинов и их механизмы положительной аллостерической модуляции ГАМКА-рецепторов. Тем не менее, между ними имеются тонкие структурные различия и различия в их фармакокинетических свойствах. Однако два важных аспекта бен-
зодиазепинов ограничивают их применение в хронической терапии эпилепсии. Во-первых, их выраженный седативный эффект (у детей может возникнутьЦпарадоксальная гиперактивность, как в случае
с барбитуратами). Вторая проблема – толерантность. Вследствие этих причин бензодиазепины используются нечасто в хроническом лечении эпилепсии.
Диазепам, вводимый внутривенно, применяется для купирования эпилептического статуса. В
форме геля для ректального введения он предназначен для применения в отдельных случаях у пациентов, резистентных к антиэпилептической терапии, постоянно получающих противоэпилептические препараты, но нуждающихся в периодическом введении диазепама для купирования эпизодов
тяжелых эпилептических приступов. Долговременная терапия вызывает толерантность.
Лоразепам чаще используетсяЭпри лечении эпилептического статуса, потому что он имеет бо-
лее длительную продолжительность действия после внутривенной инъекции.
Клоназепам – это продолжительный бензодиазепин с наиболее сильнодействующей противо-
эпилептической активностью. Он эффективен для лечения абсансов, атонических и миоклонических судорог. Как и в случае других бензодиазепинов у него выражена седация, особенно вначале терапии.
Ингибиторы карбоангидразы. Карбоангидразы (КА) – это ферменты, которые катализи-
руют взаимопревращение между CO2 и бикарбонатом. Ингибиторы КА, особенно цитозольные формы КA II и КA VII, проявляют противоэпилептическую активность. Отток бикарбоната через ГАМКА- рецепторыГможет оказывать деполяризующее (возбуждающее) влияние, которое особенно важно во время интенсивной активации ГАМКА-рецепторов. Ингибирование КА предотвращает пополнение внутриклеточного бикарбоната и подавляет деполяризующее действие бикарбоната.
Прототипом ингибитора КА является сульфонамид ацетазоламид. Он обладает клинической противоэпилептической активностью против большинства типов судорог, включая фокальные, генерализованные тонико-клонические судороги и особенно генерализованные абсансы. Тем не менее, ацетазоламид редко используется для хронической терапии, потому что быстро развивается толерантность с возвратом судорог в течение нескольких недель.
Ацетазоламид, является диуретиком, вызывает гипонатриемию и гипокалиемию, а также ацидоз. Препарат часто используется при прерывистом лечении обострений менструальных припадков у женщин.
6.6. ПРОТИВОПАРКИНСОНИЧЕСКИЕ СРЕДСТВА
Противопаркинсонические средства применяют для лечения болезни Паркинсона (дрожательного паралича) и симптоматического паркинсонизма. Идиопатическая болезнь Паркинсона – хроническое, неуклонно прогрессирующее заболевание пожилых людей, при котором поражаются дофаминергические нейроны черной субстанции среднего мозга. В этиологии симптоматического паркинсонизма имеют значение нейроинфекции, атеросклероз мозговых сосудов, мозговой инсульт, травмы мозга, интоксикации /3/.
222

НЕЙРОТРОПНЫЕ СРЕДСТВА |
6 |
Выделяют, так называемый, лекарственный паркинсонизм, или нейролептический паркинсонизм, или псевдопаркинсонизм. Возникает, как правило, в течение 1–2 недель после начала терапии нейролептиком или увеличения его дозы, реже – через несколько недель или месяцев после начала терапии.
Так как вероятность развития паркинсонизма связана с блокированием дофаминовых D2-рецеп- торов, особенно часто паркинсонизм развивается при использовании сильнодействующих нейролептиков (галоперидол, фторфеназин, трифтазин). Он может развиваться и при приеме «мягких» нейролептиков (прохлорперазин). Хотя при применении атипичных нейролептиков (клозапин, кветиапин и др.) вероятность развития паркинсонизма сведена к минимуму, тем не менее, при применении некоторых из атипичных нейролептиков — рисперидона, оланзапина, зипрасидона и арипипразола —
При идиопатическом паркинсонизме происходит Цпотеря дофаминергических нейронов в черном веществе мозга, которая обычно ингибирует выработку ГАМКергических клеток в полосатом теле
развитие паркинсонизма возможно, особенно у пожилых людей.
Патогенез паркинсонизма связан с сочетанием нарушения расщепления белков, накопления и слипания белка внутри клеток, окислительного стресса, повреждений митохондрий, воспалительных каскадов и апоптозом. Исследования в области геномики идентифицировали мутации различных генов как причины развития болезни Паркинсона. Так, в настоящее время одной из причин признана синуклеинопатия. При этом возникают мутации гена α-синуклеина или дупликация и трипликация нормального гена синуклеина. Мутации в гене паркина (белок паркин маркирует поврежденные белки, с тем, чтобы клетки могли разрушить их, прежде чем они станут токсичными и играет ключевую роль в удалении из клеток дефектных митохондрий) вызывают раннее начало, аутосомнорецессивного, семейного паркинсонизма или спорадического ювенильного паркинсонизма. Мута-
ции в гене LRRK2 (leucine-rich repeat kinase 2, богатая лейцином повторная киназа 2) и в гене UCHL1
(ubiquitin C-terminal hydrolase L1, убиквитин С-терминальная гидроксилаза, убиквитин карбокси-
терминальная гидролаза-1) также являются распространенной причиной семейной болезни Паркинсо-
на. В этиологии заболевания играют роль экологические или эндогенные токсины.
Эпидемиологические исследования показывают, что табакокурение, кофе, употребление противовоспалительных препаратов, а также высокий уровень мочевой кислоты в плазме крови, являются защитными факторами, в то время как у лиц, работающих в сфере образования, здравоохранения или сельского хозяйства, у лиц, которые подвергаются воз-
действию свинца или марганца, или страдающих дефицитом витамином D заболеваемость увеличивается.
(рис. 6.7).
Норма |
|
|
|
Черное |
Полосатое |
|
|
вещество |
тело |
|
|
Дофамин |
|
|
|
|
|
АМК |
|
|
АцХ |
|
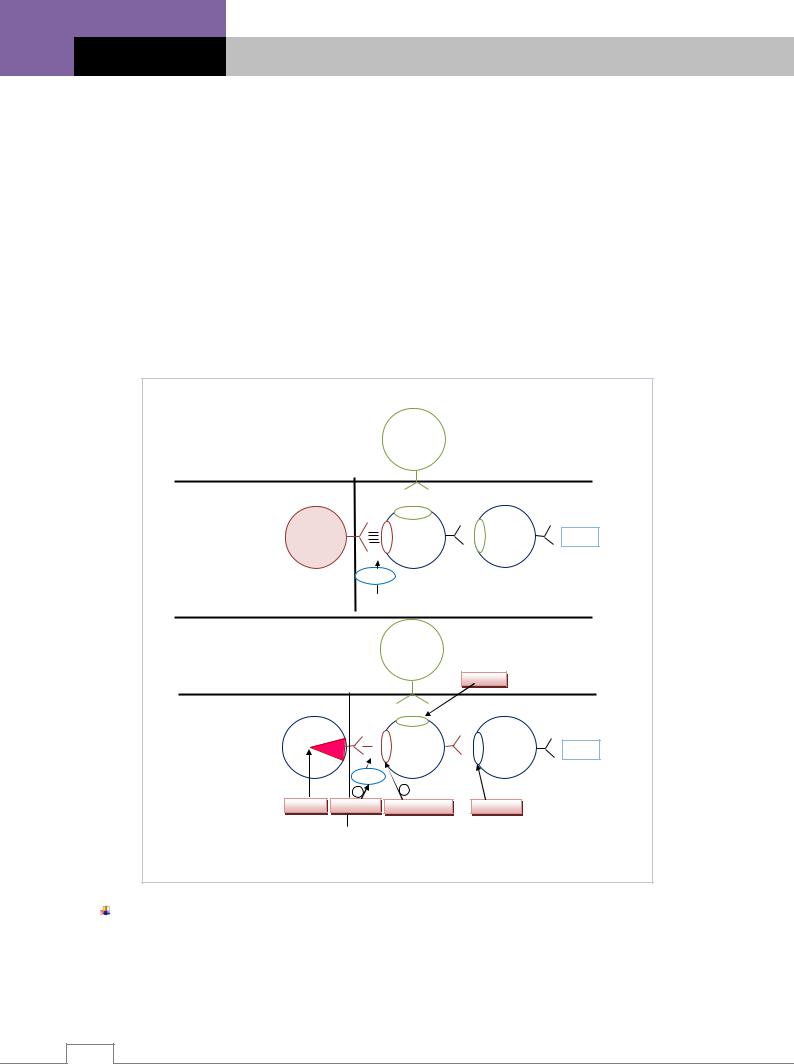
Рис. 6.7. Последовательность нейронов в |
|
Э |
нигростриатуме в норме и при |
|
|
|
||
Паркинсонизм |
|
|
паркинсонизме /8/. |
|
|
|
|
Г |
|
|
|
Паркинсонические расстройства обусловлены нарушением функций экстрапирамидной системы. |
|||
Центром экстрапирамидной системы является стриатум (хвостатое ядро и скорлупа). В нем представлены холинергические нейроны, несущие пресинаптические дофаминовые D2-рецепторы и
223

ЧАСТНАЯ ФАРМАКОЛОГИЯ
NMDA-рецепторы. Дофаминовые D2-рецепторы подавляют выделение ацетилхолина (ингибируют аденилатциклазу и снижают синтез цАМФ, активируют К+ каналы и блокируют Са2+-каналы нейронов), NMDA-рецепторы, наоборот, увеличивают. Дофамин выделяется из окончаний длинных аксонов дофаминергических нейронов, тела которых расположены в компактной части черной субстанции среднего мозга.
При болезни Паркинсона погибают 80–90% дофаминергических нейронов черной субстанции среднего мозга, первые симптомы появляются при гибели 50% нейронов. Дефицит дофамина в стри-
ВрезультатеГвосстановленияЭдофаминергической активностиЦв базальных ганглиях головного мозга с помощью агонистов леводопы и дофамина облегчаются многие двигательные нарушения. Аль-
тернативным и/или дополнительным подходом является восстановление нормального холинергического и дофаминергического баланса воздействием на базальные ганглии центральными М- холиноблокаторами.
Вклинической картине паркинсонизма преобладают следующие двигательные нарушения:атуме сопровождается избыточным выделением ацетилхолина. В итоге ослабляется регулирующее
ротонина в коре больших полушарий. При деменции в дофаминергических нейронах черной суб-
224

НЕЙРОТРОПНЫЕ СРЕДСТВА |
6 |
станции появляются тельца Леви (эозинофильные округлые образования, содержащие α-синуклеин), атрофируются гиппокамп и холинергические нейроны ядра Мейнерта.
Основные направления терапии болезни Паркинсона – активирование дофаминергических, угнетение глутаматергических и холинергических влияний (табл. 6.9).
Таблица 6.9. Классификация противопаркинсонических средств.
Вещества, активирующие дофаминергические влияния
a) предшественник дофамина |
|
Ц |
|
Леводопа |
|
б) дофаминомиметики |
|
Бромокриптин, Ропинирол, Ротиготин |
с) ингибиторы МАО В |
|
Селегилин |
Вещества, угнетающие глутаматергические влияния |
Мидантан, Гидантан |
|
Вещества, угнетающие холинергические влияния |
|
Тригексифенидил, Трипериден, |
|
|
Бипериден, Дифенилтропин |
6.6.1. Вещества, активирующие дофаминергические влияния
Для активации дофаминовыхЭD2-рецепторов, подавляющих выделение ацетилхолина в стриатуме, применяют средство заместительной терапии – предшественник дофамина леводопу, а также ингибиторы ферментов инактивации дофамина МАО В и КОМТ и прямые агонисты дофаминовых D-рецепторов /3/.
ПРЕДШЕСТВЕННИК ДОФАМИНА
Леводопа (L-диоксифенилаланин, ДОФА) является левовращающим стереоизомером дофами-
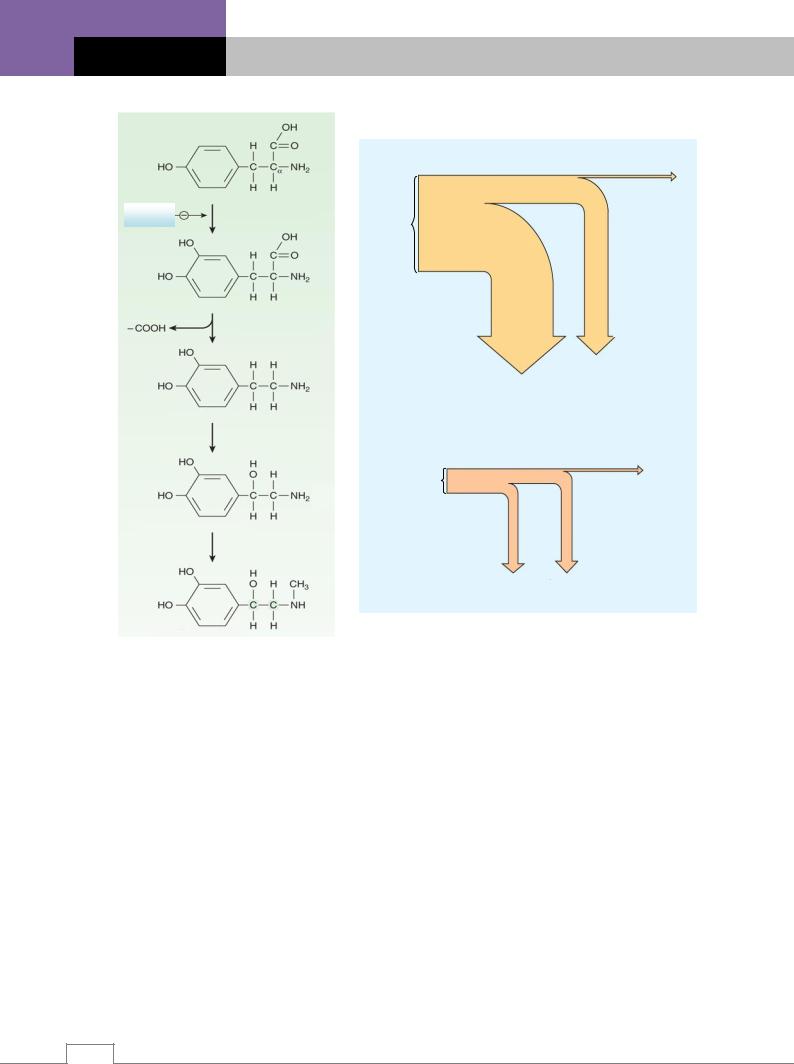
на. ДофаминГне проникает через Г Б и потому при попадании в периферическое кровообращение не имеет терапевтического эффекта при паркинсонизме. Однако леводопа, непосредственный метаболический предшественник дофамина, проходит в мозг посредством транспортера l-амино-кислоты, где она декарбоксилируется до дофамина (рис. 6.8).
Леводопа быстро всасывается из тонкого кишечника, всасывание зависит от скорости опорожнения желудка и рН желудочного содержимого. Прием пищи снижает концентрацию леводопы в плазме. Кроме того, аминокислоты пищи могут конкурировать с препаратом за всасывание из кишечника и транспортировку из крови в мозг. Основными продуктами обмена являются 3-метокси-4- гидроксифенилуксусная кислота (гомованиловая кислота) и дигидроксифенилуксусная кислота. Около 95% молекул леводопы декарбоксилируется с образованием дофамина в ЖКТ и эндотелии и только 5% дозы трансформируется в дофамин в головном мозге (1% – в стриатуме).
Для повышения доли леводопы, проникающей через ГЭБ, применяют комбинированные препараты с ингибиторами периферических ДОФА-декарбоксилаз – ароматическими L-аминокислотами карбидопой и бенсеразидом. Выпускают комбинированные препараты леводопы и карбидопы: наком, синдопа, тремонорм, тидомет форте, а также комбинированный препарат леводопы и бенсеразида – мадопар (рис. 6.9). Доза леводопы в составе комбинированных препаратов может быть сни-
жена на 60-80%.
Для повышения эффективности леводопы, устранения или уменьшения ее побочных эффектов, помимо использования ингибиторов периферической ДОФА-декарбоксилазы, применяют также ингибиторы КОМТ, например, энтакапон (комтан). Применение аналогичного препарата толкапона ограничено, так как у него выявлена выраженная гепатотоксичность.
225
ЧАСТНАЯ ФАРМАКОЛОГИЯ
|
|
|
|
|
|
Леводопа |
|
|
|
|
|
|
|
|
100% |
|
30% |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Мозг |
|
|
Тирозин |
|
|
|
Кровь |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Метиро- |
Тирозин гидроксилаза |
|
|
|
|
|
|
|
|
|
зин |
|
Доза |
Кишечник |
|
|
|
|
|
|
|
|
|
леводопы |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ДОФА |
|
|
|
|
|
|
|
|
|
|
Дофаминдекарбок- |
|
70% |
|
|
|
|
27–29% |
|
|
|
силаза |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Периферические |
|
|
|
|
|
|
|
|
Метаболизм в |
|
ткани |
|
|
|
|
|
|
|
|
ЖКТ |
|
(токсичность) |
|
|
|
|
ДОФА |
|
|
|
|
|
|
|
|
|
|
Дофамин -гидрок- |
|
Леводопа с карбидопой |
|
|
||||
|
|
силаза |
|
|
|
|||||
|
|
|
|
100% |
|
60% |
|
10% |
|
|
|
|
|
|
|
|
Кровь |
|
|
|
Мозг |
|
|
|
Доза |
Кишечник |
|
|
|
|
||
|
|
|
|
|
|
|
|
|||
|
|
|
леводопы |
|
|
|
|
|
|
|
|
|
Норэпинефрин |
|
|
|
|
|
|
|
|
|
|
Фенилэтаноламин-N-ме- |
|
|
40% |
|
50% |
|
|
|
|
|
тилтрансфераза |
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Метаболизм в |
Периферические |
|
|
||
|
|
|
|
|
|
ткани |
|
|
||
|
|
|
|
|
|
ЖКТ |
|
|
|
|
|
|
|
|
|
|
(токсичность) |
|
|
||
|
|
|
|
|
|
|
|
|
||
|
|
пинефрин |
Рис. 6.9. Фармакокинетика леводопы и |
|||||||
Рис. 6.8. Биосинтез катехоламинов. |
сочетание леводопы с карбидопой /8/. |
|||||||||
Ц |
|
|
|
|||||||
|
|
|
|
|
|
|||||
С Гназначения препаратовЭлеводопы начинают лечение в ранней стадии болезни Паркинсона у пациентов старше 70 лет, а также в поздней стадии во всех возрастных группах. Терапевтический эф-
фект наступает у 50–60% больных через несколько дней курсового применения.
В результате лечения уменьшаются ригидность, олигокинезия, дисфагия, слюнотечение. Тремор сохраняется, в начале лечения может даже усиливаться на фоне снижения мышечного тонуса.
Побочные эффекты препарата включают накопление дофамина и норэпинефрина в ЦНС и пе-
риферических органах. Возникает возбуждение, анорексия, рвота, боль в эпигастральной области,
тахикардия, аритмия, ортостатическая гипотензия, полиурия (ранние нарушения, появляющиеся в первые дни и недели терапии). Периферические дофаминомиметические эффекты можно устранить с помощью блокатора дофаминовых рецепторов домперидона (мотилиум).
Возможна повышенная тревожность, инсомния, ночные кошмары, депрессия, иллюзии, зритель-
ные галлюцинации, бред, когнитивные нарушения, дискинезии, гиперсексуальность. У молодых па-
циентов чаще возникают дискинезии, у пожилых выше вероятность психических нарушений. Галлю-
цинации сначала возникают в момент ночных пробуждений, но затем появляются и во время бодр-
ствования. Для уменьшения галлюцинаций и бреда используют атипичные антипсихотические сред-
ства клозапин, оланзапин.
226

НЕЙРОТРОПНЫЕ СРЕДСТВА |
6 |
Важно
|
|
|
Оланзапин и кветиапин при болезни Паркинсона могут усиливать гипокинезию. |
|
помнить! |
|
|
|
|
|
|
|
|
|
|
«Медовый месяц» для больного болезнью Паркинсона – так называется стабильный период эффекта леводопы, который сохраняется в течение 2–6 лет. После этого периода у 30–50% пациентов начинают развиваться побочные эффекты в двигательной сфере. Вначале появляется оральный гиперки-
нез (облизывание губ, оскаливание, причмокивание), затем присоединяются другие виды гиперкинезии: насильственные хореиформные, атетоидные, миоклоническиеЦили смешанные движения, акати-
зия, стереотипии, тики, дистонии. Болезненные дистонии протекают в виде кривошеи, писчего спазма, дистонии стоп. Двигательные нарушения сопровождаются парестезиями, депрессией, повышенной тревожностью вплоть до панической атаки, повышением АД, тахикардией.
В дальнейшем на фоне применяемой терапии появляются моторные флуктуации (чередование периодов нормальной двигательной активности «включение» и ее нарушений «выключение» в форме гипокинезии/акинезии) и дискинезии (насильственные непроизвольные движения, возникающие в различных группах мышц). Моторные флуктуации представлены следующими феноменами:
 «Дискинезия конца дозы» проявляется усилением двигательных симптомы болезни рано утром, до первого приема препаратаЭ. Феномен истощения дозы появляется уже в течение первых 2 лет терапии. Длительный прием леводопы приводит к накоплению в головном мозге 6-гидроксидофамина, повреждающего дофаминовые и адренергические нейроны.
«Дискинезия конца дозы» проявляется усилением двигательных симптомы болезни рано утром, до первого приема препаратаЭ. Феномен истощения дозы появляется уже в течение первых 2 лет терапии. Длительный прием леводопы приводит к накоплению в головном мозге 6-гидроксидофамина, повреждающего дофаминовые и адренергические нейроны.
 «Феномен изнашивания» или «wearing-off phenomenon» наступает примерно через 2–7 лет от начала терапии, т.е. лечебное действие леводопы ослабевает вследствие продолжающейся дегенера-
«Феномен изнашивания» или «wearing-off phenomenon» наступает примерно через 2–7 лет от начала терапии, т.е. лечебное действие леводопы ослабевает вследствие продолжающейся дегенера-
ции нейронов черной субстанции и уменьшения количества и чувствительности рецепторов дофамина.
 Синдром «включения-выключения», или «on-off phenomenon» синдром является неизменным следствием длительного лечения леводопой. В период «включения» симптомы болезни Паркинсона уменьшаютсяГ, но через 1–1,5 ч после приема препарата внезапно наступает «выключение» с возвратом ригидности и гипокинезии. Для предупреждения этих нежелательных синдромов рекомендуется поддерживать в крови постоянную концентрацию леводопы с помощью препаратов пролонгированного действия (мадопар), или приема леводопы в малых дозах каждые 4–6 ч, или применением леводопы совместно с дофаминомиметиками, ингибиторами МАО В, энтакапоном или амантадином. Для коррекции тяжелых форм дискинезий и дистоний назначают также ГАМК-ергические средства (седативные анксиолитики, баклофен).
Синдром «включения-выключения», или «on-off phenomenon» синдром является неизменным следствием длительного лечения леводопой. В период «включения» симптомы болезни Паркинсона уменьшаютсяГ, но через 1–1,5 ч после приема препарата внезапно наступает «выключение» с возвратом ригидности и гипокинезии. Для предупреждения этих нежелательных синдромов рекомендуется поддерживать в крови постоянную концентрацию леводопы с помощью препаратов пролонгированного действия (мадопар), или приема леводопы в малых дозах каждые 4–6 ч, или применением леводопы совместно с дофаминомиметиками, ингибиторами МАО В, энтакапоном или амантадином. Для коррекции тяжелых форм дискинезий и дистоний назначают также ГАМК-ергические средства (седативные анксиолитики, баклофен).
 Акинетический криз возникает при прекращении лечения, выраженном привыкании, нарушении всасывания леводопы (рвоте, диарее, отравлении, инфекциях), приеме дофаминовых блокаторов. Он проявляется полной иммобилизацией, грубым тремором, злокачественной гипертермией, нарушением бульбарных функций (дизартрией, дисфагией), рабдомиолизом, сердечной, дыхательной и почечной недостаточностью. Акинетический криз купируют внутривенным введением леводопы, бромокриптина или амантадина.
Акинетический криз возникает при прекращении лечения, выраженном привыкании, нарушении всасывания леводопы (рвоте, диарее, отравлении, инфекциях), приеме дофаминовых блокаторов. Он проявляется полной иммобилизацией, грубым тремором, злокачественной гипертермией, нарушением бульбарных функций (дизартрией, дисфагией), рабдомиолизом, сердечной, дыхательной и почечной недостаточностью. Акинетический криз купируют внутривенным введением леводопы, бромокриптина или амантадина.
 «Лекарственные каникулы» для леводопы (прекращение приема препарата на 3–21 день) могут временно улучшить ответ на леводопу и облегчить некоторые из ее побочных эффектов. Однако эта отмена несет в себе риск аспирационной пневмонии, венозного тромбоза, тромбоэмболии легочной артерии и депрессии вследствие неподвижности, сопровождающей тяжелый паркинсонизм. По этим причинам и из-за временного характера «лекарственные каникулы» не рекомендуется.
«Лекарственные каникулы» для леводопы (прекращение приема препарата на 3–21 день) могут временно улучшить ответ на леводопу и облегчить некоторые из ее побочных эффектов. Однако эта отмена несет в себе риск аспирационной пневмонии, венозного тромбоза, тромбоэмболии легочной артерии и депрессии вследствие неподвижности, сопровождающей тяжелый паркинсонизм. По этим причинам и из-за временного характера «лекарственные каникулы» не рекомендуется.
Для усиления и сохранения эффекта леводопу комбинируют с ингибиторами ДОФА-декарбок- силазы, ингибиторами КОМТ, дофаминомиметиками и др.
Новой технологией лечения болезни Паркинсона является непрерывная инфузия в двенадцатиперстную кишку суспензии леводопы и карбидопы в водном геле карбоксиметилцеллюлозы. Для
227
|
|
ЧАСТНАЯ ФАРМАКОЛОГИЯ |
|
|
|
|
|
|
||||||
|
инфузии проводят чрескожную эндоскопическую гастроеюностомию. При таком способе введения |
|||||||||||||
|
длительно сохраняется терапевтический эффект леводопы, реже развиваются флюктуации и дискинезии. |
|||||||||||||
|
Леводопа и препараты леводопы противопоказаны при психозах, атеросклерозе, артериальной |
|||||||||||||
|
гипертензии; тяжелых эндокринных, почечных, печеночных, сердечно-сосудистых, легочных заболе- |
|||||||||||||
|
ваниях; язвенной болезни (из-за опасности кровотечения), закрытоугольной глаукоме, заболеваниях |
|||||||||||||
|
крови, меланоме (ДОФА – предшественник меланина), беременности, грудном вскармливании, детям |
|||||||||||||
|
до 12 лет. Для лечения лекарственного паркинсонизма леводопу не используют, так как увеличение |
|||||||||||||
|
количества дофамина может спровоцировать состояние психоза. |
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
Ц |
|
||||
|
На время приема леводопы необходимо исключать из рациона питания продукты, богатые вита- |
|||||||||||||
|
мином В6 (авокадо, бобы, горох, печень, тунец), так как он служит кофактором периферических де- |
|||||||||||||
|
карбоксилаз ароматических L-аминокислот и может предотвратить терапевтический эффект леводо- |
|||||||||||||
|
пы. Действие комбинированных препаратов леводопы витамин В6 не ослабляет. Леводопу не следует |
|||||||||||||
|
назначать пациентам, принимающим ингибиторы МАО А, так как такая комбинация может приве- |
|||||||||||||
|
сти к гипертоническому кризу (рис. 6.10). |
|
|
|
|
|
|
|
|
|
||||
|
|
A |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Глутаматергический нейрон |
|
|
|
|
|||
|
|
Норма |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Э |
|
|
|
|
|
|
|||||
|
|
|
Черное вещество |
|
|
+ |
+ Глу |
|
|
Полосатое тело |
||||
|
|
|
|
|
|
|
|
NMDA |
АцХ |
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
ГАМК |
|
|
|
|
|
|
D |
|
|
|
D2 |
|
+ |
M |
- Моторные |
||
а |
|
|
|
|
|
|
|
|
+ |
- |
|
центры |
||
|
|
|
|
|
|
|
D |
|
|
|
|
|
|
|
|
|
|
Дофаминергический |
МАО-В Холинергичес- |
|
|
ГАМК- |
|
|
|||||
|
Г |
нейрон |
|
|
|
кий нейрон |
|
|
ергический нейрон |
|
|
|||
|
|
|
|
|
|
|
Глу |
|
|
|
|
|
|
|
|
Б |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Болезнь |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Паркинсона |
|
|
|
|
|
|
Мидантан |
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
Черное вещество |
|
|
|
+ |
+ |
|
|
Полосатое тело |
||||
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
NMDA |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
+ |
|
ГАМК |
|
|
|
|
|
|
|
|
|
|
|
|
|
- |
|
|
|
|
|
|
|
|
D |
|
D2 |
|
+ |
М |
- |
Моторные |
||
|
|
|
|
|
D |
|
+ |
- |
|
центры |
||||
|
|
|
|
|
|
|
|
|
+ |
|
|
|||
|
|
|
|
|
|
|
|
|
|
- |
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
МАО-В |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
- |
+ |
|
|
|
|
|
|
|
|
|
|
Леводопа |
|
Селегилин |
Бромокриптин |
|
Циклодол |
|
|
|||
|
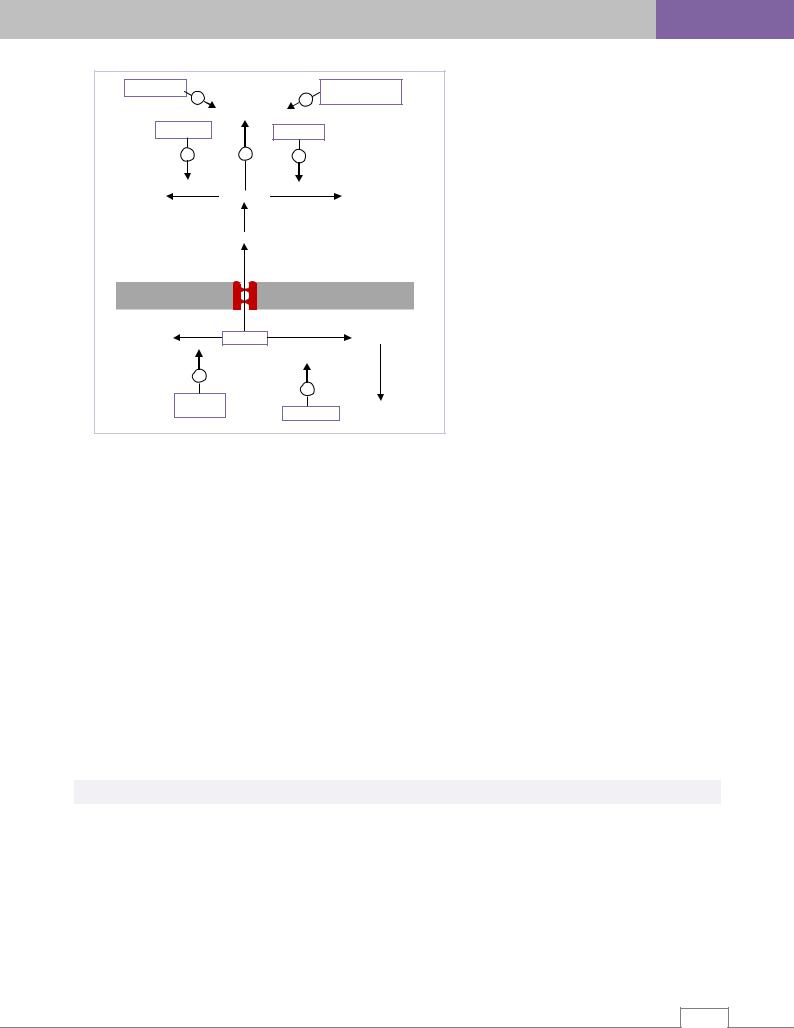
Рис. 6.10. Основная направленность действия противопаркинсонических |
|||||||||||||
|
|
|
|
|
|
средств (схема) /8/. |
|
|
|
|
|
|||
|
ДОФАМИНОМИМЕТИКИ |
|
|
|
|
|
|
|
|
|
|
|||
|
Бромокриптин (Парлодел). Полный агонист D2-рецепторов и частичный агонист D1-ре- |
|||||||||||||
|
цепторов. Уменьшает секрецию пролактина, подавляет лактацию, нормализует менструальную |
|||||||||||||
|
функцию, уменьшает продукцию гормона роста /3/. |
|
|
|
|
|
|
|||||||
|
По химическому строению это полусинтетическое производное алкалоида спорыньи эр- |
|||||||||||||
|
гокриптина (производное лизергиновой кислоты). |
|
|
|
|
|
|
|||||||
228

НЕЙРОТРОПНЫЕ СРЕДСТВА |
6 |
Принимается внутрь. Из ЖКТ всасывается около 30%. Большая часть инактивируется при первом прохождении печеночного барьера. Основной путь выведения – с желчью в кишечник.
Бромокриптин при приеме внутрь в суточной дозе 30 мг вызывает у 1/3 больных стойкое и существенное клиническое улучшение в течение 1 года. При увеличении дозы до 40 мг/сут монотерапию бромокриптином иногда удается продлить до 4–5 лет, но при этом развиваются тяжелые побочные эффекты. Бромокриптин, как правило, применяют в комбинации с леводопой.
Побочные эффекты включают тошноту, рвоту, ортостатическую гипотензию, психические нару-
шения, дискинезию и др. У больных возникает непереносимость этилового спирта. Редким осложне- Ц
нием при приеме бромокриптина является эритромелалгия – гиперемия, болезненность и отек кистей и стоп.
Ропинирол является агонистом D2- и D3-дофаминовых рецепторов. Противопаркинсониче-
ский эффект связывают с его влиянием на постсинаптические D2-дофаминовые рецепторы в неостриатуме. Угнетает секрецию пролактина. По эффективности при паркинсонизме ропинирол превосходит бромокриптин, так как является антидепрессантом.
Ропинирол, взаимодействуя с D2- и D3-рецепторами, обеспечивает адекватную коррекцию симптомов болезни Паркинсона у 60% больных на протяжении 3 лет. Препарат метаболизируется CYP1A2, другие препараты-субстраты этой изоформы могут значительно уменьшить его клиренс. Ропинирол выпускается в лекарственнойЭформе с пролонгированным высвобождением и принимается один раз в день.
Ротиготин – дофаминомиметик, применяющийся в форме ежедневной трансдермальной си-
стемы, обеспечивающей более постоянную дофаминергическую стимуляцию, чем пероральные препараты. Препарат одобрен для лечения ранней болезни Паркинсона. Преимущества и побочные эффекты аналогичны другим агонистам дофамина, но могут возникнуть реакции на месте приложения пластыря.
ДофаминомиметикиГмогут вызывать анорексию, тошноту, рвоту, которые практически отсутствуют при приеме с едой. В начале терапии развивается постуральная гипотензия. При длительном лечении возникает дозозависимый безболезненный вазоспазм пальцев, характерный для многих производных спорыньи.
Апоморфин гидрохлорид – эффективный неэрголиновый агонист дофамина, который взаимодействует с постсинаптическими D2-рецепторами в хвостатом ядре и скорлупе. Подкожные инъекции эффективны для временного облегчения («спасения») периодов акинезии у пациентов, находящихся на оптимизированной дофаминергической терапии. Препарат быстро всасывается в
кровь, а затем в мозг, эффект начинается в течение 10 минут после инъекции и продолжается до двух часов.
Основная проблема препарата – тошнота и рвота. Для предотвращения этих побочных эфектов перед введением апоморфина предварительно вводят противорвотный препарат триметобензамид в течение 3 дней.
Другие неблагоприятные эффекты апоморфина включают дискинезию, сонливость, бессонницу, боль в груди, потливость, гипотонию, обмороки, запоры, диарею, психические или поведенческие нарушения. Апоморфин не следует использовать у пациентов, принимающих антагонисты серотониновых 5-HT3-рецепторов, потому что может возникнуть тяжелая гипотония.
ИНГИБИТОРЫ МАО
Селегилин (Депренил). Является модифицированным амфетамином. Селегилин необра-
тимо ингибирует МАО В в астроцитах (в дозах до 10 мг не изменяет активности МАО А)11, препят-
11 Моноаминоксидаза А метаболизирует норэпинефрин, серотонин и дофамин, моноаминоксидаза В метаболизирует дофамин.
229

ЧАСТНАЯ ФАРМАКОЛОГИЯ
ствует окислительному дезаминированию дофамина и эндогенного дофаминомиметика фенилэтиламина (фенилэтиламин образуется в стриатуме, улучшает синаптическую передачу в коре больших полушарий, передачу нервного импульса по нервным волокнам, активирует рецепторы дофамина и его высвобождение из пресинаптических окончаний) в головном мозге, не нарушает инактивации тирамина, поступающего с пищей. С возрастом активность МАО В увеличивается.
Селегилин в дозе 0,5–1,0 мг препятствует апоптозу нейронов. Он стимулирует синтез нейротрофических факторов глиальными астроцитами, повышает экспрессию генов антиоксидантных фер-
ментов – супероксиддисмутазы и каталазы, угнетает выброс глутамата /5/.
Разагилин – другой ингибитор МАО B, являетсяЦболее сильным, чем селегилин препаратом и используется для раннего лечения пациентов с легкой симптоматикой. Препарат также используется в качестве дополнительной терапии для пролонгирования эффектов карбидопы-леводопы у пациентов с запущенной болезнью.
Обладает антидепрессивным действием, улучшает память и способность к обучению. Применяется на ранних стадиях болезни Паркинсона и в комплексной терапии с леводопой. Терапевтический
эффект селегилина развивается спустя 3–4 нед курсового приема.
Побочные эффекты: обусловлены образованием активного метаболита – метиламфетамина. Селе-
гилин может вызвать бессонницу.
Селегилин обладает нейропротекторным эффектом, уменьшая повреждение нейронов при ише-
мии и при воздействии ряда нейротоксических веществ. Частично это может быть связано с индукци-
ей фактора роста нервов, продуцируемого глиальными астроцитами. Имеются предварительные
клинические данные о благоприятном влиянии селегилина на состояние пациентов при таком нейродегенеративном заболеванииЭ, как болезнь Альцгеймера. Не исключено, что подобный эффект может проявляться и в отношении болезни Паркинсона.
Сафинамид – третий ингибитор МАО В используется для уменьшения моторных флуктуаций
(«wearing-off phenomenon» и «on-off phenomenon») у пациентов, принимающих карбидопу/леводопу. Для монотерапииГболезни Паркинсона препарат не эффективен.
Ингибиторы МАО В не следует принимать пациентам, принимающим меперидин, трамадол, метадон, пропоксифен, циклобензаприн или зверобой. Пациентам, принимающим ингибиторы МАО В, также следует избегать противокашлевой препарат декстрометорфан и все безрецептурные препараты, применяемые при простуде. Разагилин, селегилин или сафинамид не следует принимать с другими ингибиторами МАО и должны использоваться с осторожностью пациентами, получающими трициклические антидепрессанты или с ингибиторами обратного захвата серотонина из-за риска развития серотонинового синдрома (см. главу 7).
Комбинированное введение леводопы и ингибиторов МАО А и В может привести к гипертоническиму кризу, вероятно из-за накопления норэпинефрина в периферических тканях.
ИН ИБИТОРЫ КОМТ
Ингибирование ДОФА-декарбоксилазы связано с компенсаторной активацией других путей метаболизма леводопы, особенно катехол-О-метилтрансферазы (КОМТ), а это повышает уровень 3-О-метилдофы (3-ОМД) в плазме. Повышенный уровень 3-OMД вызывает плохую терапевтическую реакцию на леводопу, так как 3-OMД конкурирует с леводопой за активный носитель, транспортирующий ее через слизистую оболочку кишечника и ГЭБ. Селективные ингибиторы КОМТ, такие как толкапон и энтакапон продлевают действие леводопы путем снижения ее периферического метаболизма (рис. 6.11).
В результате клиренс леводопы уменьшается, относительная биодоступность леводопы повышается. Эти препараты могут быть полезны у пациентов, у которых развились моторные флуктуации на фоне лечения леводопой.
230
|
|
|
|
|
|
|
|
НЕЙРОТРОПНЫЕ СРЕДСТВА |
6 |
Ропинирол |
|
|
|
|
Бромокриптин, |
|
|
||
|
|
|
|
|
перголид |
|
|
||
|
+ |
Дофаминовый |
+ |
|
|
||||
|
|
|
|
|
|
||||
|
|
|
|
рецептор |
|
|
|
|
|
Селегилин |
|
|
|
Толкапон |
|
|
|
||
|
|
|
|
|
|
|
|
||
|
- |
|
|
+ |
|
- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
МАО-В |
Дофамин |
КОМТ |
3-ОМД |
|
|
|||
ДОФУК |
|
|
|
|
|
||||
|
|
|
|
ДOФA-декарбоксилаза |
Рис. 6.11. Механизмы действия |
||||
|
|
|
|
|
|
|
|
||
|
|
|
L-ДОФА |
|
|
|
противопаркинсонических средств. |
||
|
|
|
|
|
|
|
|
||
Мозг |
|
|
|
|
Транспортер L-аминокислот |
ДОФУК – дегидрооксифенилуксусная |
|||
|
|
|
|
|
|
|
кислота; 3-ОМД – 3-О-метилдофа /8/. |
||
|
|
|
|
|
|
|
|
||
ГЭБ |
|
|
|
|
|
|
|
|
|
Периферия |
|
|
|
|
|
|
|
|
|
3-ОМД |
КОМТ |
|
Леводопа |
|
|
Дофамин |
|
|
|
|
|
|
|
ДOФA-декар- |
|
|
|||
|
|
|
|
|
|
|
|||
|
|
|
|
|
боксилаза |
|
|
|
|
|
- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
- |
|
|
|
|
Энтакапон |
|
|
|
Побочные |
|
|
||
|
Толкапон |
|
|
Карбидопа |
|
|
|||
|
|
|
|
|
эффекты |
|
|
||
|
|
|
|
|
|
|
|
|
|
Толкапон имеет как центральные, так и периферические эффекты, в то время как энтакапон об- |
|||||||||
ладает периферическими эффектами. Применение толкапона ограничивает гепатотоксичность. |
|||||||||
Фармакокинетика препаратов одинакова, оба быстро всасываются, связываются с белками плазмы |
|||||||||
и метаболизируется до экскреции. Период полураспада обоих препаратов составляет около 2 часов, |
|||||||||
но толкапон имеет более длительную продолжительность действия. |
|
||||||||
Неблагоприятные эффекты ингибиторов КОМТ частично связаны с увеличенным действием ле- |
|||||||||
водопы и включают дискинезии, тошноту и спутанность сознания. Часто необходимо снизить суточ- |
|||||||||
ную дозу леводопы примерно на 30% в первые 48 часов, чтобы избежать или обратить вспять такие |
|||||||||
осложнения. |
|
|
|
|
|
|
|
Ц |
|
|
|
|
|
|
|
|
|
|
|
Другие побочные эффекты включают диарею, боль в животе, ортостатическую гипотензию, |
|||||||||
нарушения сна и окрашивание мочи в оранжевый цвет. Толкапон может вызвать повышение уровня |
|||||||||
печеночных ферментов, соответственно, его не следует применять у пациентов с патологией функции |
|||||||||
печени. У энтакапона гепатотоксичность практически отсутствует. |
|
||||||||
Коммерческий препарат под названием Сталево состоит из комбинации леводопы с карбидопой |
|||||||||
и энтакапоном. Однако, несмотря на удобство комбинации Сталево приводит к более раннему появ- |
|||||||||
лению и повышению частоты дискинезий. |
|
|
|||||||
6.6.2. Вещества, угнетающие глутаматергические влияния |
|
||||||||
|
|
|
|
Э |
|
|
|||
Амантадин, противовирусный препарат, у которого случайно были обнаружены относитель- |
|||||||||
но слабые антипаркинсонические свойства. Он может усиливать дофаминергическую активность, |
|||||||||
влияя на синтез, высвобождение или обратный захват дофамина. Вещество противодействует эффек- |
|||||||||
там аденозина за счет антагонизма с аденозиновыми A2A-рецепторами, которые угнетают функцио- |
|||||||||
нирование D2-рецептора. Препарат стимулирует выход катехоламинов из периферийных депо. |
|||||||||
АмантадинГявляется антагонистом NMDA-рецепторов глутамата, что вызывает антидискинетический |
|||||||||
эффект. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
231 |
