
- •Министерство образования Республики Беларусь
- •3 Физические свойства аминокислот 24
- •4 Химические свойства аминокислот 25
- •5 Полипептиды 34
- •6 Пространственное строение полипептидов и белков 39
- •7 Значение аминокислот и пептидов. Незаменимые аминокислоты 43
- •Введение
- •Классификация, изомерия и номенклатура
- •Классификация аминокислот
- •Неполярные r-группы
- •Изомерия аминокислот
- •Проекционные формулы энантиомеров:
- •Номенклатура аминокислот
- •Способы получения аминокислот
- •Гидролиз белков под влиянием ферментов, кислот и щелочей
- •Действие аммиака на галогензамещенные кислоты (аммонолиз)
- •Микробиологический синтез
- •Химические свойства аминокислот
- •Амфотерный характер аминокислот
- •Реакции карбоксильной группы
- •Алкилирование аминокислот
- •Действие азотистой кислоты на аминокислоты
- •Образование оснований Шиффа
- •Образование днф-производных
- •Образование фтг-производных (реакция Эдмана)
- •Качественные реакции аминокислот
- •Реакции, протекающие с одновременным участием карбоксильной и аминной групп
- •Отношение аминокислот к нагреванию
- •Биохимические превращения аминокислот
- •Полипептиды
- •Защита аминогруппы
- •Защита карбоксильной группы
- •Способы активирования карбоксильной группы
- •Пространственное строение полипептидов и белков
- •Первичная структура
- •Строение пептидной группы
- •Вторичная структура
- •Третичная структура
- •Четвертичная структура
- •Значение аминокислот и пептидов. Незаменимые аминокислоты
- •Список использованной литературы
Действие аммиака на галогензамещенные кислоты (аммонолиз)
Реакцию осуществляют при действии избытка водного, спиртового или жидкого аммиака обычно на -галогензамещенные кислоты (как наиболее доступные); при этом образуются аммонийные соли аминокислот:
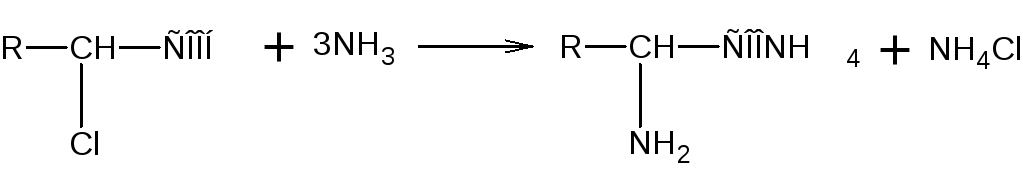
Метод удобен для синтеза самых разнообразных аминокислот, но возникают большие трудности отделения солей аминокислот от хлорида аммония.
Получение из циангидринов альдегидов и кетонов (циангидринный метод)
Важной реакцией получения -аминокислот является действие аммиака на циангидрины альдегидов или кетонов, с последующим гидролизом аминонитрила в аминокислоту:

Аминонитрилы можно получить также, действуя на альдегиды или кетоны непосредственно цианистым аммонием или смесью водных растворов хлористого аммония и цианистого калия, в результате обменного разложения дающих цианистый аммоний, который вступает в реакцию с альдегидами или кетонами:
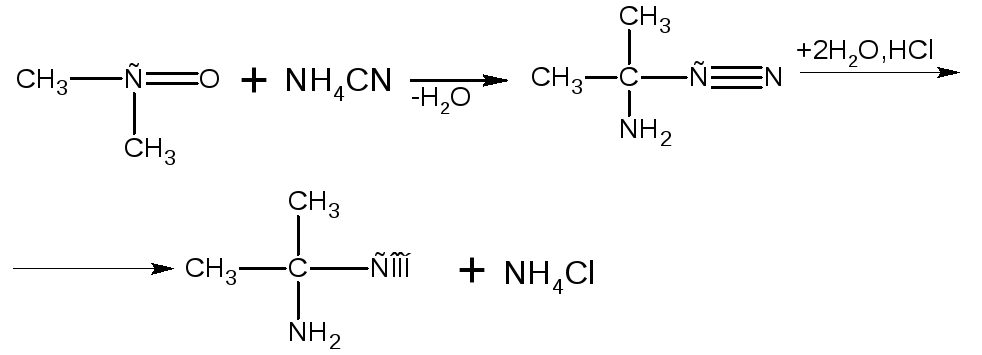
Синтезы с помощью нитроуксусного эфира
При конденсации нитроуксусного эфира с альдегидами в присутствии органических оснований (по типу альдольной или кротоновой конденсации) с последующим восстановлением и гидролизом продуктов конденсации получают различные -аминокислоты.
а)
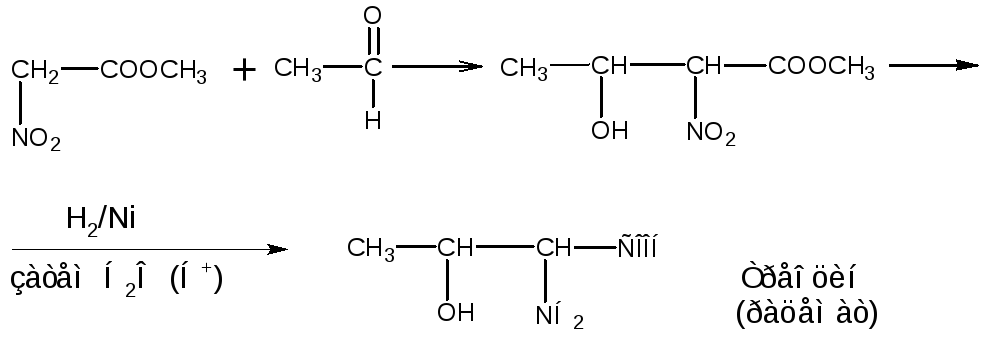
б)
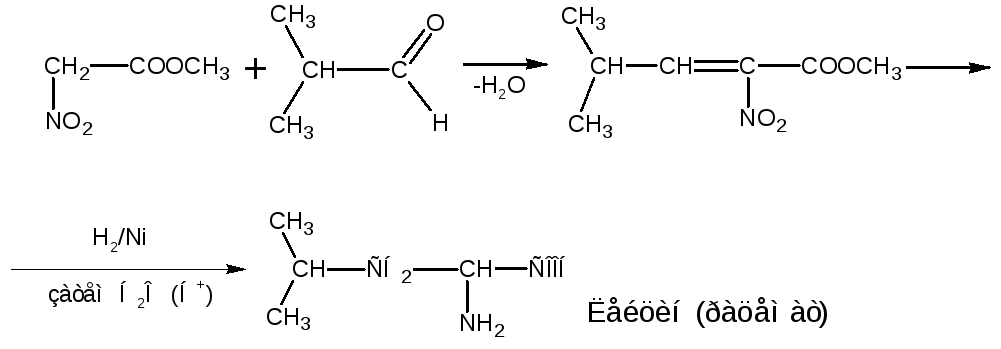
С помощью приведенных выше способов получают -аминокислоты, но разработаны способы получения-,- и других аминокислот. Следующие синтезы позволяют получить-аминокислоты.
Присоединение аммиака к-,-непредельным кислотам
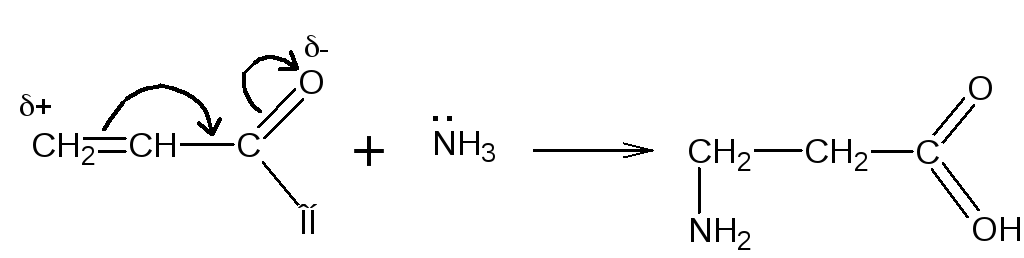
Присоединение происходит против правила Марковникова, т.е. атом водорода присоединяется к менее гидрированному атому углерода, что объясняется поляризацией двойной связи под влиянием электроноакцепторной СООН-группы.
Синтез из малонового эфира, альдегидов и аммиака (по В.М. Родионову)
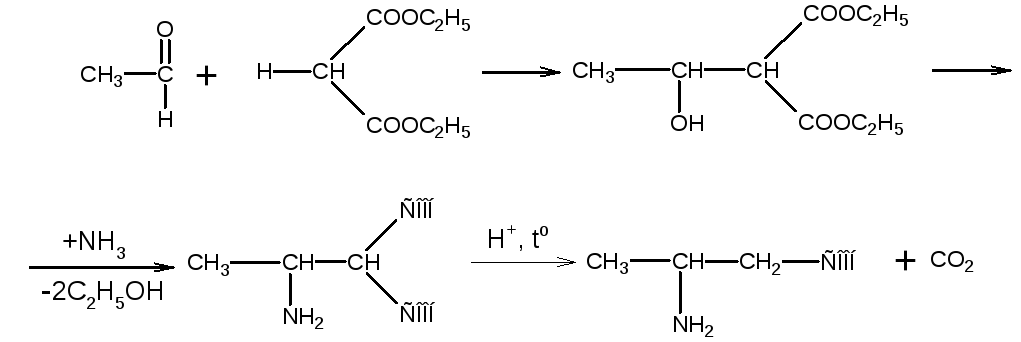
Восстановление оксимов или гидразонов альдегидо- или кетонокислот
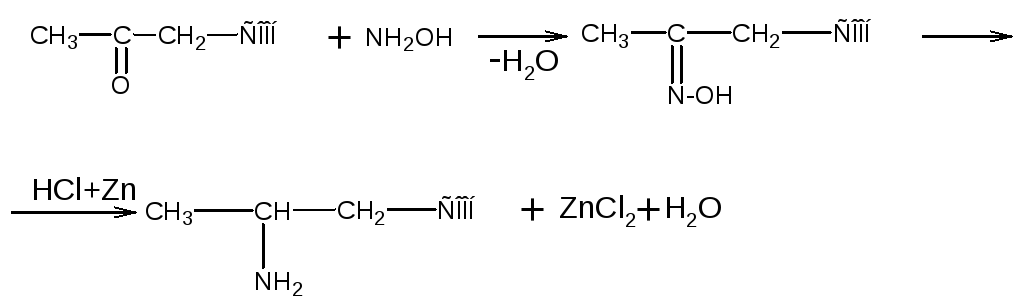
Восстановление нитрокислот
Важным способом синтеза ароматических аминокислот является восстановление орто- мета- и пара-нитробензойных кислот:
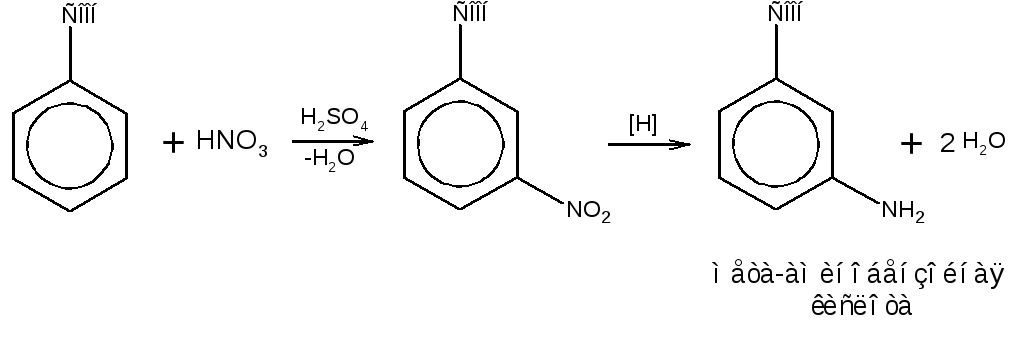
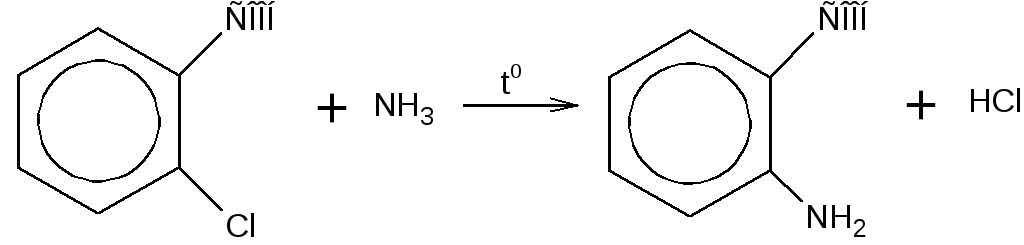
Эфиры орто-аминобензойной кислоты (антраниловой кислоты) содержатся в эфирных маслах жасмина, винограда, мандаринов. Синтетически эту кислоту получают аммонолизом орто-хлорбензойной кислоты:
Парааминобензойная кислота (витамин Н) играет большую роль в жизнедеятельности микроорганизмов, в том числе болезнетворных. Получают ее восстановлением пара-нитробензойной кислоты, а ее производные применяют в медицине в качестве анестезирующих веществ, в том числе анестезин, новокаин, пантокаин.
Микробиологический синтез
В промышленности многие аминокислоты получают микробиологическим путем, выращивая на специальной питательной среде микроорганизмы, продуцирующие в процессе своей жизнедеятельности определенные аминокислоты. Таким путем получают, например, лизин, глутаминовую кислоту.
Синтезы отдельных аминокислот
Аминокислоты с более удаленными друг от друга функциональными группами получают действием аммиака на галогензамещенные кислоты, восстановлением неполных нитрилов двухосновных кислот, с помощью бекмановской перегруппировки и т.д.
Синтез-аминокапроновой кислоты
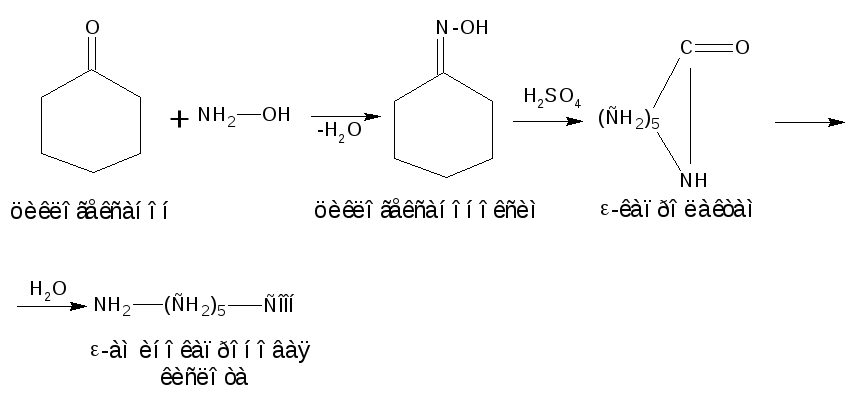
Синтез,-диаминокапроновой кислоты (лизина)
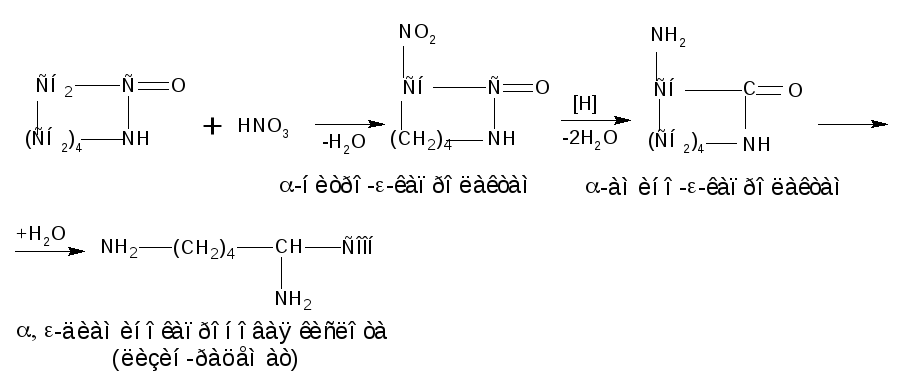
2.10.3 Синтез метионина
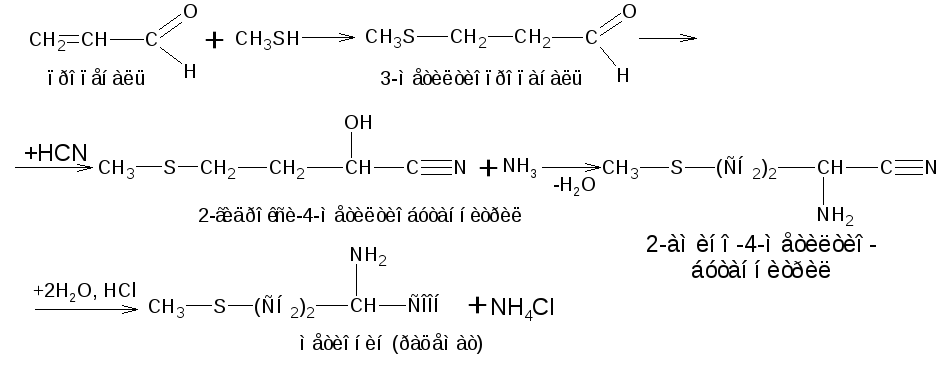
Физические свойства аминокислот
Аминокислоты – бесцветные кристаллические вещества с высокими температурами плавления (плавятся с разложением), которые мало отличаются для разных аминокислот и поэтому не характерны. Большинство из них хорошо растворяются в воде и плохо – в органических кислотах. Это свойство связано с тем, что за счет внутримолекулярной ионизации, обусловленной кислотной диссоциацией карбоксильной группы и протонированиемNН2-группы, образуется внутренняя соль, т.е. аминокислоты в водных растворах существуют в виде внутренних солей («цвиттер-ионов»), представляющих собой биполярные ионы:
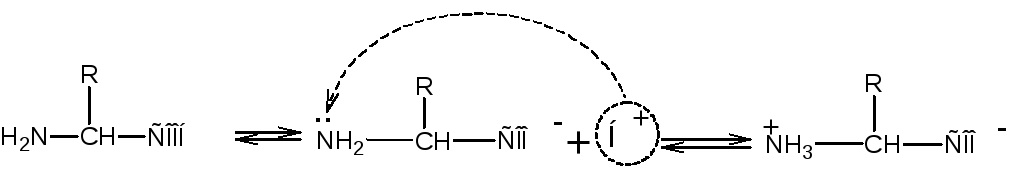
Водные растворы неполярных -аминокислот почти нейтральны (рН6,8), неэлектропроводны. В колебательных спектрах у них нет полос, относящихся к СООН иNН2-группам. Значение рН, при котором максимальное количество молекул аминокислоты находится в виде биполярных ионов и раствор является неэлектропроводным, называетсяизоэлектрической точкой аминокислоты (pI).
При подкислении вследствие нейтрализации карбоксильной группы аминокислота превращается в катион, способный двигаться к катоду в электрическом поле. В щелочной среде биполярный ион аминокислоты превращается в анион, способный в электрическом поле двигаться к аноду. На этом основано разделение -аминокислот методом электрофореза.
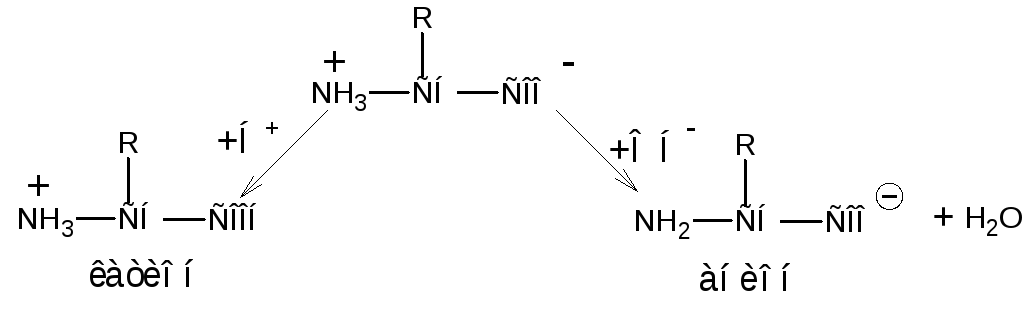
Естественно, что диаминокарбоновые кислоты (основные) имеют в растворе основную реакцию (рН>7), а аминодикарбоновые (кислые) – кислую реакцию (рН<7). В организме при физиологических значениях рН (например, рН крови 7,3–7,5) кислые кислоты находятся в виде анионов, а основные -аминокислоты находятся в виде катионов. Следует отметить, что ни одна-аминокислотаinvivoне находится в своей изоэлектрической точке и не попадает в состояние, отвечающее наименьшей растворимости в воде. Следовательно, все-аминокислоты в организме находятся в ионной форме.
