- •1. Основные понятия термодинамики
- •2. Первый закон термодинамики
- •Первое следствие. Энтальпия реакции равна разности алгебраической суммы энтальпий образования всех продуктов реакции и алгебраической суммы энтальпий образования всех исходных веществ:
- •Второе следствие Энтальпия прямой реакции численно равна энтальпии обратной реакции, но с противоположным знаком:
- •3. Понятие о самопроизвольных процессах. Энтропия
- •4. Второй закон термодинамики.
- •Биохимические реакции
- •5. Принцип энергетического сопряжения биохимических реакций
- •6. Особенности термодинамики биохимических процессов в равновесных и стационарных состояниях. Понятие о гомеостазе
- •Заключение
- •Контрольные задания
- •Вариант 13
- •Вариант 14
- •Вариант 15
- •Типовые тестовые задания
- •Контрольные тестовые задания
- •Список литературы
- •Стандартные энтальпии образования, энтропии и энергии гиббса образования некоторых веществ при 298 к (25 оС)
- •Содержание
2. Первый закон термодинамики
Первый закон (первое начало) термодинамики – это всеобщий закон природы, – закон сохранения и превращения энергии, соответствующий основному положению диалектического материализма о вечности и неуничтожимости движения.
Энергия не исчезает и не возникает из ничего, а только превращается из одного вида в другой в строго эквивалентных соотношениях.
Впервые этот закон в 1842 г. сформулировал немецкий физик Ю. Мейер, врач по образованию.
В зависимости от вида системы I закон термодинамики имеет различные формулировки.
В изолированной системе внутренняя энергия постоянна (∆U = 0).
Для закрытой системы I закон термодинамики устанавливает связь между теплотой, полученной или выделенной системой в некотором процессе, изменением внутренней энергии системы и произведённой при этом работой.
Если к закрытой системе подвести теплоту Q, то эта энергия расходуется на увеличение внутренней энергии системы U и на совершение системой работы против внешних сил окружающей среды:
Q = U + А.
В изобарно-изотермических условиях, в которых функционируют живые организмы, совершаемая работа А = pV, тогда:
Q = U + pV = (Uкон Uнач) + (pVкон pVнач) =
= (Uкон + pVкон) – (Uнач + pVнач)
Сумму внутренней энергии системы и произведения объёма на давление (U + pV) называют теплосодержанием или энтальпией.
Энтальпия (Н) – термодинамическая функция, характеризующая энергетическое состояние системы при изобарно-изотермических условиях.
Раздел химии, занимающийся изучением тепловых эффектов химических реакций, называется термохимией.
Теплота, полученная системой при р, Т = const, равна приращению энтальпии системы Н:
Q = Hкон – Ннач = Н.
Абсолютное значение энтальпии, как и абсолютную величину внутренней энергии системы, определить невозможно, поэтому в термодинамических расчётах используют лишь изменение энтальпии, происходящее при переходе системы из одного состояния в другое. Величина Н не зависит от пути процесса, а определяется, как для любой другой функции состояния, разностью энтальпий, характеризующих конечное и начальное состояния системы:
Н = Hкон – Ннач.
Количество теплоты, которое выделяется или поглощается при прохождении химической реакции в изобарно-изотермических условиях, характеризуется изменением энтальпии системы и называется энтальпией реакции (Нр).
Химические реакции и физико-химические процессы подразделяются на экзотермические и эндотермические.
Экзотермические процессы сопровождаются выделением энергии из системы в окружающую среду.
В результате экзотермических процессов энтальпия системы уменьшается (Нкон < Hнач), следовательно:
Нэкзо = (Нкон Hнач ) < 0.
Эндотермические процессы сопровождаются поглощением энергии системой из окружающей среды.
В результате эндотермических процессов энтальпия системы увеличивается (Hкон > Hнач), следовательно:
Нэндо = (Нкон Hнач ) > 0.
Энтальпия системы является экстенсивным параметром и зависит от количества вещества, температуры и давления, поэтому изменение энтальпии в результате химической реакции или других процессов определяют при стандартных условиях.
Стандартные условия: количество вещества 1 моль;
давление 760 мм рт. ст. = 101 325 Па;
температура 298 К ≈ 25 °С.
Термодинамические
параметры и функции состояния системы
или их изменения, измеренные при
стандартных условиях, обозначаются
соответствующим символом с верхним
индексом "°". Стандартную
энтальпию реакции обозначают
![]() ,
кДж/моль.
,
кДж/моль.
Стандартная энтальпия химической реакции представляет собой энергетическую характеристику реакции, проводимой при стандартных условиях. Химические уравнения, для которых указано значение энтальпии реакции, называются термохимическими уравнениями. Например, для реакции горения 1 моль ацетилена:
С2Н2(г)
+ 2,5О2(г)
= 2СО2(г)
+ Н2О(г);
![]() =1256
кДж/моль.
=1256
кДж/моль.
Кроме тепловых эффектов термохимические уравнения обязательно содержат индексы, обозначающие агрегатные состояния исходных веществ и продуктов реакции. Следует также иметь ввиду, что термохимические уравнения могут иметь дробные стехиометрические коэффициенты; это связано с тем, что тепловой эффект реакции рассчитывается только на 1 моль продукта реакции или на 1 моль одного из реагирующих веществ.
Для оценки энергетического состояния веществ в термодинамике используются значения стандартных энтальпий образования этих веществ, обозначаемые ∆Н°[вещество (агрегатное состояние)], кДж/моль.
Стандартная энтальпия образования простых веществ в их наиболее термодинамически устойчивом агрегатном и аллотропном состоянии при стандартных условиях принимается равной нулю.
Например, для
кислорода Но
(О2)
= 0, для графита
![]() (Сграфит)
= 0. Однако стандартная энтальпия
образования озона Hо
(О3)
= 142,2 кДж/моль, алмаза Но
(Салмаз)
= 1,8 кДж/моль.
(Сграфит)
= 0. Однако стандартная энтальпия
образования озона Hо
(О3)
= 142,2 кДж/моль, алмаза Но
(Салмаз)
= 1,8 кДж/моль.
Стандартная энтальпия образования сложного вещества равна энтальпии реакции получения 1 моль этого вещества из простых веществ при стандартных условиях.
Например, стандартная энтальпия образования этанола равна стандартной энтальпии гипотетической реакции:
2Сграфит + 3Н2(г) + 0,5О2 (г) = С2Н5ОН(ж);
Но (С2Н5ОН) = 277 кДж/моль.
Значение стандартной энтальпии образования сложного вещества зависит от природы вещества и его агрегатного состояния. Числовые значения стандартных энтальпий образования веществ приводятся в справочниках.
Энтальпию реакции можно определить как экспериментально, так и методом расчёта с использованием стандартных энтальпий образования веществ, участвующих в химической реакции, на основе закона, открытого российским учёным Г. И. Гессом (1840 г.).
Энтальпия реакции, то есть тепловой эффект реакции, зависит только от природы и состояния исходных веществ и конечных продуктов и не зависит от пути, по которому протекает реакция.
Закон Гесса является вполне строгим для процессов, происходящих при постоянном давлении или при постоянном объёме. Для этих процессов он может рассматриваться как частная форма выражения закона сохранения энергии применительно к химическим реакциям.
|
Герман Иванович Гесс (7.VIII 1802—12.XII 1850). Русский химик, академик Петербургской АН (с 1830). Родился в Женеве 7 августа 1802 г. Окончил Дерлтский университет (доктор медицины, 1825). Совершенствовал образование в Стокгольмском университете (1825). С 1830 – профессор Петербургского технологического института, в 1832–1849 –Петербургского горного института. Один из основоположников термохимии. Значительно раньше J. П. Ю. Ю. Томсена и П. Э. М. Бертло выдвинул (1840) положение, согласно которому величины тепловых эффектов реакции могут служить мерой химического сродства. |
|
Открыл (1840) основной закон термохимии – закон постоянства количества тепла, по которому тепловой эффект реакции зависит только от начального и конечного состояний реагирующих веществ, а не от количества стадий процесса (закон Гесса). Доказал (1842), что при смешении нейтральных солевых растворов тепловой эффект отсутствует (правило термонейтральности). Установил, что при нейтрализации грамм-эквивалента любой сильной кислоты сильным основанием всегда выделяется одинаковое количество тзп-ла (13,5 ккал). Открыл и определил (1830–1834) состав четырех новых минералов – вертита, уваровита, гидроборацита и фольбортита. Предложил (1833) способ получения теллура из теллурида серебра — минерала, который был им впервые изучен. Изучал (1832) окислы кобальта. Установил катализирующее и адсорбционное свойства мелкораздробленной платины. Одним из первых изучал состав кавказских нефтей. Открыл сахарную кислоту. Написал учебник «Основания чистой химии» (1831), выдержавший семь изданий.
В его честь теллурид серебра назван гесситом.
Закон Гесса можно проиллюстрировать следующей схемой:
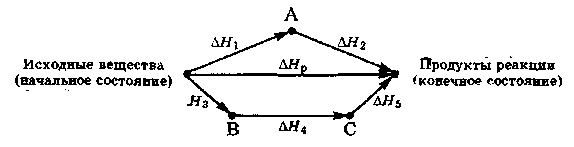
Переход системы из начального состояния в конечное можно осуществить разными путями:
непосредственно через реакцию, энтальпия которой равна Hр;
в результате двухстадийного процесса через промежуточное состояние А, энтальпии отдельных стадий которого равны соответственно H1 и H2;
через ряд реакций трёхстадийного процесса через промежуточные состояния В и С, для которых энтальпии отдельных стадий равны соответственно H3, H4 и H5.
В соответствии с законом Гесса:
Hр = H1 + H2 = H3 + H4 + H5.
В термохимических расчётах большое значение имеют следствия из закона Гесса.