
- •СОДЕРЖАНИЕ
- •РАЗДЕЛЫ КУРСА «ХИМИЯ»
- •ТЕМЫ ПРАКТИЧЕСКИХ ЗАНЯТИЙ
- •НАИМЕНОВАНИЯ ЛАБОРАТОРНЫХ РАБОТ
- •Пример
- •Решение
- •Ответ:
- •Индивидуальные задания
- •Пример 1
- •Решение
- •Ответ:
- •Пример 2
- •Решение
- •Ответ:
- •Индивидуальные задания
- •Пример 1
- •Решение
- •Ответ:
- •Пример 2
- •Решение
- •Пример
- •Решение
- •Индивидуальные задания
- •Гальванические элементы
- •Индивидуальные задания
- •Процессы электролиза
- •Катодные процессы
- •Анодные процессы
- •Пример 1
- •Решение
- •Ответ:
- •Пример 2
- •Решение
- •Ответ:
- •Индивидуальные задания
- •Пример 1
- •Решение
- •Ответ
- •Пример 2
- •Решение
- •Ответ:
- •Индивидуальные задания
- •Применение электрохимических процессов в технике
- •Индивидуальные задания
- •Химия конструкционных материалов
- •Химия металлов и сплавов
- •Элементарные и сложные полупроводники
- •Индивидуальные задания
- •ЛИТЕРАТУРА
- •ПРИЛОЖЕНИЕ
- •Термодинамические характеристики некоторых простых и сложных веществ

59
изделия. В образующемся макрогальваническом элементе протектор служит анодом и корродирует, а на защищаемом изделии — катоде идут процессы восстановления окислителя среды.
В условиях плохо проводящей среды используют электрозащиту (катод-
ную защиту) — подсоединение защищаемой конструкции к отрицательному полюсу источника постоянного тока, а к положительному полюсу — вспомо-
гательного электрода, любого по активности. При этом создается электролиз-
ная система, в которой защищаемая конструкция служит катодом, а на положительном вспомогательном электроде — аноде идут процессы окисления: самого анода (электрод растворимый) или восстановителя окружающей сре-
ды (электрод инертный).
Пример 1
Определить, какая среда является наиболее опасной для изделий из олова: кислая ( pH =3) без доступа O2 или нейтральная ( pH = 7 ) с доступом O2. Ответ необходимо обосновать приведением соответствующих электрохимических систем, уравнений первичных (анодно-катодных) и вторичных процессов, а также расчетами.
Решение
Рассмотрим предполагаемые электрохимические системы, возникающие при коррозии оловянных изделий вследствие наличия в металле примесей, менее активных, чем олово.
В результате возникают короткозамкнутые микрогальванические элементы, в которых примесные центры выполняют роль катодных участков
(φSn0 2+ Sn < φ0прим. ц. ).
Sn < φ0прим. ц. ).
В случае кислой среды ( pH = 3) без доступа O2 возникают элементы по схеме
Sn |
+ |
H2O |
Примесные |
H , |
центры |
||
|
pH = 3 |
||
|
|
||
Из прил., табл. 2 находим значение φSn0 2+ Sn = − 0,136 В. Исходя из условия за-
дачи, анодом будет служить Sn, а на примесных центрах будут разряжаться ионы H+ (окислитель окружающей среды):
A : Sn −2e =Sn2+ , φa = φSn0 2+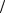 Sn = − 0,136 В;
Sn = − 0,136 В;
K : 2H+ +2e = H2 , φк = φ2рH+ H2 = − 0,059 pH = − 0,059 · 3 = − 0,177 В.
H2 = − 0,059 pH = − 0,059 · 3 = − 0,177 В.
Так как φк <φa , E =φк −φа < 0 и ∆G = −nFE > 0 , то коррозия оловянных из-
