
ZO-2010
.pdf
зан с шириной щели a по формуле (2). Из условия задачи видно, что угол ϕ весьма мал. Поэтому для углов менее 5°
sinϕ » tgϕ = 2bl .
Отсюда, полагая, что в формуле (2) k = 1, имеем λ = ab . Подставив это значение |
||||||||||
λ в (1), найдем |
|
|
|
|
|
|
2l |
|
|
|
|
|
h2l |
|
|
|
|
|
|
||
|
υ = |
|
. |
|
|
|
(3) |
|||
|
|
|
|
|
|
|
||||
|
|
|
mab |
|
|
|
|
|
||
Проверим наименование единицы измерения скорости в системе «СИ» |
||||||||||
н.е.и. υ = |
Дж × с × м |
|
= |
нм × с |
= |
кгм × мс |
= |
м |
. |
|
кг × м × м |
|
кг × м |
|
|
||||||
|
|
|
|
с2 × кгм |
с |
|||||
Произведем вычисления, предположив, что υ << c . Считаем электрон классической частицей, тогда m = m0 = 9,11·10–31 кг и расчет дает
υ = |
6,63×10−34 × 2 × 0,5 |
= 4,55·106 (м с). |
|
9,11×10−31 × 2 ×10−6 ×80 ×10−6 |
|||
|
|
Так как в действительности масса движущегося электрона не меньше его массы покоя m0 , то истинное значение скорости υ , определяемое по (3), будет не
больше, чем вычисленное нами. Таким образом, предположение о том, что υ << c , соответствует действительности и, значит полученный результат правильный. Если бы полученный результат противоречил неравенству υ << c , это означало бы, что электрон следует рассматривать как релятивистскую частицу, масса которой зависит от скорости. Тогда, чтобы получить правильный ответ, надо подставить в
(3) вместо m её значение
m = |
|
mo |
||
|
|
|||
1- |
υ2 |
|||
|
||||
|
c2 |
|||
|
|
|
||
и решить квадратное относительно υ уравнение.
2. Исходя из соотношения неопределенностей, найти наименьшую неточ- ность х , с которой можно вычислить координату электрона в атоме во- дорода, если его средняя кинетическая энергия  Eк
Eк  в невозбужденном ато-
в невозбужденном ато-
ме равна 2,18·10–18 Дж.
Дано
 Eк
Eк  = 2,18·10–18 Дж me = 9,1·10–19 кг
= 2,18·10–18 Дж me = 9,1·10–19 кг
h= 6,63·10–34 Дж·с х – ?
Анализ и решение
Как следует из соотношения неопределённостей
DхDрх ³ h ,
где х , Dрх – неопределенности координаты и про-
екции импульса на ось Х микрочастицы, h – постоянная Планка, неточность координаты электрона в
101

атоме водорода |
h |
|
|
|
Dх ³ |
. |
(1) |
||
|
||||
|
Dрх |
p (точнее его среднее квадратич- |
||
Величина рх неизвестна, однако сам импульс |
||||
ное значение) легко найти, так как нам известна средняя кинетическая энергия электрона. Так как  Ek
Ek  << m0c2 , то электрон можно считать нерелятивистской
<< m0c2 , то электрон можно считать нерелятивистской
частицей. Тогда его импульс р и кинетическая энергия áEк ñ связаны соотношением
áЕк ñ = mеυ2 |
= |
mе2υ2 |
= |
р2 |
. |
|
|||
|
|
|
|||||||
е |
2 |
|
|
2mе 2mе |
|
||||
Отсюда |
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
p = |
|
|
. |
(2) |
||||
|
|
2meEк |
|||||||
Теперь сравним величины Dрх и p . Поскольку импульс |
p – вектор, то по- |
||||||||
следняя формула позволяет лишь вычислить модуль этого вектора, тогда как его направление остается неизвестным. Поэтому проекция импульса px на ось Х ока-
зывается неопределенной: её величина лежит в интервале (– p , p ). Это значит, что
неопределенность проекции импульса на ось Х равна
рх = 2 р или рх ~ p ,
то есть величины Dрх и p одного порядка. Поэтому, заменив Dрх в формуле (1) величиной p и учитывая соотношение (2), получим ответ
|
|
Dх ³ |
h |
= |
|
h |
|
|
|
. |
|
|
|
|
р |
|
|
|
|
|
|
|
|||
|
|
|
|
|
2mе áЕек ñ |
|
|
|||||
Произведя вычисления, найдем |
|
|
|
|
|
|
|
|
|
|||
Dх ³ |
|
6,63×10−34 |
|
|
= 3,3·10 |
–10 |
(м). |
|||||
|
|
|
|
|
|
|
|
|||||
2 ×9,1×10−31 × 2,18 ×10-18 |
|
|||||||||||
|
|
|
|
|
|
|
|
|||||
Следовательно, наименьшая, допустимая соотношением неопределенностей минимальная неточность ( х ), с которой можно определить координату электрона в атоме водорода, есть величина порядка 10–10 м.
ЗАДАЧИ
441.Найти длину волны де Бройля λД для электрона, обладающего кинетической энергией Eк 1) 100 эВ; 2) 3,00 MэВ.
442.Приняв, что минимальная энергия E нуклона в ядре равна 10,0 эВ, оценить, исходя из соотношения неопределенностей, линейные размеры l ядра.
443.Какую энергию необходимо сообщить электрону, чтобы его дебройлевская длина волны λД уменьшилась от 100 до 50,0 пм?
102
444. Электрон в атоме водорода движется по первой боровской орбите. Неопределенность скорости υ электрона составляет 10 % от её числового значения. Определить неопределенность координаты х электрона. Применимо ли в данном случае для электрона понятие траектории?
445. Электрон обладает кинетической энергией Eк = 1,02 МэВ. Во сколько раз изменится длина волны де Бройля λД , если кинетическая энергия электрона уменьшится в два раза?
446.Используя соотношение неопределенностей, показать, что ядра атомов не могут содержать электронов. Принять радиус ядра rя = 1,00·10–13 см.
447.Найти длину волны де Бройля λД электрона, прошедшего ускоряющую разность потенциалов ϕ : 1) 1,00 кВ; 2) 1,00 МВ.
448. При какой относительной погрешности L / L момента импульса электрона на первой боровской орбите его угловая координата ϕ окажется совершенно неопределенной?
449.Определить, при каком числовом значении кинетической энергии Eк длина волны де Бройля λД электрона равна его комптоновской длине волны λК .
450.Атом испустил фотон с длиной волны λ = 600 нм. Продолжительность
излучения τ = 20,0 нс. Определить наибольшую неточность λ , с которой может быть измерена длина волны излучения.
Тема 26. Строение атомных ядер. Модели ядра. Дефект массы. Энергия связи ядра. Ядерные реакции
|
|
|
Примеры решения задач |
|
|
|
|
|
1. Вычислить энергию связи Eсв и дефект массы m ядра гелия 24 He . |
||
|
Дано |
|
Анализ и решение |
|
|
||
|
|
Опытным путем было установлено, что масса покоя |
|
|
|
||
Не – гелий |
|
ядра mя всегда меньше суммы масс покоя составляющих |
|
ma |
= 6,6443·10–27 кг |
|
его нуклонов. Но так как всякому изменению массы |
mH = 1,6736·10–27 кг |
|
должно соответствовать изменение энергии, то, следова- |
|
mn |
= 1,6721·10–27 кг |
|
тельно, при образовании ядра должна выделяться опре- |
|
|
|
деленная энергия. Энергия равная работе, которую нужно |
Eсв |
– ? m – ? |
|
|
|
совершить, чтобы разделить образующие ядро нуклоны |
||
(протоны и нейтроны) и удалить их друг от друга на расстояния, при которых они практически не взаимодействуют, называется энергией связи ядра Eсв
Есв = с |
2 |
é |
ù |
- mя}, |
|
{ëZmр + (A - Z)mn û |
|||
103
здесь c – скорость света в вакууме;mp , mn , mR – соответственно массы протона,
нейтрона и ядра; Z – количество протонов в ядре; A – массовое число (число нуклонов в ядре); (A − Z) = N – число нейтронов в ядре.
Это соотношение практически не нарушится, если заменить массу протона mp массой атома водорода mН , а массу ядра mR – массой атома mА . Указанная заме-
на будет означать добавление к уменьшаемому и вычитаемому выражениям, стоящим в фигурных скобках, одинаковой величины, равной Zme где me – масса элек-
трона
ZmH − ma = Z(mp + me ) − (mя + Zme ) = Zmp − mя .
Тогда |
= с2 {[Zm |
|
] - m |
}. |
|
Е |
+ (A - Z)m |
(1) |
|||
св |
H |
n |
a |
|
|
Это соотношение удобнее предыдущего, потому что в таблицах даются обычно не массы ядер mя , а массы атомов ma .
Величина
é |
ù |
- mя |
, |
Dm = ëZmp + (A - Z )mn û |
|||
или |
|
|
|
Dm = [ZmH + (A - Z)mn ] |
- ma |
(2) |
|
называется дефектом масс ядра. На эту величину уменьшается масса всех нуклонов при образовании из них атомного ядра.
В состав ядра 42 He , входят два протона ( Z = 2) и два нейтрона ( A– Z ) = 2. Подставляя эти величины в формулу (1) получим
Есв = 9×1016 éë2×1,6736×10−27 + 2×1,6721×10−27 - 6,6443×10−27 ùû = 4,239 ×10−12 ( Дж).
Рассчитаем дефект масс по формуле (2)
Dm = éë2 ×1,6736 ×10−27 + 2 ×1,6721×10−27 - 6,6443×10−27 ùû = 4,71×10−29 (кг).
Ответ: энергия связи ядра гелия Eсв = 4,24·10–12 Дж, дефект масс
m= 4,71·10–29 кг.
Вядерной физике часто пользуются внесистемной единицей энергии, при которой значение энергии системы численно равно значению её массы. Она называется атомной единицей энергии (а.е.э) и её можно определить с помо-
щью соотношения ε = mc2 : 1 а.е.э. = 1 а.е.м.·с2 = 1,66·10-27·кг (3·108)2 м2/c2 =
= 1,49·10-10 Дж = 931 МэВ.
Массу частиц в ядерной физике принято выражать в атомных единицах массы (а.е.м.), являющейся так же внесистемной единицей измерения. За 1
а.е.м. принята 1/12 массы изотопа углерода 126 C:
1 а.е.м. = 1,6605655·10–27 кг.
104

2. Определить энергию E ядерной реакции деления ядра азота нейтронами 14 N(n, p)14 C , если энергия связи ядра азота Есв N = 104,66 МэВ и ядра угле- рода Есв С = 105,29 МэВ.
Дано
Есв N = 104,66 МэВ Есв С = 105,29 МэВ
Едел – ?
Анализ и решение
Согласно условию задачи здесь нужно применить не стандартное решение с использованием таблиц масс ядер, а решение с использованием данных энергий связи. В ядерной реакции
147 N + 01n = 146C + 11H
число нейтронов (N = A − Z = 8) а и число протонов ( Z = 7) не изменяется. По-
этому, если представить энергию покоя ядра как разность энергий свободных нуклонов и энергии их связи
E0 = c2 (Zmp + Nmn ) −Wсв ,
то энергии свободных нуклонов в уравнении закона сохранения энергии
Eдел = (WN +Wn ) − (WC +Wp )
взаимно уничтожатся. Действительно,
Eдел = [c2(7mp + 7mn + mp ) − EсвN ] −[c2 (6mp + 8mn + mp ) − EсвC ] = EсвC − EсвN ,
то есть энергия в ядерной реакции выделяется в виде тепла за счет изменения энергии связи ядра. Подставив данные в задаче величины, получим
Eдел = 105,29 – 104,66 = 0,63 (МэВ).
ЗАДАЧИ
451. При бомбардировке изотопа 63 Li дейтонами 21 H образуются две
α -частицы тия.
4
2
Hе и выделяется энергия E = 22,3 МэВ. Найти массу изотопа ли-
452.Какая энергия связи Eсв выделится при образовании m = 1,00 г гелия 42 H из протонов и нейтронов.
453.При соударении α -частицы с ядром бора 105 В произошла ядерная реакция
врезультате которой образовалось два новых ядра. Одно из них – ядро атома во-
дорода 11 H . Определить порядковый номер Z и массовое число A второго ядра. Записать ядерную реакцию и определить её энергетический эффект.
454. При бомбардировке с помощью α -частиц бора 115 В наблюдается вылет
нейтронов. Написать уравнение ядерной реакции, приводящей к вылету одного нейтрона. Каков энергетический выход E этой реакции?
455. Определить массу m изотопа 157 N , если изменение массы m при образовании ядра 157 N составляет 0,2508·10–27 кг.
105

456.Найти энергию реакции 94 Be+ 11 H → 42 He+ 63 Li, считая, что кинетические энергии и направления движения ядер неизвестны.
457.Какую наименьшую энергию связи Eсв нужно затратить, чтобы оторвать
один нейтрон от ядра азота 147 N ?
458.При отрыве нейтрона 01n от ядра гелия 42 Hе образуется ядро 23 Hе . Определить энергию связи Eсв , которую необходимо для этого затратить.
459.Определить энергию связи Eсв бериллия 94 Ве и полную выделившуюся
энергию E , если при реакции 94 Be+ 21 H → 105 Be+ 01n подверглись превращению все ядра, содержащиеся в 1,00 г бериллия.
460. Вычислить дефект массы m и энергию связи Eсв ядра изотопа лития
37Li .
Тема 27. Радиоактивное излучение и его виды. Закон радиоактивного распада
Примеры решения задач
1. Определить число ядер, которые распадутся за 10,0 минут и за 10 суток
в радиоактивном препарате иода 13153 I массой m = 10–10 кг. Период полурас- |
||||
пада иода T = 8,00 суток. |
|
|
||
Дано |
|
Анализ и решение |
|
|
|
|
|||
t1 = 10,0 мин, t2 = 10,0 сут |
|
Самопроизвольное превращение |
одних |
|
m = 10–10 кг, T = 8,0 сут |
|
атомных ядер в другие, сопровождаемое ис- |
||
N1 – ? |
|
пусканием элементарных частиц, называется |
||
|
радиоактивным распадом. Закон, по которо- |
|||
N2 – ? |
||||
му происходит распад, описывается формулой |
||||
|
|
dN = −λNdt , |
(1) |
|
где dN – число ядер, распавшихся за промежуток времени от t до (t + dt) , N –
число ядер, нераспавшихся к моменту времени t , λ – постоянная радиоактив-
ного распада; знак минус указывает, что общее число радиоактивных ядер в процессе распада уменьшается. Интегрируя это уравнение, получим
N = N0e−λt , |
(2) |
где N0 – число радиоактивных ядер в момент t |
= 0. |
Время, за которое исходное число радиоактивных ядер в среднем уменьшается вдвое, называется периодом полураспада T . Период полураспада и постоянная распада связаны соотношением
Tλ = ln 2 . |
(3) |
106

Так как период полураспада радиоактивного иода намного больше времени t1 , то можно считать, что в течение этого промежутка времени число нераспав-
шихся ядер N остается практически постоянным и равным их начальному числу N0 . Тогда для нахождения числа распавшихся ядер N1 применим закон радио-
активного распада (1), записав его так
N1 = −λN t1 ,
или, учитывая (3),
DN1 = lnT2 N0Dt1.
Чтобы определить начальное число ядер (атомов) N0 , умножим постоянную Авогадро NA на число молей ν , содержащихся в данном препарате:
|
|
|
N |
|
= N ν = N |
|
m0 |
, |
|
|
(4) |
||||||
|
|
|
|
A M |
|
|
|||||||||||
|
|
|
|
0 |
|
|
A |
|
|
|
|
131 I, |
|
||||
где m |
– начальная масса препарата, |
|
M – |
молярная масса иода |
численно |
||||||||||||
0 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
53 |
|
|
равная (приблизительно) его массовому числу. С учетом (4) получим |
|
||||||||||||||||
|
|
|
DN = ln 2 |
N |
|
m0 |
Dt . |
|
|
|
|||||||
|
|
|
|
|
1 |
|
T |
|
A M |
|
1 |
|
|
|
|||
Произведем вычисление с учетом, что ln 2= 0,693, в результате |
|
|
|||||||||||||||
|
DN = |
0,693 |
|
|
|
23 |
10-10 |
|
|
9 |
(ядер). |
|
|||||
|
|
6,02 ×10 |
|
|
|
|
|
|
|
600 = 277 ×10 |
|
||||||
|
6,91×105 |
|
131×10-3 |
|
|||||||||||||
|
1 |
|
|
|
|
|
|
|
|
|
|||||||
Во втором случае время |
t2 и период полураспада иода – величины одного |
||||||||||||||||
порядка, и дифференциальная форма закона радиоактивного распада (1) здесь неприменима. Поэтому для решения задачи воспользуемся интегральной формой (2) закона, справедливой для любого промежутка времени. Тогда получим
DN2 = N0 - N = N0 (1- e-λt ) ,
или, учитывая (3) и (4),
|
m |
|
-ln 2Dt2 |
|
|
DN2 = NA |
0 |
(1- e |
T |
). |
|
M |
|||||
|
|
|
|
Подставим числовые значения данных величин в системе «СИ» и произведем вычисления
|
|
23 10-10 |
- |
0,693 |
8,64×105 |
|
|
|
|
|
6,9110× 5 |
12 |
|||||
DN2 |
= 6,02 ×10 |
|
|
(1- e |
|
|
) = 266 ×10 |
(ядер). |
131-3 |
|
|
||||||
Ответ: число распавшихся ядер за время за 10 минут – 277·109, за 8 суток –
266·1012.
ЗАДАЧИ
461. Каков возраст t урановой руды, если известно, что на массу m = 1,00 кг
урана 23892 U приходится масса m = 320 г свинца 20682 Рb? Считать, что весь свинец является конечным продуктом распада уранового ряда.
107
462.Определить массу m изотопа 13153 I, имеющего активность A = 37,0 ГБк. Сколько атомов этого препарата распадется за время 5 суток?
463.Некоторое число атомов N* радона помещено в замкнутый сосуд. По-
строить кривую зависимости изменения числа атомов N / N* радона в сосуде от времени в интервале 0 ≤ t ≤ 20 суток через каждые 2 суток. Постоянная распада радона λ = 0,181 сут–1. Из графика найти период полураспада T1/ 2 радона.
464. Изменение во времени массы изотопа радиоактивного кальция характеризуется следующей таблицей:
Время наблюдения t , сут |
0 |
20 |
40 |
60 |
80 |
100 |
Масса препарата m , г |
1,0000 |
0,9126 |
0,8398 |
0,7704 |
0,7112 |
0,6500 |
Из графика зависимости ln m = f (t) найти период полураспада изотопа кальция.
465.В образцах урановой руды всегда содержится некоторое количество атомов тория-234, образовавшихся в результате α -распада урана-238. Торий также радиоактивен. Сколько атомов тория содержится в образце урановой руды, содержащего m = 0,50 г урана-238? (Период полураспада тория равен 24 суткам).
466.Флюоресцирующий экран площадью S = 0,03 см2 находится от пылинки
радия 22688 Rа массой m = 18,0 нг на расстоянии r = 1,00 см. Сколько вспышек возникнет на экране за время t = 60,0 c?
467.Масса радиоактивного изотопа фосфора 3215 Р m = 1,00 мг. Определить число N ядер, распадающихся в течение времени: 1) t1 = 1,00 мин; 2) t2 = 5 сут.
468.Радий помещен в замкнутый сосуд. Через какое время t число атомов ра-
дона N будет отличаться на 10 % от числа атомов радона N* , соответствующего радиоактивному равновесию радия с радоном? Построить зависимость изменения
N / N* в сосуде от времени t в интервале 0 ≤t ≤ 6 T1/ 2 . За единицу времени принять период полураспада радона T1/ 2 . Для расчета воспользоваться формулой
NRn = No Ra (1− e−λRnt )λRa /λRn .
469. Радиоактивный препарат 2760 Со распадается по β -распаду. Какой элемент образуется? Сколько граммов m2 этого элемента образуется за 2,65 года из m1 = 1 10–10 кг радиоактивного кобальта?
470. Крупинка с радием 22688
Rа , находится на расстоянии r = 1,20 см от флюо-
ресцирующего экрана. Какую массу m имеет крупинка, если на площади экрана S = 0,602 см2 в течение t = 1,00 мин было зарегистрировано n = 47 сцинтилляций?
108

ПРИЛОЖЕНИЕ
d l
d l
l
I1 I2
I2
I2
Рис. 3.1 |
Рис. 3.2 |
I2 
 l
l
I1 
r b r
Рис. 3.3
|
Р |
S′′ |
θ |
|
|
|
x |
d |
|
ϕ |
|
|
|
|
|
S |
|
|
|
S′ |
|
|
Q2 |
a |
|
b |
|
|
|
||
|
l |
|
Э |
|
Рис. 4.1 |
|
|
|
|
|
109
|
|
S |
|
|
|
Э |
|
S1 |
α |
r |
|
|
|
xmin |
|
d |
2α |
а |
|
O |
|||
|
|
||
S2 |
|
|
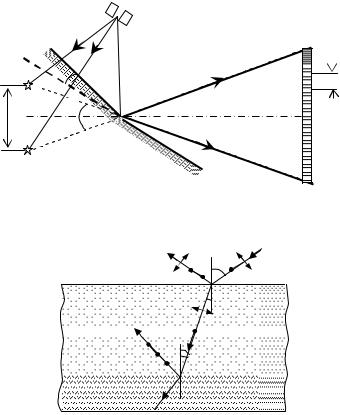
Рис. 4.2
α
γ
nж α′б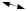
nст
Рис. 4.3
110
