
- •Учебник подготовлен в рамках Инновационной образовательной программы
- •ISBN 978-5-7262-0821-3
- •5.1. Однокомпонентные диаграммы фазового равновесия,
- •5.2.1. Диаграмма с полной взаимной растворимостью
- •5.2.4. Диаграммы с наличием трехфазного равновесия
- •5.2.5. Диаграммы с эвтектическим и эвтектоидным
- •5.2.6. Диаграммы с монотектическим и монотектоидным
- •5.2.8. Диаграммы с перитектическим и перитектоидным
- •7.1. Физико-химические основы взаимодействия
- •7.1.4. Роль термодинамики и химической кинетики
- •7.2.3. Пленки на металлах как продукты химической
- •7.2.9. Формирование защитных жаростойких пленок
- •7.2.10. Влияние внешних и внутренних факторов
- •7.3.3. Механизм электрохимической коррозии. Работа
- •7.3.4. Гетерогенность поверхности и микрогальванические
- •7.3.7. Термодинамика процессов электрохимической
- •7.4.3. Влияние примесей в жидких металлах
- •7.4.4. Основные пути снижения взаимодействия
- •конструкционных материалов с жидкометаллическими
- •7.5. Защита от коррозии на стадии проектирования и разработки
- •Предисловие к тому 2
- •Глава 4. ТЕРМОДИНАМИКА В МАТЕРИАЛОВЕДЕНИИ
- •Введение.
- •4.1. Основные понятия термодинамики
- •4.2. Метод термодинамических потенциалов
- •4.3. Прикладная термохимия
- •4.4. Фазовые равновесия
- •4.5. Термодинамика растворов
- •4.6. Физическая химия неидеальных растворов
- •4.7. Термодинамическая теория диаграмм состояния
- •Список использованной литературы
- •Глава 5. ДИАГРАММЫ ФАЗОВОГО РАВНОВЕСИЯ
- •Введение
- •5.2.2. Диаграмма с расслоением твердого раствора
- •5.2.3. Диаграмма с наличием упорядочения
- •5.2.4. Диаграммы с наличием трехфазного равновесия
- •5.2.7. Диаграмма с метатектическим равновесием
- •5.2.9. Диаграмма с синтектическим равновесием
- •5.2.10. Диаграммы с промежуточными фазами
- •5.3. Диаграмма железо – углерод
- •5.4. Анализ сложных диаграмм фазового равновесия
- •Контрольные вопросы
- •Список использованной литературы
- •6.4. Закономерности сегрегации примесей
- •Контрольные вопросы
- •Список использованной литературы
- •Глава 7. СОВМЕСТИМОСТЬ И КОРРОЗИЯ МАТЕРИАЛОВ
- •7.1.1. Совместимость материалов со средой
- •7.1.2. Коррозия. Основные понятия и определения
- •7.1.3. Коррозионные проблемы
- •7.1.5. Классификация процессов коррозии
- •7.2. Химическая коррозия металлов
- •7.2.1. Химическая газовая коррозия
- •7.2.4. Состав и структура оксидов. Эпитаксия
- •7.2.5. Толщина и защитные свойства пленок
- •7.2.7. Механизм химической газовой коррозии
- •7.2.8. Оксидные пленки на поверхности железа
- •7.2.11. Химическая коррозия в газовых теплоносителях
- •7.3. Электрохимическая коррозия
- •7.3.1. Основные признаки и причины
- •7.3.2. Электролиты
- •7.3.6. Электродные потенциалы
- •7.3.8. Диаграммы Пурбе
- •7.3.9. Кинетика электрохимических процессов коррозии
- •7.3.10. Электрохимическая защита
- •7.4. Коррозия в жидкометаллических средах
- •7.4.1. Типы процессов
- •7.4.2. Растворение твердого металла в жидком
- •7.5. Защита от коррозии на стадии проектирования
- •7.5.1. Коррозия и вопросы конструирования
- •7.5.2. Выбор материалов и их совместимость
- •7.5.3. Выбор рациональной формы элементов
- •7.5.4. Учет влияния механических нагрузок
- •7.5.5. Рациональные способы сборки конструкций
- •Контрольные вопросы
- •Список использованной литературы

ГЛАВА 7. СОВМЕСТИМОСТЬ И КОРРОЗИЯ МАТЕРИАЛОВ
Решение проблем, связанных с устойчивостью металлических изделий и конструкций против разрушения в результате воздействия на них окружающей среды, всегда было актуальным и не потеряло своего значения в настоящее время.
При внешнем воздействии окружающей среды на металлические поверхности имеют место различные виды взаимодействия между ними (химическое, электрохимическое, физико-химическое, механическое, радиационное и др.), что может привести во многих случаях к разрушению или порче оборудования, ухудшению экологии и другим нежелательным последствиям.
Одним из эффективных путей создания еще на стадии проектирования надежных конструкций, способных длительное время работать в агрессивных средах, является грамотное и обоснованное использование в них совместимых материалов, т.е. таких, которые могут находиться в рабочих условиях длительное время без заметного химического взаимодействия друг с другом.
Критерий совместимости во многих случаях является определяющим для надежности и долговечности конструкции или для установления принципиальной возможности использования данных материалов в конкретных условиях.
Решение проблем, связанных с совместимостью, требует повышения уровня знаний специалистов в области коррозии материалов и способов защиты от нее, как одной из основных проблем совместимости. Для этого необходимо, прежде всего, знание механизма и общих закономерностей важнейших коррозионных процессов.
7.1. Физико-химические основы взаимодействия материалов с окружающей средой
7.1.1. Совместимость материалов со средой
Материалы считают совместимыми в конкретных температур- но-временных условиях, если химическое взаимодействие между
445
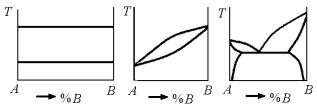
ними отсутствует или они взаимодействуют с допустимой скоростью, не изменяя заметно свой состав, структуру и свойства. Суждение о совместимости можно составить из анализа диаграмм состояний бинарных систем (рис. 7.1).
а б в
Рис. 7.1. Равновесные диаграммы состояний бинарных систем сплавов: а – компоненты системы не взаимодействуют ни в жидком, ни в твердом состояниях; б – компоненты системы образуют непрерывный ряд твердых растворов; в – система с ограниченной растворимостью компонентов друг в друге и эвтектикой
Как видно из рис. 7.1,а компоненты никак не взаимодействуют ни в жидком, ни в твердом состояниях. Эти металлы совместимы. Металлы, диаграммы которых представлены на рис. 7.1,б, в, при комнатных и невысоких температурах могут быть совместимы, так как степень их взаимодействия при этом невысока. Высокие температуры повышают их химическую активность, усиливающую взаимодействие, что приводит к их несовместимости.
Определенное влияние на характер и скорость физикохимического взаимодействия оказывают содержащиеся в контактирующих материалах и окружающей среде примеси (чаще всего газовые), допустимые содержания которых необходимо установливать заранее.
Взаимодействие материалов со средой имеет химическую, электрохимическую, физико-химическую и физическую природу. Химическим взаимодействием является окисление металлов в газовой среде и в сухом паре (без конденсации влаги на поверхности металла), т.е. образование оксидов, гидридов, нитридов, карбидов и других химических соединений. При контакте металлов и сплавов с влажным воздухом и водой возникает электрохимическая коррозия. Физико-химическое взаимодействие имеет место при раство-
446
рении металлов и сплавов в жидких металлах. Разрушение поверхности металла под действием быстро движущейся среды (кавитации) может быть примером физического взаимодействия. Указанные процессы развиваются на границе раздела материал–среда и приводят к коррозионному разрушению поверхностного слоя эксплуатируемых изделий, изменению их состава, структуры и свойств.
7.1.2.Коррозия. Основные понятия и определения
Всвете современных представлений коррозию рассматривают как самопроизвольное поверхностное разрушение металлических материалов вследствие физико-химического взаимодействия их с компонентами окружающей среды.
Всистеме международной стандартизации это понятие рассматривается как физико-химическое взаимодействие между металлом
исредой, в результате которого изменяются свойства и часто происходит ухудшение функциональных характеристик металла, среды или включающей их технической системы. Процесс коррозии представляют как эволюцию термодинамической системы, состоящей из металла и жидкой и/или газообразной среды. Изменение в любой части коррозионной системы, вызванное взаимодействием компонентов системы, называется коррозионным эффектом.
Металлическое состояние практически всех металлов (кроме некоторых благородных) является неустойчивым, и при взаимо-
действии с окислительным компонентом (О2, СО, SO2, Cl и др.) окружающей среды они переходят в более устойчивое окисленное состояние. Реакция окисления металла сопровождается потерей металлом электронов и образованием новых веществ – продуктов коррозии, состоящих из оксидов, гидроксидов, солей и других соединений корродирующего элемента. Видимые продукты атмосферной коррозии сплавов железа, состоящие в основном из гидратированных оксидов, называют ржавчиной, а продукты газовой коррозии – окалиной.
Цветные металлы не ржавеют, а корродируют. Неметаллические материалы, например пластмассы, могут набухать или трескаться,
447
дерево – расслаиваться или гнить, а бетон крошиться. К таким материалам, подвергающимся воздействию внешних эксплуатационных факторов, в том числе и действию микроорганизмов, приме-
няют термин старение, или деструкция.
Количество металла, превращенного в продукты коррозии за определенное время, относят к коррозионным потерям. Коррозионные потери массы металла с единицы поверхности или толщина прокорродировавшего слоя металла в единицу времени характери-
зуют скорость коррозии.
В некоторых случаях химическое взаимодействие металла и среды сопровождается физическим разрушением в результате механического повреждения от истирания или ударов частиц среды (например, теплоносителя). Такое разрушение называется коррози-
онной эрозией, или коррозионным износом. Разрушения могут вы-
зываться и другими процессами, такими как проникновение в металл водорода, приводящего к водородному охрупчиванию, или взаимодействие его с легкоплавким металлом.
Эффект повреждений, связанный с потерями механической прочности металла, называют коррозионным разрушением, а продвижение повреждений в глубину материала в единицу времени –
скоростью проникновения коррозии.
Таблица 7.1
Оценка коррозионной стойкости при равномерной коррозии
(по ГОСТ 13819-68)
Группа стойкости |
Скорость коррозии металла, |
Балл |
|
мм/год |
|||
|
|
||
Совершенно стойкие |
< 0,001 |
1 |
|
Весьма стойкие |
0,001–0,005 |
2 |
|
0,005–0,01 |
3 |
||
|
|||
Стойкие |
0,01–0,05 |
4 |
|
0,05–0,1 |
5 |
||
|
|||
Пониженно-стойкие |
0,1–0,5 |
6 |
|
0,5–1,0 |
7 |
||
|
|||
Малостойкие |
1,0–5,0 |
8 |
|
5,0–10,0 |
9 |
||
|
|||
Нестойкие |
> 10,0 |
10 |
|
|
448 |
|
