
- •III.2 Ароматичні вуглеводні
- •2.1 Ароматичність. Будова молекули бензену
- •2.2 Класифікація, номенклатура
- •2.3 Ізомерія
- •2.4 Фізичні властивості
- •2.5 Хімічні властивості бензену
- •Ііі.2.6 Вплив замісників на реакційну здатність ароматичних сполук
- •2.7 Хімічні особливості гомологів бензену
- •2.8 Властивості поліядерних аренів
- •2.9 Одержання аренів
- •2.10 Використання аренів
2.8 Властивості поліядерних аренів
Ароматичні вуглеводні з неконденсованими ядрамивступають у реакції електрофільного заміщення значно легше, ніж бензен, – подібно до толуолу. Причому, утворюються переважно продуктиn-заміщення:


+ 2HO-NO2 ----------- + H2O
H2SO4
Дифеніл 4,4-Динітридифеніл
Ди- і три-фенілметани, крім того, піддаються реакціям радикального заміщення та окислення по sp3-гібридизованому атому Карбону, наприклад:

Br2, УФ
 --------------
+ HBr2
--------------
+ HBr2

---------- Бромдифенілметан
 [O]
[O]
---------------
CrO3, t0
Бензофенон
Конденсовані поліаренивиявляють ще більшу схильність до реакції електрофільного заміщення, які протікають, в основному, по-положенню.

+Br2, 400C
 --------------------
+ HBr
--------------------
+ HBr
CH3COOH

 1-Бромнафталін
1-Бромнафталін
----- HO-NO2
-------------------- + H2O
H2SO4
Нафталін
 1-Нітронафталін
1-Нітронафталін
СH3COCl
-------------------- + HCl
AlCl3
1-Ацетонафтон
Сульфування нафталіну залежно від температури може давати різні продукти, один з яких здатний ізомеризуватися в інший за певних умов:

HO-SO3H, 800
 -----------------------
+ H2O
-----------------------
+ H2O

------- Нафталін-1-сульфонова кислота
 HO-SO3H,
1600
HO-SO3H,
1600
----------------------- + H2O
Нафталін-2-сульфонова кислота
 Якщо
нафталін вже містить один замісник, то
орієнтація вступу другого замісника
підкоряєтьсяпевним правилам,
схематично які можна зобразити так:
Якщо
нафталін вже містить один замісник, то
орієнтація вступу другого замісника
підкоряєтьсяпевним правилам,
схематично які можна зобразити так:
І роду
І роду
ІІ роду
ІІ роду
Реакції, що супроводжуються порушенням ароматичності, для нафталіна проходять легше, ніж для бензену. Він може відновлюватися навіть воднем у момент виділення, наприклад, внаслідок взаємодії Na із спиртом:
 С2H3-OН+Na,
800
С2H3-OН+Na,
800
 -------------------------
-------------------------

------- 1,4-Дигідронафталін
 ізо-С5H11OН+Na,
1300
ізо-С5H11OН+Na,
1300
-----------------------------
1,2-Тетрагідронафталін
Каталітичне гідрування проходить поступово:

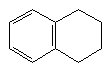

H2 H2
----------- ---------------
Ni, 1500 Ni, 200-3000
Нафталін Тетралін Пергідронафталін
(декалін)
Окиснюється нафталін теж значно легше порівняно з бензеном і може давати різні продукти залежно від умов:
 CrO3,
CH3COOH,
2500
CrO3,
CH3COOH,
2500
 ---------------------------------
---------------------------------

 -------
Нафтохінон-1,4
-------
Нафтохінон-1,4
O2, 4000
---------------------------------
Фталевий ангідрид
У заміщених похідних нафталіну окисненню піддається кільце з підвищеною електронною густиною:


І роду [O]
------------
Фталева кислота
 ІІ роду
ІІ роду
[O] II роду
------------
Заміщена фталева кислота
Антрацен і фенантрен характеризуються ще більшою реакційною здатністю, ніж нафталін. У реакціях SE переважно утворюються продукти заміщення у положенні 9:

Br2
------------- + HBr
FeBr3
 Антрацен
9-Бромантрацен
Антрацен
9-Бромантрацен

+ Br2 -------- + HBr
Фенантрен 9-Бромфенантрен
Нітрування, алкілювання, ацилювання триядерних конденсованих аренів теж протікає в положення 9, а сульфування – залежно від концентрації H2SO4 може давати,(1,8)- чи,(2,6)-продукти:
 HO-SO3H
(розв.)
HO-SO3H
(розв.)
 -----------------------
+ H2O
-----------------------
+ H2O

 -------
Антрацен-2.6-дисульфонова
кислота
-------
Антрацен-2.6-дисульфонова
кислота
HO-SO3H (конц.)
-------------------------- + H2O
Антрацен-1,8-дисульфонова кислота

 Ці
поліарени легко відновлюються до
дигідропохідних і легко окиснюються
до відповідних хінонів:
Ці
поліарени легко відновлюються до
дигідропохідних і легко окиснюються
до відповідних хінонів:

Na+C2H5OH CrO3, CH3COOH
<-------------- ------------------
[H] [O]
 9,10-Дигідроантрацен
Антрацен
Антрахінон-9,10
9,10-Дигідроантрацен
Антрацен
Антрахінон-9,10


Na+C2H5OH CrO3, CH3COOH
<--------------- ------------------
[H] [O]
9,10-Дигідрофенантрен Фенантрен Фенантренхінон-9,10
Антрахінон і фенантренхінон є сировиною для добування багатьох барвників (алізарину, індатренового синього та ін.) та лікарських препаратів.
