
- •Патогенез острого ишемического и реперфузионного повреждения миокарда
- •Патогенез ишемического повреждения миокарда
- •Механизмы реперфузионного повреждения миокарда
- •Острое необратимое реперфузионное повреждение миокарда
- •Механизмы позднего необратимого реперфузионного повреждения миокарда
- •Феномен постишемического невосстановления кровотока (no-reflow)
- •Механизмы no-reflow
- •Оглушенный (станнированный) миокард
- •Механизмы станнирования
- •Лечение оглушенного миокарда
- •Гибернирующий (спящий) миокард
- •Механизмы краткосрочной и хронической гибернации
- •Лечение гибернации миокарда
- •Фиксированная и динамическая обструкция коронарных артерий
- •Феномен обкрадывания
- •Литература.
Механизмы no-reflow
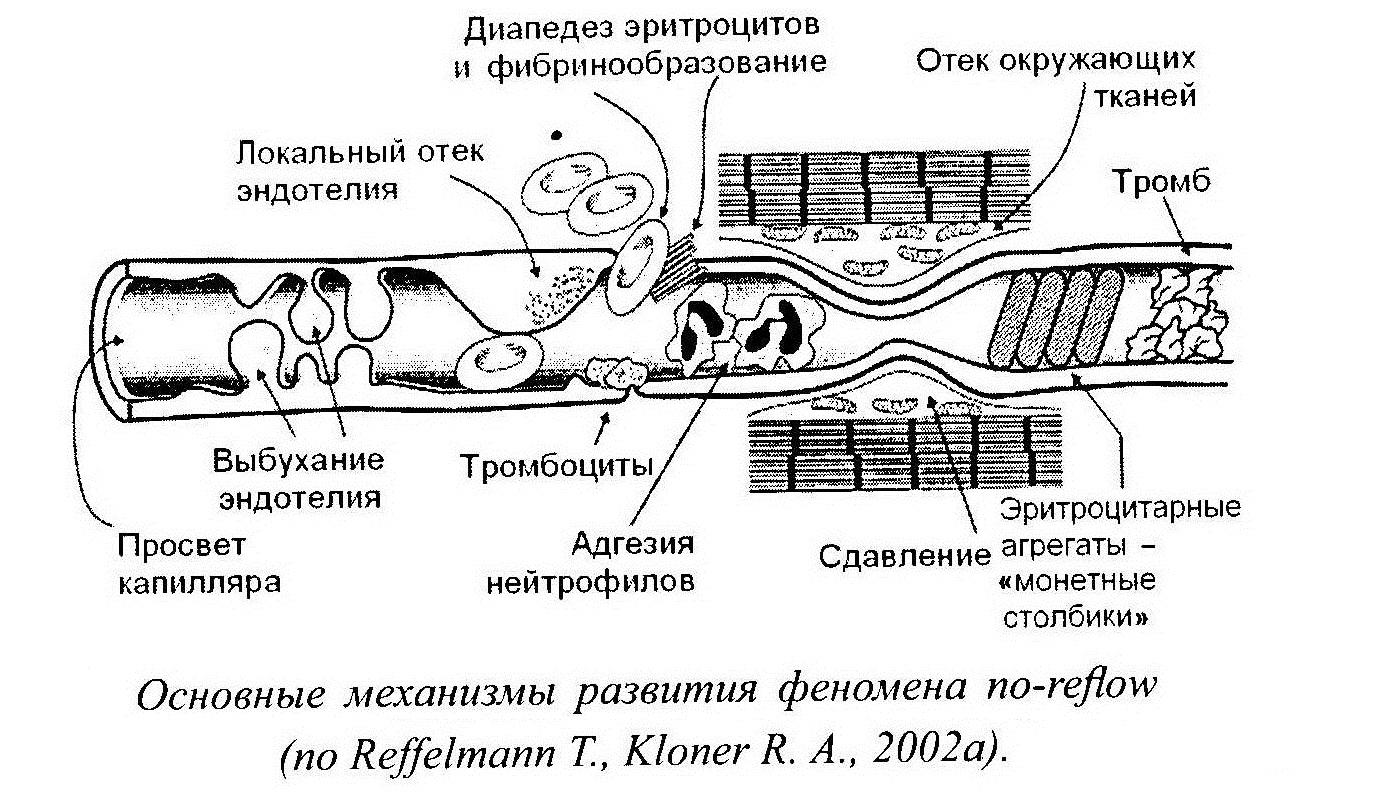
Отек эндотелиоцитов, способствующий уменьшению просвета капилляров.
Повреждение и истончение слоя гликокаликса, находящегося на люминальной поверхности эндотелия приводящее к адгезии активированных лейкоцитов к эндотелию с последующим повреждением микрососудов.
Закупорка сосудов микроциркуляторного русла лейкоцитарными агрегатами. вследствие адгезии лейкоцитов к эндотелию в результате усиленной экспрессии молекул адгезии на поверхности эндотелиоцитов и лейкоцитов.
Образование микротромбов и эритроцитарных агрегатов в просвете микрососудов.
Вазоконстрикция, обусловленная тромбоксаном А2, эндотелином-1 и серотонином.
Отек интерстиция и внутриклеточный отек кардиомиоцитов, что приводит к сдавлению микрососудов извне и уменьшению их просвета.
Для патогенетического лечения no-reflow применяют следующие подходы:
Коррекцию дисфункции эндотелия
Коррекция состояний, при которых имеются условия для нарушения микроциркуляции (СД, атеросклероз)
Профилактика и лечение тромбоза
Лечение тахиаритмий, при которых возрастает потребность миокарда в О2 и возникает риск развития ишемии.
Оглушенный (станнированный) миокард
Станнирование относится к состояниям, при которых выявляется стойкая систолическая дисфункция левого желудочка в отсутствие необратимого повреждения миокарда после реперфузии. Эти состояния обозначаются термином «жизнеспособный дисфункционирующий миокард». Феномен оглушенного (станнированного) миокарда проявляется обратимым угнетением сократимости миокарда, сохранившего жизнеспособность после реперфузии. Станнирование миокарда является осложнением реперфузии и является одной из форм реперфузионного повреждения миокарда. Дисфункция миокарда при станнировании может проявляться снижением, отсутствием или изменением сократительной активности левого желудочка.
Выраженность сократительной дисфункции после реперфузии зависит от целого ряда факторов:
продолжительности ишемического периода,
тяжести ишемии (полная или неполная),
степени восстановления кровотока после проведения соответствующих лечебных мероприятий
скорости восстановления коронарной перфузии,
объема ишемизированного миокарда
выраженности нагрузки на сердце.
Важным признаком оглушенного миокарда является наличие несоответствия между кровотоком и функцией миокарда: в то время как коронарный кровоток полностью или почти полностью восстановлен, сохраняются нарушения сократительной функции миокарда.
Механизмы станнирования
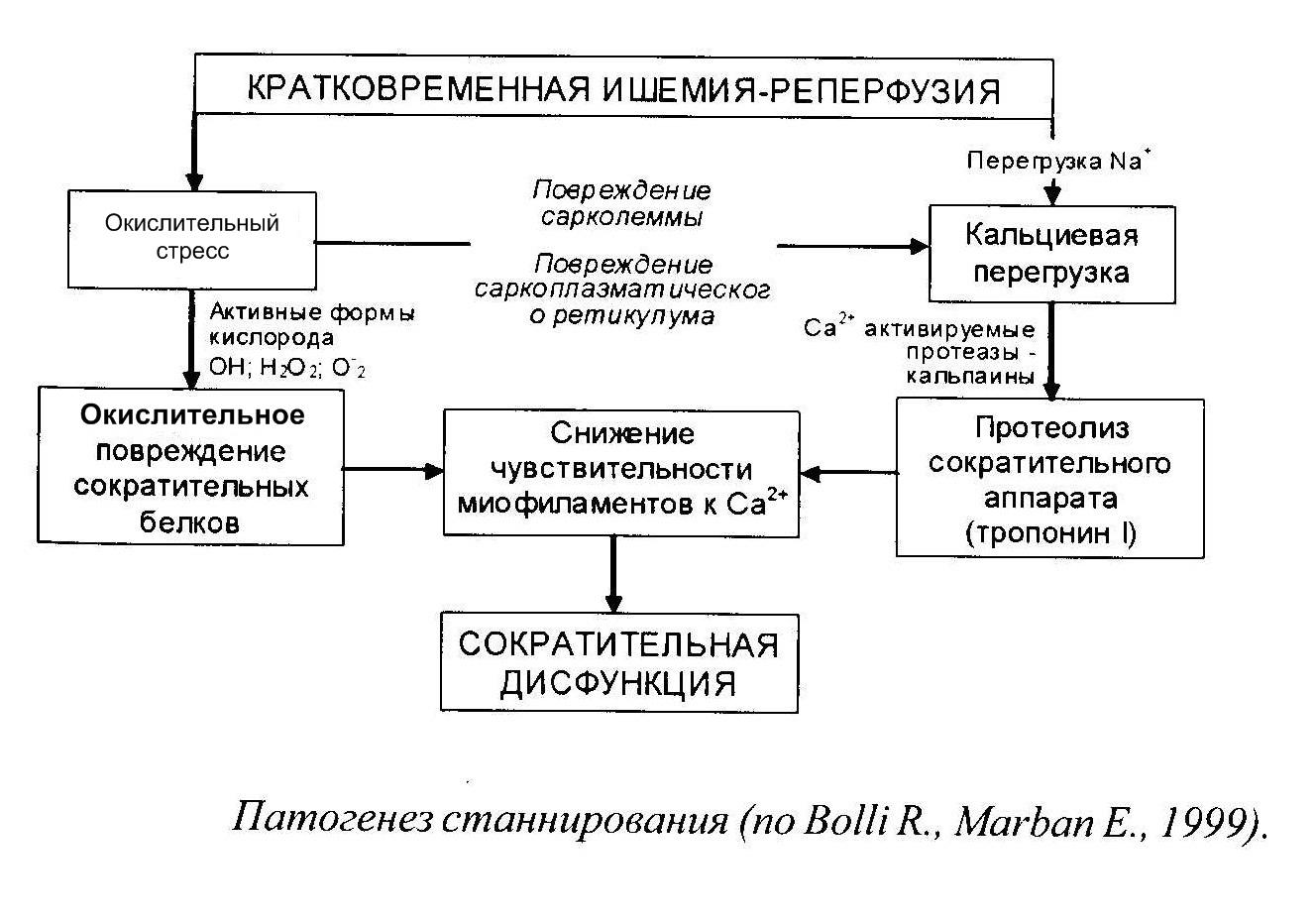
При реперфузии ишемизированного миокарда АФК и АФА образуются в результате нарушения процесса переноса электронов по дыхательным цепям митохондрий, активации различных ферментов, включая НАДФН-оксидазы, а также аутоокисления катехоламинов. АФК ингибируют Na+/K+-ATФазу, что приводит к перегрузке клетки Na+ и активации Na+/Ca2+обменника. Таким образом, избыточная продукция АФК вызывает повышенное поступление Ca2+ в клетку и, в конечном итоге, перегрузку клетки этими ионами. В то же время, АФК снижают чувствительность миофиламентов к Ca2+ путем избирательного повреждения некоторых сократительных белков. В ответ на повышение внутриклеточной концентрации Ca2+ активируется группа ферментов, объединенных общим названием кальпаины. Кальпаины широко распространены в клетках различных тканей, в т. ч. в миокарде. Эти ферменты вызывают ограниченный протеолиз, в результате которого из белков образуются крупные полипептидные фрагменты. Показано, что кальпаин-1 способен расщеплять как структурные белки сократительного аппарата, к которым относятся тайтин, а-фодрин, десмин и а-актинин, так и регуляторные белки, например, тропонин I и тропонин Т.
Наконец, АФК обладают способностью повреждать функцию саркоплазматического ретикулума.
О сущетвовании феномена оглушенного миокарда необходимо знать при выполнении операций в условиях искусственного кровообращения. Послеоперационная сократительная дисфункция миокарда в той или иной степени возникает во всех случаях, однако при длительной аноксии в период реоксигенации может развиваться тяжелое тотальное нарушение насосной функции сердца.
Важно помнить, что станнирование может развиваться у пациентов после успешно выполненной сердечно-легочной реанимации по поводу внезапной остановки сердца. Основными факторами, определяющими выраженность дисфункции миокарда при этом состоянии, являются продолжительности остановки сердца, степень ишемической контрактуры и возникновение феномена невосстановления кровотока.
Сократительная дисфункция достаточно легко выявляется методом эхокардиографии (ЭхоКГ). Перфузия миокарда может быть оценена с помощью сцинтиграфии миокарда или позитронно-эмиссионной томографии с одним из перфузионных агентов. Классическим признаком станнирования является нормальная или почти нормальная перфузия в участках миокарда с нарушенной сократимостью.
