
- •114 Марчук с.И., Петрущак с.В. Конспект лекций по курсу «Материаловедение»…
- •Введение
- •Строения материалов
- •2.1 Строение идеальных кристаллов
- •2.2 Дефекты кристаллического строения
- •2.3 Линейные дефектыМарчук с.И., Петрущак с.В. Конспект лекций по курсу «Материаловедение»…
- •2.4 Взаимодействие дефектов кристаллического строения
- •3.1 Упругая и пластическая деформация. Механизм пластической деформации.
- •3.2 Влияние холодной пластической деформации
- •3.3 Влияние нагрева на структуру и свойства деформированного металла.
- •4.1. Движущая сила кристаллизации
- •4.2. Гомогенная кристаллизация
- •4.3. Гетерогенная кристаллизация
- •4.4. Строение металлического слитка
- •4.5 Стеклование и аморфизация
- •Двухкомпонентных систем
- •5.1 Диаграмма фазового равновесия сплавов с неограниченной растворимостью в жидком и твердом состоянии
- •5.2 Диаграмма фазового равновесия сплавов с неограниченной растворимостью в жидком и ограниченной растворимостью в твердом состоянии
- •5.2.1 Диаграммы состояния эвтектического типа
- •5.2.3 Двойная диаграмма состояния перитектического типа
- •5.2.4 Диаграммы состояния двух компонентов, образующих промежуточные фазы
- •5.2.5 Двойные диаграммы состояния сплавов полиморфных компонентов и промежуточных фаз
- •Железо - углерод
- •6.1 Компоненты
- •6.2 Фазы в системе железо - углерод
- •6.3 Диаграмма состояния системы железо-углерод
- •6.4 Формирование структуры технического железа
- •6.5 Формирование структуры сталей
- •6.6 Влияние углерода и постоянных примесей на структуру и свойства сталей
- •6.7 Классификация и маркировка углеродистых сталей
- •6.8 Формирование структуры чугунов
- •6.8.1 Формирование структуры белых чугунов
- •6.8.2 Влияние скорости охлаждения на формирование структуры чугунов
- •6.8.3 Формирование структуры ковкого чугуна
- •6.8.4 Маркировка чугунов с графитом
- •7.1 Превращения при нагреве сталей
- •7.2 Превращения аустенита при охлаждении
- •7.2.I Распад аустенита в изотермических условиях
- •7.2.2 Распад аустенита в условиях непрерывного охлаждения
- •8.1 Отжиг
- •8.1.1 Отжиг первого рода
- •8.1.2 Отжиг второго рода
- •1 6 4,6 5 2 3 Отжиг 1 рода:
- •8.1.3 Виды отжига второго рода
- •8.2 Закалка стали
- •8.2.1 Способы объемной закалки
- •8.3 Отпуск закаленной стали
- •8.3.1 Превращения в закаленной стали при нагреве (отпуске )
- •8.3.2 Структура и свойства отпущенной стали
- •8.3.3 Виды отпуска
- •8.4 Поверхностное упрочнение стали
- •8.4.1 Поверхностная закалка
- •8.4.1.1 Структура и свойства стали после закалки твч
- •8.4.2 Химико-термическая обработка
- •8.4.2.1 Формирование структуры цементованного изделия
- •8.4.2.2 Термическая обработка после цементации
- •Время, ч
- •8.4.3 Азотирование стали
- •9.1 Влияние легирующих элементов на свойства фаз в сталях
- •9.1.2 Влияние легирующих элементов на устойчивость переохлажденного аустенита
- •9.2 Маркировка легированных сталей
- •9.3 Классификация легированных сталей
- •9.4 Конструкционные стали
- •9.4.1 Низколегированные строительные стали
- •9.4.2 Машиностроительные стали
- •9.4.2.1 Цементуемые стали
- •9.4.2.2 Улучшаемые стали
- •9.4.2.3 Рессорно-пружинные стали
- •9.4.2.4 Шарикоподшипниковые стали
- •9.4.2.5 Износостойкие стали
- •9.4.2.6 Коррозионностойкие стали
- •9.5 Инструментальные стали
- •9.5.1 Стали для режущего инструмента
- •9.5.2 Стали для деформирующего инструмента (штамповые стали)
- •9.5.3 Стали для мерительного инструмента
- •9.6 Твердые сплавы
- •10.1 Титан и его сплавы
- •10.2 Алюминий и его сплавы
- •10.3Магний и его сплавы
- •10.4 Медь и ее сплавы
- •11.1 Структура и основные свойства полимеров
- •11.2 Пластические массы
- •11.3 Резина
- •11.4 Стекло
- •11.5 Ситалы.
- •11.6 Керамика
- •11.7 Композиционные материалы
5.2.5 Двойные диаграммы состояния сплавов полиморфных компонентов и промежуточных фаз
Полиморфизмом или аллотропией называется способность простых и сложных веществ иметь различную кристаллическую решетку в зависимости от внешних условий (температуры и давления). Разные кристаллические формы одного и того же вещества называются полиморфными модификациями. Часто полиморфные металлы ограниченно взаимно растворяются в твердом состоянии. Вид диаграмм состояния таких систем усложнен. Полиморфными могут быть и промежуточные фазы.
Двойные диаграммы состояния сплавов с полиморфизмом компонентов будут рассмотрены на примере диаграммы железо-углерод.
ТЕМА № 6 АНАЛИЗ ДИАГРАММЫ СОСТОЯНИЯ СИСТЕМЫ
Железо - углерод
6.1 Компоненты
О сновным
компонентом является железо. Чистое
железо – металл серебристо-белого
цвета, атомный номер 26, атомная масса –
55.85, температура плавления – 1539°С. Железо
– полиморфный металл. Имеются 2 полиморфные
модификации (рис. 6.1).-модификация
– существует ниже 911°С, имеет
объемноцентрированную кубическую
решетку. В интервале 1392 – 1539°С железо
также имеет ОЦК решетку и его обозначают
как -Fe.
В интервале температур 911 – 1392°С
существует -железо
с гранецентрированной кубической
решеткой. Ниже температуры 768°С (точка
Кюри) -железо
ферромагнитно.
сновным
компонентом является железо. Чистое
железо – металл серебристо-белого
цвета, атомный номер 26, атомная масса –
55.85, температура плавления – 1539°С. Железо
– полиморфный металл. Имеются 2 полиморфные
модификации (рис. 6.1).-модификация
– существует ниже 911°С, имеет
объемноцентрированную кубическую
решетку. В интервале 1392 – 1539°С железо
также имеет ОЦК решетку и его обозначают
как -Fe.
В интервале температур 911 – 1392°С
существует -железо
с гранецентрированной кубической
решеткой. Ниже температуры 768°С (точка
Кюри) -железо
ферромагнитно.
Химически чистое железо содержит менее 0.0001% примесей и имеет твердость около 50 НВ. Твердость технически чистого железа (< 0.1 – 0.15% примесей) значительно выше – более 90 НВ. При этом в около 250 Н/мм2, относительное удлинение порядка 40%, относительное сужение – более 70%.
Углерод в твердом состоянии существует также в виде двух модификаций – графит и алмаз. Но для образования алмаза необходимы весьма специфические условия – высокая температура и очень высокое давление.
6.2 Фазы в системе железо - углерод
Основными фазами железоуглеродистых сплавов являются жидкие и твердые растворы углерода в железе, графит и цементит.
Твердый раствор внедрения углерода в - и -железе называется ферритом и характеризуется ОЦК решеткой. Высокотемпературный -феррит имеет максимальную концентрацию углерода 0,1%. Максимальная растворимость углерода в -феррите составляет 0,025% при 723°С. Феррит является мягким (около 80 НВ) и пластичным. Он ферромагнитен до 768 °С и парамагнитен при более высоких температурах.
Твердый раствор углерода в -железе называется аустенитом. Он характеризуется ГЦК решеткой. Аустенит, стабилизированный путем легирования, имеет твердость около 200 НВ и высокую упрочняемость. В отличие от феррита, в аустените не наблюдается хладноломкость. Он парамагнитен. Граничная растворимость углерода в аустените – около 2%.
Графит - одна из полиморфных модификаций углерода с гексагональной решеткой, в которой атомы расположены слоями. Между атомами углерода каждого слоя действуют сильные ковалентные связи. Слои находятся на большом расстоянии один от другого, и между ними действуют слабые поляризационные силы.
Ц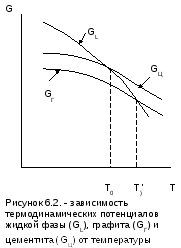 ементит
- карбид железа Fe3C
со сложной орторомбической решеткой.
Силы межатомной связи имеют комплексную,
вероятно, ковалентно-металлическую
природу. Цементит характеризуется
большой твердостью (около 70 HRC ) и
хрупкостью. В углеродистых железных
сплавах цементит является относительно
стойкой (метастабильной) фазой. Стабильной
высокоуглеродистой фазой, характеризующейся
минимальным значением термодинамического
потенциала, является графит (рис.6.2).
ементит
- карбид железа Fe3C
со сложной орторомбической решеткой.
Силы межатомной связи имеют комплексную,
вероятно, ковалентно-металлическую
природу. Цементит характеризуется
большой твердостью (около 70 HRC ) и
хрупкостью. В углеродистых железных
сплавах цементит является относительно
стойкой (метастабильной) фазой. Стабильной
высокоуглеродистой фазой, характеризующейся
минимальным значением термодинамического
потенциала, является графит (рис.6.2).
Для образования графита необходимо, чтобы в одном участке собралось 100% атомов углерода, поэтому считают, что образование графита выгодно термодинамически и для этого необходимо медленное охлаждение. Для образования цементита достаточно 25% атомов углерода, при этом из объема не удаляются все атомы железа, поэтому такой процесс может произойти быстрее и считают, что образование цементита выгоднее кинетически и происходит при ускоренном охлаждении.
