
61.08 Фізична хімія
.pdfЛабораторна робота №4
ЕЛЕКТРОПРОВІДНІСТЬ РОЗЧИНІВ ЕЛЕКТРОЛІТІВ
Мета роботи ознайомитися з класичним методом визначення електропровідності розчинів слабких та сильних електролітів та навчитися розраховувати питому та еквіваленту електропровідності розчинів електролітів, ступінь та константу дисоціації розчинів слабких електролітів та коефіцієнт електропровідності сильних електролітів.
Теоретичні відомості
За електричною провідністю розрізняють провідники першого і другого роду. До перших належать всі метали та їх сплави, а до других – розчини і розплави електролітів. В розчинах електролітів електричний струм проводиться за допомогою іонів, які переміщуються до відповідних електродів.
Згідно з теорією Арреніуса, молекули електролітів у водн их розчинах дисоціюють на іони, які і переносять електричний струм. Одні електроліти дисоціюють в розчинах повністю (сильні), інші частково (слабкі). Електрична провідність слабких електролітів визначається в основному ступенем дисоціації, яка залежить від концентрації електроліту і температури.
Властивість систем проводити електричний струм визначається опором або електричною провідністю. Опір R провідника пропорційний
його довжині l (м) і обернено пропорційний площині поперечного перерізу S (м2).
|
|
R ρ |
l |
|
(4.1) |
|
S |
||||||
|
|
|
|
|||
Коефіцієнт пропорційності (Ом м), який дорівнює опору провідника |
||||||
при l = 1 м і S= 1 м2 називається питомим опором. |
|
|||||
Електрична провідність – величина, обернена опору, Ом-1: |
|
|||||
I |
1 |
, |
(4.2) |
|||
|
||||||
|
R |
|
||||
а питомa електричнa провідність – величина, обернена питомому опору, См/м:
|
1 |
(4.3) |
|
|
|||
|
|
Питома електрична провідність електроліту – електрична провідність розчину об’ємом 1 м3, що міститься між двома паралельними електродами, площа кожного з яких становить 1 м2.
Питома електрична провідність являє собою струм, який переноситься через одиницю поперечного перерізу при градієнті потенціалу
31
1 В/м. Питома електрична провідність визначається швидкістю руху іонів (рухливістю), їх концентраціями в розчині і температурою.
Еквівалентна електрична провідність (молярна) визначається як електрична провідність розчину, в об’ємі якого міститься 1 г-екв розчиненого електроліту і який розміщений між двома паралельними металевими провідниками, віддаленими один від одного на 1 м, [См м2 /моль].
λ χ 1000 |
(4. 4) |
де = 1/С розведення, тобто число літрів розчину, в якому міститься 1 г-екв розчиненої речовини. Враховуючи швидкість руху іонів (катіонів та аніонів) ( k a ) , ступінь дисоціації електроліту , коефіцієнт
електропровідності f , можна записати:
F f |
( |
|
). |
|
(4. 5) |
|||
|
|
|
k |
|
a |
|
|
|
де F - стала Фарадея |
|
|
|
|
|
|
|
|
Прийнявши до уваги, що |
рухливість |
катіонів k F k . і аніонів |
||||||
a F a ., маємо |
|
|
|
|
|
|
|
|
f |
|
( |
k |
|
). |
(4. 6) |
||
|
|
|
|
a |
|
|||
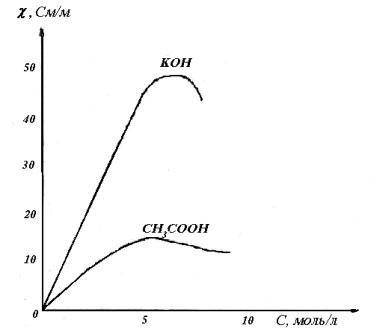
Залежність від концентрації наведена на рис.4.1.
Питома електрична провідність розчинів зростає зі збільшенням концентрації електролітів до певної межі, тому що в 1 мл об’єму збільшується кількість переносників електричного струму – іонів. Як видно з рис.4.1, для слабких електролітів при деякій концентрації питома електрична провідність зменшується, тому що зменшується ступінь їх дисоціації.
Для сильних електролітів зі збільшенням концентрації зменшується відстань між іонами, внаслідок чого зростає взаємне гальмування за рахунок наявності електрофоретичного та асиметричного ефектів і, відповідно, зменшується швидкість руху іонів. Крім того, зі збільшенням концентрації електроліту зростає в’язкість розчину, що також гальмує рух іонів.
Рис. 4.1. Залежність питомої електричної провідності від концентрації
32

розчину сильного та слабкого електроліту
Еквівалентна електрична провідність слабких і сильних електролітів (рис. 4.2) збільшується з розведенням: для слабких
– внаслідок збільшення ступеню дисоціації електроліту, для сильних
– внаслідок зростання рухливості іонів.
Рис. 4.2. Залежність еквівалентної електричної провідності від розведення розчину
Електрична провідність розчинів слабких електролітів
В розчинах слабких електролітів при значних розведеннях іони рухаються незалежно один від одного і їх електрична провідність при
нескінченному розведенні підпорядковується правилу адитивності, |
тому коли |
||||
f =1 рівняння (4.6) має вигляд |
|
|
|
||
|
(4.7) |
||||
|
|
|
k |
a |
|
При нескінченному розведені величина ступеню дисоціації прямує |
|||||
до одиниці =1, отже: |
|
|
|||
|
(4.8) |
||||
|
|
k |
a |
|
|
Виходячи із рівнянь 4.7 та 4.8, отримуємо закон Арреніуса: |
|
||||
|
λ |
|
(4.9) |
||
λ |
|
|
|||
Математичний вираз рівняння (4.8) отримав назву закону Кольрауша: еквівалентна електрична провідність при нескінченному розведенні дорівнює сумі рухливостей іонів.
Електрична дисоціація являє собою зворотній процес, тому до нього може бути застосований закон діючих мас і константа електролітичної дисоціації, наприклад, для оцтової кислоти може бути записана
КСН ССН3СОО
ДССН3СООН
Якщо загальна концентрація С, а ступінь дисоціації ,
СН ССН3СОО С ; ССН3СООН С (1 )
33

Тоді константа дисоціації з врахуванням (4.9) буде мати вигляд:
|
|
С С |
|
2 |
С |
|
|
2 |
С |
|
|||
К |
|
|
|
|
|
|
. |
(4.10) |
|||||
Д |
|
|
|
|
|
|
|||||||
|
С(1 |
) |
1 |
|
|
( |
|
) |
|
||||
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|||
Рівняння (4.10) дістало назву закону розведення Оствальда, відповідно до якого константа електролітичної дисоціації за сталої температури не залежить від концентрації розчину (як константа рівноваги процесу дисоціації).
Електрична провідність розчинів сильних електролітів
Сильні електроліти внаслідок повної дисоціації не підлягають закону діючих мас. Еквівалентна електрична провідність сильних електролітів відрізняється від такої слабких електролітів не тільки значенням, але й характером залежності від концентрації. Так, якщо навести графічно залежність від 
 С , для слабких електролітів у ділянці великих розведень одержується крива, а для сильних — пряма лінія, яка описується емпіричним рівнянням
С , для слабких електролітів у ділянці великих розведень одержується крива, а для сильних — пряма лінія, яка описується емпіричним рівнянням
|
|
|
|
|
|
|
а С |
(4.11) |
|
|
|
|
|
|
В цьому рівнянні коефіцієнт а залежить від природи розчинника і температури. В цілому другий член рівняння а
 С xaрактеризує зменшення електричної провідності за рахунок взаємного гальмування іонів. Для визначення ∞ проводять лінійну екстраполяцію до нульової концентрації. Відрізок, який відсікається на осі ординат, відповідає значенню ∞. Одержані значення порівняють з вирахуваними за рівнянням (4.8), яке справедливе для розведених розчинів сильних електролітів. Відношення електричної провідності за даної концентрації до електричної провідності при нескінченному розведенні для сильних електролітів називається коефіцієнтом електричної провідності
С xaрактеризує зменшення електричної провідності за рахунок взаємного гальмування іонів. Для визначення ∞ проводять лінійну екстраполяцію до нульової концентрації. Відрізок, який відсікається на осі ординат, відповідає значенню ∞. Одержані значення порівняють з вирахуваними за рівнянням (4.8), яке справедливе для розведених розчинів сильних електролітів. Відношення електричної провідності за даної концентрації до електричної провідності при нескінченному розведенні для сильних електролітів називається коефіцієнтом електричної провідності
|
|
|
|
|
f |
|
|
. |
(4.12) |
|
||||
|
|
|
|
|
|
|
|
|
|
Цей коефіцієнт може приймати значення менше одиниці не в результаті неповної дисоціації, а за рахунок міжіонної взаємодії.
Методика виміру електричної провідності
Схему приладу для визначення опору провідника наведено на рис.4.3. Вона принципово не відрізняється від схеми моста для вимірювання опору провідників першого роду. Перша відмінність схеми полягає в тому, що для живлення моста тут застосовується не постійний, а змінний струм. Це є необхідним для того, щоб уникнути електролізу розчину і поляризації електродів. Суть цього явища: в результаті проходження постійного струму через розчин електроліту, наприклад, у розчині СН3СООН, на електродах відбуватимуться такі процеси:
на катоді 2Н++ 2е→2Н→Н2
34

на аноді 4ОН–– 4е→О2+2Н2О
|
Таким чином, при вимірах |
||||||
|
опору |
електроліту |
буде |
||||
|
додаватися опір на електродах |
||||||
|
в результаті |
газовиділення. |
|||||
|
Джерелом змінного струму, як |
||||||
|
правило, |
|
є |
|
генератори |
||
|
звукової |
частоти. |
Задовільні |
||||
|
результати |
одержують |
при |
||||
|
вимірюванні |
з |
використанням |
||||
|
струму |
промислової частоти |
|||||
|
(50 Гц). Так, на схемі (рис. |
||||||
|
4.3) струм |
|
від |
джерела |
|||
Рис. 4.3. Схема для вимірювання |
надходить в точку А, де він |
||||||
розгалужується до точок О і К, |
|||||||
електричної провідності розчинів |
|||||||
а потім через точку В |
|||||||
|
|||||||
|
повертається до джерела. |
|
|||||
Повзучий контакт К дозволяє, змінюючи співвідношення опорів R1 |
і R2, |
||||||
досягти відсутності струму в ланцюгу ОК, що фіксується індикатором (НІ). У якості індикатора може бути використаний осцилограф або гальванометр змінного струму.
Завдання на виконання роботи
1.Визначити електричну сталу посудини (електролітична комірка).
2.Встановити залежність питомої електропровідності від концентрації слабких та сильних електролітів.
3.Встановити залежність еквівалентної електропровідності від концентрації слабких та сильних електролітів.
4.Визначити ступінь дисоціації та константу дисоціації залежно від концентрації слабких електролітів.
5.Визначити коефіцієнт електропровідності сильних електролітів.
Установки, прилади, лабораторний посуд, реактиви
Реохордний міст Р-38, посудина для вимірів, електричні провідники І роду, 0,02 н розчин КСl, розчини електролітів, піпетки на 20 або 25 мл.
35
Лабораторна робота № 4.1 ВИЗНАЧЕННЯ ЕЛЕКТРОПРОВІДНОСТІ РОЗЧИНІВ СЛАБКИХ
ЕЛЕКТРОЛІТІВ
Порядок виконання роботи
1. Визначення сталої посудини проводять за допомогою 0,02 н розчину КСl, питомий опір якого відомий. В посудину, попередньо промиту цим же розчином наливають його стільки, щоб рівень рідини на 3–5 мл перевищував верхній край електродів. Визначають Rx з використанням моста Р-38 і підставляють в рівняння
|
|
|
Const KCL Rx |
|
|
(4.1) |
|
Значення |
KCl беруть з табл. 4.1 при відповідній температурі. |
|
|||||
|
|
|
|
|
|
|
Таблиця 1 |
См/ см |
|
0,002243 |
0,002397 |
0,002501 |
0,002606 |
|
0,002765 |
С |
|
15 |
18 |
20 |
22 |
|
25 |
2.Вимірюють опори розчинів електроліту різної концентрації. Для цього
впосудину, яку попередньо промили цим же розчином, заливають розчин елекроліту того ж об’єму, що і при визначенні сталої посудини, а потім методом послідовного розведення одержують розчини 1:1; 1:2; 1:4; 1:8; 1:16. Після кожного розведення розчини перемішують. При всіх вимірах об’єм рідини в посудині повинен бути одним і тим же. (Зауваження: в процесі роботи з мостом Р-38 необхідно слідкувати за надійністю контактів та відсутністю короткого замикання в ланцюгу електродів).
Опрацювання результатів
1. Розраховують питому електропровідність розчинів слабких електролітів
|
const |
(4.14) |
|
Rx |
|||
|
|
2.За формулами (4.4), (4.8), (4.9), (4.10) розраховують , , і КД для досліджуваних концентрацій. Для розрахунків значення к і a беруть із довідкових таблиць.
3.Одержані дані заносять до табл.4.2.
Таблиця 4.2
№ |
|
|
|
|
const |
|
λ χ 1000 |
|
К |
|
|
|
2 С |
. |
|
С |
=1/С |
Rx |
|
= / ∞ |
Д |
1 |
|
||||||||
п/п |
Rx |
|
|
|
|
||||||||||
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||
4.Знаходять середнє значення константи дисоціації і порівнюють його з табличним.
5.Будують графіки залежностей ( , , ) = f(C).
36

Лабораторна робота № 4.2 ВИЗНАЧЕННЯ ЕЛЕКТРОПРОВІДНОСТІ РОЗЧИНІВ СИЛЬНИХ
ЕЛЕКТРОЛІТІВ
Порядок виконання роботи
1.Визначення сталої посудини проводять відповідно до п.1 роботи № 4.1.
2.Вимірюють опори розчинів електроліту різної концентрації відповідно до п.2 роботи № 4.1.
Опрацювання результатів
1.За формулами (4.14) та (4.4) обчислюють питому та еквівалентну електропровідність.
2.Одержані дані заносять до табл. 4.3.
Таблиця 4.3
№ |
С |
|
Rx |
|
|
const |
|
|
λ |
|
|
|
1000 |
|
|
|
|
fλ |
|
|
|
|
|
|
С |
|
|||||||||||||
п/п |
|
|
Rx |
|
|
|
|
|
|||||||||||
C |
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
3. Еквівалентну електропровідність за нескінченного розведення |
|||||||||||||||||||
|
|
|
– |
|
|
|
|
|
|||||||||||
знаходять за |
графіком |
в координатах |
|
С , отриману |
пряму |
лінію |
|||||||||||||
екстраполюють на вісь ординат, точка перетину з ординатою дає значення .
4.Отриману величину порівнюють із розрахованою за рівнянням (4.8).
5.Розраховують коефіцієнт електропровідності для всіх концентрацій за формулою (4.12).
Оцінка похибки вимірювань
1. В загальну похибку |
|
входить |
відносна похибка |
вимірів |
|
електропровідності, яка дорівнює: |
|
|
|
|
|
R |
|
R1 |
R2 |
, |
(4.15) |
R |
|
R1 |
R2 |
|
|
де R – абсолютна похибка при вимірах плеча моста. Відношення тим більше, чим менше плече. Похибка мінімальна при R1 = R2. Для обчислення похибки при вимірах електропровідності слід брати до уваги похибки при вимірах сталої посудини і розчину електроліту.
Прийнявши R 2мм і R1 = R2 = 250мм , отримаємо:
|
|
2 R |
|
2 R |
|
8 |
0.032, |
тобто 3,2 % |
|
|
R |
R |
25 |
||||||
|
|
|
|
|
У відповідності з цим, питому електропровідність слід розраховувати з точністю до третьої значущої цифри. Але це в кращому випадку.
2.Похибка роботи самого моста Р-38 складає 5 % .
3.Похибка при заповненні посудини розчином за допомогою піпетки на 20
мл складає приблизно 0,3/20=0,015; тобто 1,5 % .
37
4. Таким чином, загальна похибка може сягати 10 % .
Аналіз одержаних результатів, висновки
На основі аналізу результатів дослідів та керуючись довідниковими даними, студенти роблять висновок про приналежність досліджуваного електроліту до того чи іншого класу.
Питання для самоперевірки
2.Охарактеризуйте типи провідників.
3.Чим відрізняються сильні електроліти від слабких?
4.Що називають питомою електричною провідністю розчину? Як змінюється її значення з концентрацією в сильних та слабких електролітах? Які фактори зумовлюють цю зміну?
5.Як експериментально вимірюють питому електричну провідність? Одиниця питомої електричної провідності.
6.Що називається еквівалентною електричною провідністю? Як змінюється її значення зі зменшенням концентрації розчинів сильних та слабких електролітів? Чинники, що зумовлюють зміну. Одиниця еквівалентної електричної провідності.
7.Що називають абсолютною швидкістю іону, рухливістю? Сформулюйте закон Кольрауша.
8.Сформулюйте закон розведення Оствальда.
9.Який зв’язок існує між ступенем дисоціації та ізотонічним коефіцієнтом?
10.Охарактеризуйте схему та принцип вимірювання електричної провідності. Чому вимір опору розчинів електролітів рекомендують проводити
звикористанням змінного струму?
11.Стала посудини та її вимірювання. Одиниця сталої посудини.
38
Лабораторна робота № 5
ЕЛЕКТРОРУШІЙНІ СИЛИ
Мета роботи навчитися вимірювати електрорушійні (ЕРС) сили гальванічних елементів, складених з електродів першого та другого роду та на основі отриманих експериментальних даних обчислювати електродні потенціали досліджуваних електродів.
Теоретичні відомості
Електрохімія вивчає закономірності перетворення енергії хімічних реакцій в електричну при збереженні загального енергетичного балансу. Таке перетворення практично реалізується для електрохімічних систем в формі роботи гальванічних елементів, у яких проходять окисно-відновні реакції.
На межі поділу любих двох фаз тверда–тверда, (наприклад Zn/Сu, Cd/Ag), тверда–рідка, (наприклад Zn/розчин ZnSO4, Cu/розчин CuSO4), рідка–рідка (розчин ZnSO4, розчин CuSO4), кожна з яких окремо є електронейтральною, виникає стрибок електричного потенціалу.
Розглянемо систему, яку в електрохімії називають "метал в розчині своїх іонів" (прикладом є мідна пластинка занурена в розчин сульфату міді). Через деякий час на межі Cu/розчин CuSO4 встановлюється рівновага, обумовлена рівністю хімічних потенціалів речовини в обох фазах і їй відповідає рівноважний стрибок потенціалу.
В розглянутому випадку іони міді в металі містяться у вузлах металевої ґратки, а в водному розчині вони гідратовані. Щоб вилучити іони міді з розчину, необхідно подолати енергію гідратації Uг, тобто енергію зв’язку його з молекулами води, а для видалення іону з металевої ґратки, необхідно подолати енергію Uв , що дорівнює роботі виходу іона з металу. При зануренні металевої пластинки в розчин своїх іонів напрям переходу іонів визначається співвідношенням Uг і Uв, тобто, якщо Uв Uг (як для міді) – іони металу будуть переходити із розчину на межу поділу метал–розчин. Оскільки іони міді несуть позитивні заряди, пластинка набуде позитивного заряду, а розчин – негативного. Відповідні заряди в обох середовищах (позитивні в металі і негативні в розчині) розташовуються поблизу поверхні, утворюючи на поверхні метал – розчин подвійний електричний шар (ПЕШ). При співвідношенні Uв Uг, метал зарядиться негативно, а розчин – позитивно (рис. 5.1). В цьому випадку подвійний електричний шар утворюється надлишковими електронами на металі та іонами металу в розчині.
39

Рис. 5.1. Схема утворення подвійного електричного шару (ПЕШ)
Різниця потенціалів , що виникає між металом і розчином, називається міжфазовим потенціалом. Прямих методів вимірювання абсолютних значень міжфазових потенціалів поки що немає, можна виміряти лише різницю потенціалів між точками, що знаходяться в межах однієї фази.
Гальванічний елемент – це пристрій для перетворення хімічної енергії будь-якої окиснювально-відновної реакції в електричну енергію.
Розглянемо гальванічний елемент Якобі - Даніеля, схема якого наведена на рис. 5.2.
Рис. 5.2. Схема гальванічного елемента Даніеля-Якобі: 1 – цинковий напівелемент;
2 – цинковий електрод; 3 – розчин ZnSO4;
4, 5 – скляні трубки з зовнішніми проводами; 6 – розчин CuSO4; 7 – мідний напівелемент; 8 – мідний електрод; 9 – склянка з насиченим розчином KCl (соляний місток)
Контакт між електродами здійснюється за допомогою з'єднуючого провідника (будь-якого провідника першого роду), а контакт між електролітами – за допомогою пористої перетинки, що перешкоджає механічному змішуванню розчинів і не перешкоджає переносу струму іонами, або за допомогою проміжного агар-агарового містка, виготовленого на розчині хлористого калію. Цей кордон розділяє гальванічний елемент на два напівелементи.
40
