
1stAttestationOCh
.pdf
1. Реакции электрофильного ароматического замещения
Галогенирование
Алкилирование по ФриделюКрафтцу
Ацилилирование по ФриделюКрафтцу
Нитрование
Сульфирование
+Cl2
+CH3Cl
O
+CH3 C Cl
Cl
+ O
O
+HO N
O-
O
+ HO S OH
O
AlCl3
AlCl3
AlCl3
H2SO4
SO3
Cl

 CH3
CH3
O
C CH3
CH3
O
N O
O
+ 
 -
-
O
S OH O
8

Электрофильное замещение водорода в бензольном кольце
образование образование π-комплекса σ-комплекса
9

Механизм:
Шаг 1: Атака электрофила с образованием σ-комплекса
σ-комплекс Шаг 2: Потеря протона с образованием продукта замещения
основание
основание-Н
10

1a. Галогенирование
Бензол не реагирует с бромом и хлором, взаимодействие
возможно только в присутствии кислоты Льюиса.
|
Br |
Br |
FeBr3 |
Br |
Br |
FeBr |
|
|
|
|
|
|
3 |
|
H |
|
|
H |
|
|
|
|
|
H |
|
|
|
|
|
|
H |
|
Br |
|
H |
H |
|
|
_ |
||
|
|
Br |
|
|||
|
Br |
Br |
FeBr3 |
+ FeBr4 |
+ HBr |
|
|
+ |
|||||
H |
H |
|
H |
H |
|
|
|
|
|
|
|
||
|
H |
|
|
H |
|
|
|
|
|
|
|
|
11
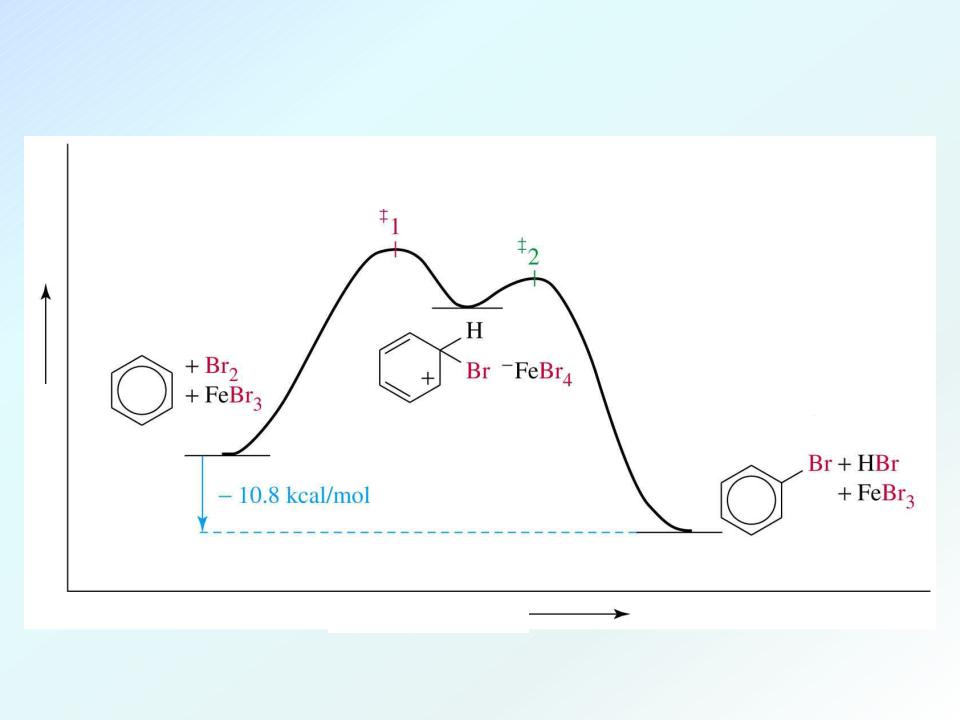
Энергетический профиль реакции бромирования:
энергия
Скорость-определяющая стадия
реагирующие
вещества
интермедиат |
продукты |
|
координата реакции
12

Хлорирование и йодирование
•Хлорирование протекает аналогично бромированию.
В качестве кислоты Льюиса обычно используют AlCl3.
•Йодирование возможно только в присутствии кислотного окислителя, как азотная кислота, которая окисляет йод до йодоний-катиона.
H+ + HNO3 + 1/2 I2 |
I+ |
+ NO2 + H2O |
HNO3 I
+ I2
86% |
13 |
|

1b. Нитрование бензола
|
H2SO4 |
|
|
|
|
NO2 |
|
|
|
|
|
|
|
||
+ HNO3 |
|
|
|
|
+ H O+ |
+ HSO - |
|
|
|
|
|
|
|||
|
|||||||
|
50-55oC |
|
|
|
3 |
4 |
|
|
85% |
|
|
|
|||
|
|
|
|
|
|||
Для образования электрофила – катиона нитрония –
необходима серная кислота.
O |
O |
H |
O |
_ |
|
|
|
|
|
H O S O H |
H O N |
H O |
N + HSO4 |
|
O |
O |
+ |
O |
|
|
|
|||
H O |
O |
NO + |
затем образует |
2 |
|
H O N |
H2O + |
N |
+ |
сигма-комплекс с бензолом, |
|||
теряет H+ с образованием |
|||||||
+ |
O |
|
O |
|
|||
|
|
|
продукта нитрования |
14 |
|||
|
|
|
|
|
|||
|
|
|
|
|
|
||

Механизм:
катион нитрония
сигма-связь
медленно
HSO4-
быстро
15

1c. Сульфирование бензола
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
||||
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
S |
|
OH |
||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||
+ |
|
|
|
|
concd |
. |
H2SO4 |
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
S |
25 oC |
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
O |
|||||||||||
|
O |
|
|
O |
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
триоксид серы |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
бензолсульфоновая кислота |
|||||||||||||
|
Sulfur trioxide |
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
Benzenesulfonic acid |
||||||||
|
|
|
|
|
|
|
|
|
||||||||||
±½»ÇËá.
(56%)
SO3, растворенный в концентрированной серной кислоте, |
||||||
является электрофилом |
|
|
|
|
|
|
O |
_ |
|
|
|
|
|
O |
|
O |
|
O |
|
|
S |
S + |
|
S + |
|
S + |
|
O O |
O O |
O |
O |
_ |
_ O O |
|
|
|
H |
_ |
|
HO |
O |
O |
|
O |
|
S |
||
|
|
|
|
|||
|
S |
O |
|
|
|
|
S |
|
|
|
O |
||
O |
+ |
O |
|
|
|
|
O |
H |
|
|
|
||
|
|
|
|
|||
|
|
|
|
|
||
|
|
|
|
benzenesulfonic acid |
||
|
|
|
|
|
||
|
|
|
|
|
|
16 |

Десульфирование
Каждая стадия сульфирования является равновесной; следовательно, вся реакция целиком является обратимой. Таким образом, как Ar-H может быть просульфирован в конц. H2SO4, так и Ar-SO3H может быть десульфирован (с образованием Ar-H) путем кипячения в разбавленной серной кислоте.
Этот процесс используют для получения дейтеробензола:
|
H |
|
|
|
D |
||||||
|
|
D |
|
|
|
D |
|||||
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
large excess |
|
|
|
|||
H |
|
|
|
H |
большой избыток |
|
|
|
|||
|
|
|
|
|
D2SO4/D2O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
H |
|
D |
|
|
|
D |
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
D |
|||
|
H |
|
|
|
|||||||
|
|
d6Benzene-бензол-d6 |
17 |
||||||||
|
|
|
|
|
|
||||||
