
- •Методичні матеріали
- •Тема 2. Рівноприскорений прямолінійний рух. Рух тіла по вертикалі під дією сили тяжіння.
- •Тема 3. Рух по параболі під дією сили тяжіння
- •Тема 4. Рівномірний рух по колу
- •Тема 5. Закони ньютона
- •Тема 6. Закон всесвітнього тяжіння. Супутники.
- •Тема 7. Сила пружності. Вага і невагомість.
- •Тема 8. Сили тертя.
- •Тема 9. Динаміка руху тіла по колу.
- •Тема 10. Динаміка руху системи зв'язаних та статичних тіл
- •Тема 11. Статика.
- •Тема 12. Закон збереження імпульсу.
- •Тема 13. Механічна робота. Потужність. Ккд. Прості механізми
- •Тема 14. Закон збереження механічної енергії
- •Тема 15. Елементи механіки рідин і газів
- •Тема 16. Основи молекулярно-кінетичної теорії
- •Тема 17. Рівняння стану ідеального газу. Ізопроцеси
- •Тема 18. Насичена пара. Вологість повітря
- •Тема 19. Поверхневий на тяг. Капілярність
- •Тема 20. Властивості твердих тіл. Механічні деформації
- •Тема 21. Основи термодинаміки
- •Тема 22. Зміна агрегатних станів речовини. Рівняння теплового балансу
- •Тема 23. Закон кулона. Напруженість поля
- •Тема 24. Потенціал. Різниця потенціалів. Робота електростатичного поля
- •Тема 25. Електроємність. Конденса тори
- •Тема 26. Постійний струм. Закон ома для ділянки кола
- •Тема 27. Закон ома для повного (замкненого) кола
- •Тема 28. Робота і потужність струму. Закон джоуля – ленца
- •Тема 29. Струм у різних середовищах
- •Тема з0. Магнітне поле
Тема 16. Основи молекулярно-кінетичної теорії
• Основні положення молекулярно-кінетичної теорії (МКТ):
1) Речовина складається з частинок, між якими є проміжки. Структурними елементами речовини є атоми, молекули, іони.
Атом — найдрібніша частинка хімічного елемента, що зберігає його хімічні властивості. Різновидів атомів існує стільки, скільки хімічних елементів міститься в таблиці Менделєєва. Молекула — найдрібніша частинка хімічної сполуки, що зберігає її хімічні властивості. Молекули складаються з атомів. Молекули різних речовин відрізняються набором атомів, що входять до складу молекули. Іон— електрично заряджена частинка, яка утворилась шляхом утрати (позитивний іон) або приєднання (негативний іон) атомом електронів. Електрон – елементарна негативно заряджена частинка.
Ч
 астинки
речовини перебувають у неперервному
хаотичному русі. Характер руху частинок
за агрегатного стану. Швидкість руху
частинок залежить від температури.
астинки
речовини перебувають у неперервному
хаотичному русі. Характер руху частинок
за агрегатного стану. Швидкість руху
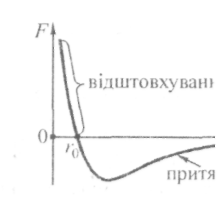
частинок залежить від температури.Між частинками речовини діють сили притягання і сили відштовхування. Рівнодійну цих сил називають силою взаємодії молекул (атомів). При зменшенні відстані між частинками переважають сили відштовхування, а при збільшенні — сили притягання.
На
рисунку зображено графік залежності
модуля рівнодійної сил від відстані
між частинками, де r0
—
відстань, на якій![]() ,
тобто
,
тобто![]()
• Досліди, що підтверджують основні положення МКТ.
Дифузія — явище самовільного змішування речовин унаслідок хаотичного руху частинок цих речовин. Швидкість дифузії залежить від агрегатного стану та температури речовини.
Броунівський рух — невпорядкований рух мікрочастинок у рідині або газі, зумовлений хаотичним рухом молекул середовища.
— Виникнення
сил пружності при механічних
деформаціях.
Розміри атомів і молекул
дуже малі. Атом в основному стані має
розмір близько![]()
Молекули
неорганічних сполук мають розміри 1–3![]() ,
а молекули органічних сполук — сотні
ангстрем.
,
а молекули органічних сполук — сотні
ангстрем.
Маси атомів і молекул дуже малі. їх виражають в атомних одиницях маси (а.о.м). 1 а.о.м. дорівнює 1/12 маси атома Карбону
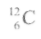
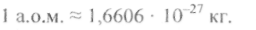
Відносна атомна (молекулярна) маса — це маса атома чи молекули в а.о.м.
![]()
де![]() —
маса молекули (атома) даної речовини,
—
маса молекули (атома) даної речовини,![]() —
маса атома Карбону. Відносна атомна
маса елементів міститься в таблиці
Менделєєва.
—
маса атома Карбону. Відносна атомна
маса елементів міститься в таблиці
Менделєєва.
1 моль — це кількість речовини, що містить стільки ж частинок, скільки їх є у 12 г Карбону
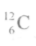
Стала Авогадро — величина, яка чисельно дорівнює кількості частинок в 1 молі будь-якої речовини.
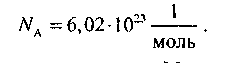
Молярна маса М — маса одного моля даної речовини.
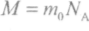 .
Одиницею вимірювання молярної маси у
СІ є
.
Одиницею вимірювання молярної маси у
СІ є .
.
Молярна
та відносна атомна маси зв'язані
співвідношенням
![]()
Молярну масу будь-якої хімічної сполуки можна обчислити, використавши дані таблиці Мєндєлєєва.
Наприклад:![]()
• Кількість речовини v — це кількість молів у даній масі речовини.
![]()
де![]() —
кількість частинок у даній масі речовини.
Одиницею вимірювання кількості речовини
у СІ є 1 моль – еталон. Кількість речовини
суміші дорівнює сумі кількостей речовини
окремих компонентів.
—
кількість частинок у даній масі речовини.
Одиницею вимірювання кількості речовини
у СІ є 1 моль – еталон. Кількість речовини
суміші дорівнює сумі кількостей речовини
окремих компонентів.
![]()
• Кількість атомів чи молекул у даній масі речовини можна обчислити за формулою
![]()
