
- •Методичні матеріали
- •Тема 2. Рівноприскорений прямолінійний рух. Рух тіла по вертикалі під дією сили тяжіння.
- •Тема 3. Рух по параболі під дією сили тяжіння
- •Тема 4. Рівномірний рух по колу
- •Тема 5. Закони ньютона
- •Тема 6. Закон всесвітнього тяжіння. Супутники.
- •Тема 7. Сила пружності. Вага і невагомість.
- •Тема 8. Сили тертя.
- •Тема 9. Динаміка руху тіла по колу.
- •Тема 10. Динаміка руху системи зв'язаних та статичних тіл
- •Тема 11. Статика.
- •Тема 12. Закон збереження імпульсу.
- •Тема 13. Механічна робота. Потужність. Ккд. Прості механізми
- •Тема 14. Закон збереження механічної енергії
- •Тема 15. Елементи механіки рідин і газів
- •Тема 16. Основи молекулярно-кінетичної теорії
- •Тема 17. Рівняння стану ідеального газу. Ізопроцеси
- •Тема 18. Насичена пара. Вологість повітря
- •Тема 19. Поверхневий на тяг. Капілярність
- •Тема 20. Властивості твердих тіл. Механічні деформації
- •Тема 21. Основи термодинаміки
- •Тема 22. Зміна агрегатних станів речовини. Рівняння теплового балансу
- •Тема 23. Закон кулона. Напруженість поля
- •Тема 24. Потенціал. Різниця потенціалів. Робота електростатичного поля
- •Тема 25. Електроємність. Конденса тори
- •Тема 26. Постійний струм. Закон ома для ділянки кола
- •Тема 27. Закон ома для повного (замкненого) кола
- •Тема 28. Робота і потужність струму. Закон джоуля – ленца
- •Тема 29. Струм у різних середовищах
- •Тема з0. Магнітне поле
Тема 17. Рівняння стану ідеального газу. Ізопроцеси
• Стан газу характеризують кілька фізичних величин — тиск р, об'єм V, абсолютна температура Т, які називають макроскопічними параметрами стану. Стан, у якому всі параметри як завгодно довго залишаються незмінними, називають станом термодинамічної рівноваги.
• Рівняння стану ідеального газу (рівняння Менделєєва — Клапейрона) описує зв'язок між трьома макроскопічними параметрами в стані термодинамічної рівноваги і має вигляд:
![]() ,
,
де![]() —
кількість речовини,М
— молярна маса ідеального газу,
—
кількість речовини,М
— молярна маса ідеального газу,
![]() —універсальна
газова стала.
—універсальна
газова стала.
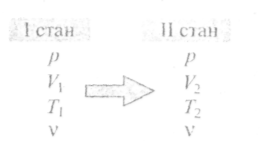
• Термодинамічний
процес —
це перехід ідеального газу з одного
стану в інший, що супроводжується зміною
параметрів газу. Схематично термодинамічний
процес можна зобразити так:
Термодинамічний
процес —
це перехід ідеального газу з одного
стану в інший, що супроводжується зміною
параметрів газу. Схематично термодинамічний
процес можна зобразити так:
• Якщо
під час термодинамічного процесу
кількість речовини не змінюється![]() ,
то з рівняння стану слідує, що
,
то з рівняння стану слідує, що .
Це рівняння називаютьоб'єднаним
газовим законом (ОГЗ),
або рівнянням Клапейрона.
.
Це рівняння називаютьоб'єднаним
газовим законом (ОГЗ),
або рівнянням Клапейрона.
• Ізопроцес—
це теомодинамічний процес, що відбувається
зі сталою кількістю речовини, при якому
один із параметрів (тиск![]() об'єм
об'єм![]() абсолютна
температура
абсолютна
температура![]() залишається
незмінним.
залишається
незмінним.
• Ізотермічний процес — це ізопроцес, при якому температура ідеального газу не змінюється.
З
ОГЗ слідує, що
![]() ,
або — закон Бойля — Маріотта.
,
або — закон Бойля — Маріотта.
З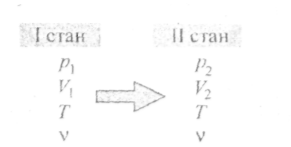 а
незмінної температури та кількості
речовини
тиск
ідеального газу обернено пропорційний
до його об'єму.
а
незмінної температури та кількості
речовини
тиск
ідеального газу обернено пропорційний
до його об'єму.
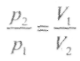
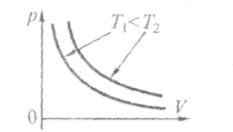
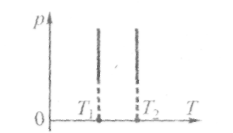
Графіки
ізотермічного процесу в координатах![]() називаютьізотермами.
називаютьізотермами.
• Ізобарний процес — це ізопроцес, при якому тиск ідеального газу не змінюється.
З ОГЗ слідує, що,

або — закон Гей-Люссака.
За незмінного тиску та кількості речовини об'єм ідеального газу прямо пропорційний до його абсолютної температури.
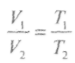
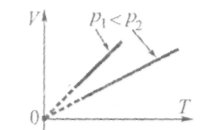


Графіки ізобарного процесу в координатах VT,pV,pT називають ізобарами.
• ізохорний проце — це ізопроцес, при якому об'єм ідеального газу не ізмінюється.
З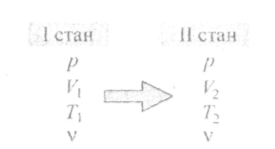 ОГЗ слідує, що, абс
ОГЗ слідує, що, абс![]() —
закон Шарля. За незмінного об'єму та
кількостіречовини тиск ідеального газу
прямо пропорційний до його абсолютної
температури.
—
закон Шарля. За незмінного об'єму та
кількостіречовини тиск ідеального газу
прямо пропорційний до його абсолютної
температури.
![]()
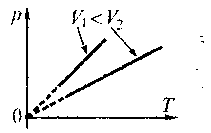
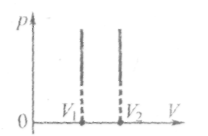

Графіки
ізохорного процесу в координатах
![]() називають
ізохорами.
називають
ізохорами.
Тема 18. Насичена пара. Вологість повітря
Пароутворенням називають перехід речовини з рідкого стану в газоподібний. Існує два види пароутворення — випаровування та кипіння.
Випаровування — це пароутворення з вільної поверхні рідини. Випаровування відбувається за довільної температури. Оскільки під час випаровування рідину залишають найбільш швидкі частинки, то температура рідини, що випаровується, знижується. Швидкість випаровування залежить від роду та температури рідини, площі поверхні та стану повітря над поверхнею рідини (атмосферного тиску, вологості та наявності вітру).
К
 ипіння—
це пароутворення в товщі рідини всередину
бульбашок. Кипіння відбувається за
сталої температури, яку називають
температурою кипіння. Температура
кипіння залежить від роду рідини та
тиску над її поверхнею (див. графік).
ипіння—
це пароутворення в товщі рідини всередину
бульбашок. Кипіння відбувається за
сталої температури, яку називають
температурою кипіння. Температура
кипіння залежить від роду рідини та
тиску над її поверхнею (див. графік).
У рідині містяться мікроскопічні неоднорідності (домішки), які при підвищенні температури стають центрами утворення бульбашок. Розчинені у рідині гази виділяються на них у вигляді бульбашок, в які надалі випаровується рідина. Об'єм бульбашок зростає, під сили Архімеда бульбашки піднімаються на поверхню рідини, де лускають (за умови, що тиск пари всередині бульбашки стає рівним атмосферному).
• Газоподібна речовина існує у вигляді пари або газу.
Пара — це газоподібна речовина, яка за даної температури може бути зріджена шляхом стискання. Газ — це газоподібна речовина, яку не можна зрідити шляхом стискання без попереднього охолоджені температури, яку називають критичною.
• .Якщо в закритій посудині містяться рідина та її пара, то пара буде насиченою тоді, коли процеси пароутворення і конденсації скомпенсовані (стан термодинамічної рівноваги між парою та її рідиною).
При відсутності рідини пара буде насиченою, якщо будь-яке зменшення її об'єму супроводжується утворенням крапель рідини. У стані насичення густина та парціальний тиск насиченої нари за даної температури є максимальними. Залежність густини та тиску насиченої пари від температури подана в таблицях.
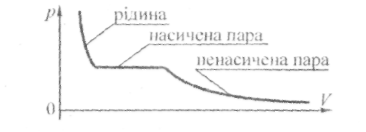
• Властивості насиченої пари.
Тиск насиченої пари залишається сталим при зміні об'єму пари (див. графік).
При збільшенні температури тиск насиченої пари зростає стрімкіше порівняно з ідеальним газом (див. графік
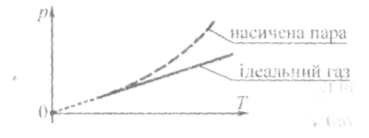
Точка роси — це температура, за якої водяна пара стає насиченою.
Вологістю повітря називають фізичну величину, що характеризує вміст водяної пари в атмосфері. Poзрізняють абсолютну та відносну вологості повітря.
Абсолютна вологість повітря — це густина водяної пари, що міститься у повітрі (парціальний тиск водяної пари).
Відносною вологістю повітря називають відношення густини
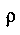 (тиску
(тиску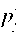 )
водяної пари, що міститься у і вітрі за
даної температури, до густини
)
водяної пари, що міститься у і вітрі за
даної температури, до густини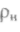 (тиску
(тиску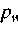 ,)
насиченої водяної пари за цієї ж
температури:
,)
насиченої водяної пари за цієї ж
температури:
![]()
Відносна вологість — безрозмірна величина. Часто її виражають у процентах. Знаючи точку роси, відносну вологість можна обчислювати за формулою
![]()
де![]() — густина та тиск насиченої водяної
пари при точці роси;
— густина та тиск насиченої водяної
пари при точці роси;
![]() —
густина та тиск насичено пари
за
даної температури.
—
густина та тиск насичено пари
за
даної температури.
• Способи підвищення відносної вологості.
І
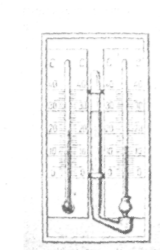 зотермічний
стиск до об'єму, за якого
зотермічний
стиск до об'єму, за якого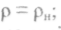
Ізохорне охолодження до температури, за якої з'являється роса;
При сталому об'ємі та температурі додаткове пароутворення певної кількості води.
• Для вимірювання відносної вологості використовують:
а) металевий гігрометр — прилад, за допомогою якого можна виміряти точку роси;
б) психрометр р— прилад, що вимірює відносну вологість за різницею показів сухого та вологого термометрів. Що більша різниця температур сухого та вологого термометрів, то менша відносна вологість повітря.
