
- •Никотинамидные дегидрогеназы. Их строение и роль. Механизм участия над в окислит реакции
- •Что такое окислительное фосфорилирование? Как можно выразить его эффективность?
- •Реакция синтеза лимонной кислоты
- •Роль витамина с в биогенезе коллагена
- •Формула сукцината. Роль
- •Определение метаболизма, анаболизма и катоболизма. Формула атф. Свойства и биологич роль атф
- •Привести по одному примеру окисления субстратов полной и укороченной цепей митох окисл. (реакции)
- •Окислит р-и, катализир-е диоксигеназами (общ вид). Их биол значение.
- •Активные формы кислорода. Их свойства и биол значение.
- •Формула витимина в2. Роль
- •Суммарная реация окислит декарбоксилирования пвк. От каких витаминов зависит протекание данной р-и?
- •Пути использования атф в митохондриях и цитоплазме
- •Перечислить основные неферм компоненты антиоксидантной защиты
- •Биологическая роль монооксигеназного окисления. Р-я обр. Тирозина из фенилаланина
- •Формула над. Биол ф-я
- •Строение флавиновых дегидрогеназ, их роль в биол окисл. Формула фмн. Механизм его участия в окислит. Р-ях. (недостаточно)
- •ННаписать р-ю, катализируемую протеин-лизин-6-оксидазой. Ее роль в биосинтезе коллагена.
- •Дать определение понятию общие метаболиты. Формулв главнейш из них
- •Роль глутатиона в системе антиоксидантной защиты
- •Формула кофермента q, его роль
- •Строение, свойства и функции митох цитохромов. Механизм их участия в окислительных реакциях.
- •Суммарная реакция окислит декарбоксилирования альфа-кетаглутаровой кислоты. От каких витаминов зависит протекание данной реакции?
- •Роль витамина е в ао
- •Окислительные реакции, катализируемые оксидазами (общ вид). Строение и локализация ф. Биол значение оксидазного окисл.
- •Формула атф. Биохимич р-я
- •Общая характеристика цтк. Итоговое уравнение и биохимич значение процесса
- •Написать р-ю, катализируемую протеин-лизин-5-гидроксилазой. Ее роль в биосинтезе коллагена.
- •Формула витамина с. Биох ф-я
- •Убихинон.
- •Способы обр-я атф.
- •Реакция цтк сопряженные с декарбоксилированием
- •Формула пвк. Роль
- •Роль витамина а в митох окисл
- •Реакции Цтк с обр атф
- •Основные ферменты пероксидантной защиты. Реакция катализируемая пероксидазой слюны.
- •Окислительные реакции, катализируемые десатуразами. Строение и локализация, роль.
- •Механизм сопряжения окисления и фосфорилирования. Строение и свойства протон-зависимой атф-синтетазы.
- •2.ЦТк до альфакетогл
- •Роль витамина с в окислит р-ях
- •Формула альфа-кетоглутаровой кислоты. Роль.
- •Окислительное фосфорилирование. Эффективность. Коеф р/о.
- •Написать реакцию субстратного фосфорилирования, протекающую в цтк. Класс фермента
- •Автономная саморегуляция м/о (дыхательный контроль). Энергетический заряд клетки, возможный диапазон его значений.
- •2. Написать реакции цтк от суккцинил-КоА до оксалоацетата.Энерг итог.
- •Окислительные реакции, катализ оксидазами. Строение и роль.
- •4. Активные формы кислорода, их свойства и био знаечние.
- •Формула витамина с, функции.
- •Дать сравнительный анализ способов образования атф в организме человека. Привести примеры реакций, сопряженных с образованием атф.
- •Написать формулы метаболитов цтк, являющихся субстратами м/о.
- •Автономная регуляция цтк
- •Лизил-5гидроксилаза
-
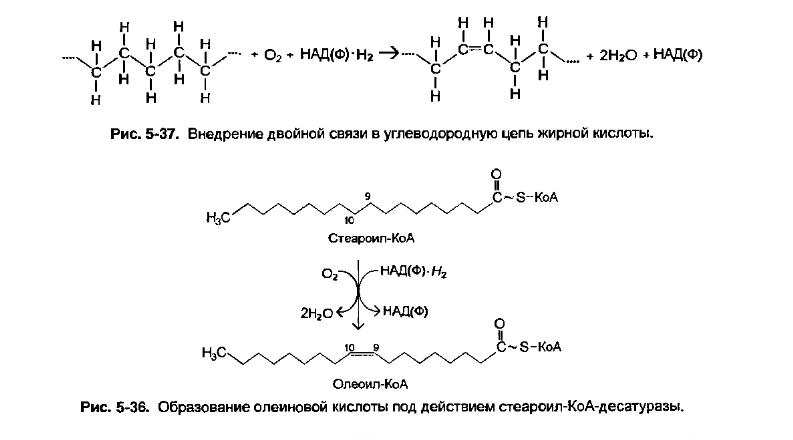
Окислительные реакции, катализируемые десатуразами. Строение и локализация, роль.
Название свое ферменты этой группы получили по способности превращать насыщенные жирные кислоты в ненасыщенные (и далее в полиненасыщенные). Образование двойной связи они обеспечивают путем отнятия двух атомов водорода у соседних углеродных атомов. При этом отнимаемый водород передается прямо на кислород. Но, в отлнчие от оксидаз- ных реакций, здесь происходит не двухэлектронное восстановление молекулы кислорода, а четырехэлектронное. Поэтому образуется не перекись водорода, а две молекулы воды. Недостающую пару электронов (и протонов) де- сатуразы получают от НАД(Ф)-//г- (с учетом того, что формируемая двойная связь имеет, как правило, ^с-конфигурацию).
Полнота восстановления 02 обеспечивается тем, что десатураза (несущая 1 атом неге- мового железа) - это не одиночный белок, а составная часть комплексов, встроенных в мембрану ЭР. В такой комплекс входят также цитохром Ь5 и цитохром(Ь$)-редуктаза, которая содержит ФАД и использует НАД(Ф)Я2 для восстановления железа цитохрома Ъ5_
Важная роль десатураз обусловлена тем, что биосинтез любой жирной кислоты протекает путем поэтапной конденсации двухуглеродных фрагментов (происходящих из ацетил- КоА), приводя к образованию полностью насыщенной углеводородной цепи (с группой -СООН на одном из концов). И только затем возможно внедрение двойных связей, что и осуществляют десатуразы. Жирные кислоты вступают в реакцию только в активированном состоянии, т.е., в форме соединения с коферментом А (ацил-КоА).
В отличие от растений клетки животного организма имеют очень ограниченную способность формировать двойную связь в молекулах жирных кислот. В отношении насыщенных известен только один фермент - стеарош- КоА -десатураза. открытая в печени как интегральный белок мембраны ЭР. Она относится к Д9-десатуразам, ибо внедряет двойную связь в положении 9 (т.е., между 9-м и 10-м атомами углерода, считая от карбоксильной группы). При этом стеариновая кислота С(18):0 превращается в олеиновую С(18):1 (рис. 5-38). Аналогичным образом стеароил-КоА-десатураза действует и на ряд других насыщенных жирных кислот, преобразуя их в моноеновые. В частности, она превращает пальмитиновую кислоту С(16):0 в пальмитолеиновую С(16):1
Полиеновые кислоты должны поступать в организм животных извне. Точнее, из всех жирных кислот незаменимыми компонентами пищн являются линолевая и а-линоленовая (содержащие по 18 углеродных атомов). Как отмечено в табл. 3.1, первая содержит две двойных связи (в позициях 9 и 12), а вторая - три (в положениях 9, 12 и 15). Обе они служат материалом для создания еще более ненасыщенных жирных кислот, которые необходимы для построения липидов биологических мембран и, кроме того, для образования сигнальных молекул из группы эйкозаноидов.
сначала линолевая и а-линоленовая кислоты подвергаются десатурации в положении 6, что превращает их соответственно в триеновую у-линоленовую кислоту и в ее тетраеновый аналог. В обоих случаях процесс катализирует линолеош-КоА-десатураза. По строению, локализации и механизму действия она очень близка стеароил-КоА-десатуразе, но специализирована на внедрении двойной связи в позиции 6 (т.е., является Дб~десатуразой). Образовавшиеся продукты могут подвергаться удлинению специальной системой ЭР, обозначаемой как элонгаза. Как и при биосинтезе насыщенных жирных кнслот, это происходит путем наращивания карбоксильного конца молекулы двухуглеродным фрагментом, происходящим из ацетил-КоА. Такое удлинение отодвигает от группы -СООН (на два номера) положение тех двойных связей, которые уже имелись в молекуле. В итоге С 18-кислоты преобразуются в 20-углеродные (эйкозано- вые), а двойные связи смещаются из положений 6, 9, 12... в позиции 8, 11, 14—, соответственно. Последующая десатурация по 5-му углеродному атому приводит к превращению исходной линолевой кислоты в 5,8,11,14-эйко- затетраеновую (арахидоновую кислоту), а а-линоленовой - в 5,8,11,14,17-эйкозапента- еновую. Пути превращения последних в биологически активные молекулы будут рассмотрены в разделах
-
Витамин В3 PP
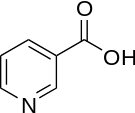
Никотиновая кислота
B5
Ниацин
Участвует в процессах клеточного дыхания (перенос H+ и e–). Регулирует секреторные и мо-торные функции желудочно-кишечного тракта и печени. Вхо-дит в состав НАД и НАДФ.
Мясо, печень, почки, рыба, дрожжи.
Признаки недост: Воспаление кожи (пеллагра), расстройства желудочно-кишечного тракта.
Билет №9
