- •Никотинамидные дегидрогеназы. Их строение и роль. Механизм участия над в окислит реакции
- •Что такое окислительное фосфорилирование? Как можно выразить его эффективность?
- •Реакция синтеза лимонной кислоты
- •Роль витамина с в биогенезе коллагена
- •Формула сукцината. Роль
- •Определение метаболизма, анаболизма и катоболизма. Формула атф. Свойства и биологич роль атф
- •Привести по одному примеру окисления субстратов полной и укороченной цепей митох окисл. (реакции)
- •Окислит р-и, катализир-е диоксигеназами (общ вид). Их биол значение.
- •Активные формы кислорода. Их свойства и биол значение.
- •Формула витимина в2. Роль
- •Суммарная реация окислит декарбоксилирования пвк. От каких витаминов зависит протекание данной р-и?
- •Пути использования атф в митохондриях и цитоплазме
- •Перечислить основные неферм компоненты антиоксидантной защиты
- •Биологическая роль монооксигеназного окисления. Р-я обр. Тирозина из фенилаланина
- •Формула над. Биол ф-я
- •Строение флавиновых дегидрогеназ, их роль в биол окисл. Формула фмн. Механизм его участия в окислит. Р-ях. (недостаточно)
- •ННаписать р-ю, катализируемую протеин-лизин-6-оксидазой. Ее роль в биосинтезе коллагена.
- •Дать определение понятию общие метаболиты. Формулв главнейш из них
- •Роль глутатиона в системе антиоксидантной защиты
- •Формула кофермента q, его роль
- •Строение, свойства и функции митох цитохромов. Механизм их участия в окислительных реакциях.
- •Суммарная реакция окислит декарбоксилирования альфа-кетаглутаровой кислоты. От каких витаминов зависит протекание данной реакции?
- •Роль витамина е в ао
- •Окислительные реакции, катализируемые оксидазами (общ вид). Строение и локализация ф. Биол значение оксидазного окисл.
- •Формула атф. Биохимич р-я
- •Общая характеристика цтк. Итоговое уравнение и биохимич значение процесса
- •Написать р-ю, катализируемую протеин-лизин-5-гидроксилазой. Ее роль в биосинтезе коллагена.
- •Формула витамина с. Биох ф-я
- •Убихинон.
- •Способы обр-я атф.
- •Реакция цтк сопряженные с декарбоксилированием
- •Формула пвк. Роль
- •Роль витамина а в митох окисл
- •Реакции Цтк с обр атф
- •Основные ферменты пероксидантной защиты. Реакция катализируемая пероксидазой слюны.
- •Окислительные реакции, катализируемые десатуразами. Строение и локализация, роль.
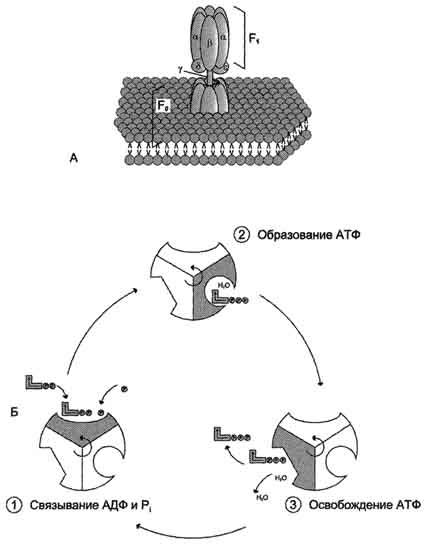
- •Механизм сопряжения окисления и фосфорилирования. Строение и свойства протон-зависимой атф-синтетазы.
- •2.ЦТк до альфакетогл
- •Роль витамина с в окислит р-ях
- •Формула альфа-кетоглутаровой кислоты. Роль.
- •Окислительное фосфорилирование. Эффективность. Коеф р/о.
- •Написать реакцию субстратного фосфорилирования, протекающую в цтк. Класс фермента
- •Автономная саморегуляция м/о (дыхательный контроль). Энергетический заряд клетки, возможный диапазон его значений.
- •2. Написать реакции цтк от суккцинил-КоА до оксалоацетата.Энерг итог.
- •Окислительные реакции, катализ оксидазами. Строение и роль.
- •4. Активные формы кислорода, их свойства и био знаечние.
- •Формула витамина с, функции.
- •Дать сравнительный анализ способов образования атф в организме человека. Привести примеры реакций, сопряженных с образованием атф.
- •Написать формулы метаболитов цтк, являющихся субстратами м/о.
- •Автономная регуляция цтк
- •Лизил-5гидроксилаза
-
Механизм сопряжения окисления и фосфорилирования. Строение и свойства протон-зависимой атф-синтетазы.
Каким же образом осуществляется сопряжение этих двух процессов? Наиболее обоснованный ответ на этот вопрос даёт хемиосмотическая теория Митчелла, предложенная им в 1961 г. Основные положения были подтверждены и разработаны детально совместными усилиями многих исследователей в последующие годы.
1. Протонный градиент и электрохимический потенциал
Перенос электронов по дыхательной цепи от NADH к кислороду сопровождается выкачиванием протонов из матрикса митохондрий через внутреннюю мембрану в межмембранное пространство. На эту работу затрачивается часть энергии электронов, переносимых по ЦПЭ.
Протоны, перенесённые из матрикса в межмембранное пространство, не могут вернуться обратно в матрикс, так как внутренняя мембрана непроницаема для протонов. Таким образом, создаётся протонный градиент, при котором концентрация протонов в межмембранном пространстве больше, а рН меньше, чем в матриксе. Кроме того, каждый протон несёт положительный заряд, и вследствие этого появляется разность потенциалов по обе стороны мембраны: отрицательный заряд на внутренней стороне и положительный - на внешней. В совокупности электрический и концентрационный градиенты составляют электрохимический потенциал ΔμН+ - источник энергии для синтеза АТФ. Так как наиболее активный транспорт протонов в межмембранное пространство, необходимый для образования ΔμН+, происходит на участках ЦПЭ, соответствующих расположению комплексов I, III и IV, эти участки называют пунктами сопряжения дыхания и фосфорилирования (рис. 6-11, 6-13).
Механизм транспорта протонов через мито-хондриальную мембрану в пунктах сопряжения недостаточно ясен. Однако установлено, что важную роль в этом процессе играет KoQ. Наиболее детально механизм переноса протонов при участии KoQ изучен на уровне комплекса III (рис. 6-14).
KoQ переносит электроны от комплекса I к комплексу III и протоны из матрикса в межмембранное пространство, совершая своеобразные циклические превращения, называемые Q-циклами. Донором электронов для комплекса III служит восстановленный убихинон (QH2), а акцептором - цитохром с. Цитохром с находится с внешней стороны внутренней мембраны митохондрий; там же располагается активный центр цитохрома с1 с которого электроны переносятся на цитохром с.
мембране существует стационарный общий фонд Q/QH2, из которого каждая молекула QH2 в одном цикле обеспечивает перенос протонов из матрикса в межмембранное пространство и электронов, которые в конечном итоге поступают на кислород. На работу, совершаемую при выкачивании протонов, расходуется часть свободной энергии, которая освобождается при переносе электронов по градиенту редокс-потенциала. Энергия электрохимического потенциала (∆μH+) используется для синтеза АТФ, если протоны возвращаются в матрикс через ионные каналы АТФ-синтазы.
2. Строение АТФ-синтазы и синтез АТФ
АТФ-синтаза (Н+-АТФ-аза) - интегральный белок внутренней мембраны митохондрий. Он расположен в непосредственной близости к дыхательной цепи. АТФ-синтаза состоит из 2 белковых комплексов, обозначаемых как F0 и F1 (рис. 6-15).
Гидрофобный комплекс F0 погружён в мембрану. Он служит основанием, которое фиксирует АТФ-синтазу в мембране. Комплекс F0 состоит из нескольких субъединиц, образующих канал, по которому протоны переносятся в матрикс.
Комплекс F1 выступает в митоховдриальный матрикс. Он состоит из 9 субъединиц (Зα, 3β, γ, ε, δ). Субъединицы аир уложены попарно, образуя "головку"; между α- и β-субъединицами располагаются 3 активных центра, в которых происходит синтез АТФ; γ-, ε-, δ- субъединицы связывают комплекс F1 с F0.
Повышение концентрации протонов в межмембранном пространстве активирует АТФ-синтазу. Электрохимический потенциал ΔμH+ заставляет протоны двигаться по каналу АТФ-синтазы в матрикс. Параллельно под действием ΔμH+ происходят конформационные изменения в парах α, β-субъединиц белка F1, в результате чего из АДФ и неорганического фосфата образуется АТФ. Электрохимический потенциал, генерируемый в каждом из 3 пунктов сопряжения в ЦПЭ, используют для синтеза одной молекулы АТФ.
3.Коэффициент окислительного
фосфорилирования
Окисление молекулы NADH в ЦПЭ сопровождается образованием 3 молекул АТФ; электроны от FAD-зависимых дегидрогеназ поступают в ЦПЭ на KoQ, минуя первый пункт сопряжения. Поэтому образуются только 2 молекулы АТФ. Отношение количества фосфорной кислоты (Р), использованной на фосфорилирование АДФ, к атому кислорода (О), поглощённого в процессе дыхания, называют коэффициентом окислительного фосфорилирования и обозначают Р/О. Следовательно, для NADH Р/О = 3, для сукцината Р/О - 2. Эти величины отражают теоретический максимум синтеза АТФ, фактически эта величина меньше.
4.Дыхательный контроль
Окисление субстратов и фосфорилирование АДФ в митохондриях прочно сопряжены. Скорость использования АТФ регулирует скорость потока электронов в ЦПЭ. Если АТФ не используется и его концентрация в клетках возрастает, то прекращается и поток электронов к кислороду. С другой стороны, расход АТФ и превращение его в АДФ увеличивает окисление субстратов и поглощение кислорода. Зависимость интенсивности дыхания митохондрий от концентрации АДФ называют дыхательным контролем. Механизм дыхательного контроля характеризуется высокой точностью и имеет важное значение, так как в результате его действия скорость синтеза АТФ соответствует потребностям клетки в энергии. Запасов АТФ в клетке не существует. Относительные концентрации АТФ/АДФ в тканях изменяются в узких пределах, в то время как потребление энергии клеткой, т.е. частота оборотов цикла АТФ и АДФ, может меняться в десятки раз.
Общее содержание АТФ в организме 30-50 г, но каждая молекула АТФ в клетке "живёт" меньше минуты. В сутки у человека синтезируется 40-60 кг АТФ и столько же распадается. Увеличение концентрации АДФ немедленно приводит к ускорению дыхания и фосфорилирования.