
- •1. Термодинамика. Химическая термодинамика. Основные понятия. Термодинамическая система. Фаза. Классификация термодинамических процессов.
- •2. Системы гомогенные и гетерогенные. Основные параметры системы:
- •3. Понятие термодинамической функции. Внутренняя энергия, полная энергия системы. Устойчивость состояния системы.
- •4. Теплота, работа. 1-й закон термодинамики.
- •6. Энтропия, ее определение. Определение Клаузиуса и Планка. Второй закон термодинамики.
- •7. Классификация химических процессов. 1) по знаку; 2) по условиям протекания; 3) по самопроизвольности.
- •9. Энтропия образования вещества в результате химической реакции.Стандартная энтропия образования вещества (s ).Закономерности изменения энтропии.
- •10. Термодинамическое равновесие. Самопроизвольные процессы.
- •12. Влияние отдельных факторов на изменение энергии Гиббса.
- •16. Закон Гесса. Следствия из закона Гесса.
- •17. Обратимые и необратимые реакции. Состояние равновесия.Истинное равновесие. Стационарное и кажущееся равновесие. Константа равновесия.
- •18. Теория активации химических реакций.Механизм сложной химической реакции.
- •19. Закон Лавуазье-Лапласа.Закономерности изменения энтропии.
- •20. Виды химических реакций. Факторы, определяющие процесс реакции.
- •21. Химические реакции в твердой фазе.Способы инициирования реакций
- •22. Способы инициирования реакций Механохимия. Трибохимия
- •24. Виды диффузионных процессов в твердом теле.
- •25. Избыточная энтальпия.
- •26. Третий закон термодинамики.
- •27. Растворы. Дисперсии. Истинные растворы.
- •28. Идеальные растворы. Закон Рауля и отклонения от него.
- •29. Закон действующих масс. Закон разбавления Оствальда
- •30. Термодинамика процесса растворения. Физическая и Химическая сторона процесса растворения. Теплота растворения.
- •31. Энтропия растворения.Энергия Гиббса.
- •32. Уравнение Нернста
- •34. Методы идентификации продуктов реакции
- •2. Структурный анализ
21. Химические реакции в твердой фазе.Способы инициирования реакций
Немногим более сорока лет назад химики, так же как металлурги и металловеды, считали невозможным выяснение механизма химической реакции, решающие стадии которой протекают внутри твердого тела или на его поверхности.К таким реакциям относятся, например, окисление металлов и сплавов, восстановление руд, выделение новой фазы и закалка металлических сплавов, а также процессы, лежащие в основе приготовления керамики. В то время во многих случаях отсутствовали как необходимые термодинамические, так кинетические данные, например данные о коэффициентах диффузии собственных элементов решетки и посторонних атомов и ионов; не существовало и удовлетворительных рабочих гипотез для объяснения реакций в твердой фазе и процессов, связанных с «обменом местами» в твердых телах. Не удивительно поэтому, что практически все работы того времени, касающиеся реакционной способности твердых тел, были чисто эмпирическими, поэтому из них нельзя было вывести достаточно глубоких закономерностей механизма реакций.
В большей своей части реакционная способность твердых тел значительно ниже реакционной способности жидкостей и газов, однако нередко, предполагают, она все же выше. В отдельных случаях, например при реакции твердых меди и серебра с серой и селеном, реакционная способность оказывается даже величиной того же порядка, что и в жидких реагирующих :телах. Но зато есть реакции, которые даже при температурах 10000С протекают настолько медленно, что приходится вести опыты днями, неделями, чтобы получить измеримые результаты.
Химические реакции в твердой фазе, классификация по типу химических превращений: разложение, обмен, восстановление, окисление, присоединение, изомеризация, димеризация, полимеризация. Классификация такая же как и в случае реакций в газообразной и жидкой средах.
Химические реакции в твердой фазе классификация по агрегатному состоянию реагентов и/или продуктов:
твердое тело твердое тело,
твердое тело твердое тело + газ,
твердое тело + твердое тело твердое тело,
твердое тело + газ твердое тело,

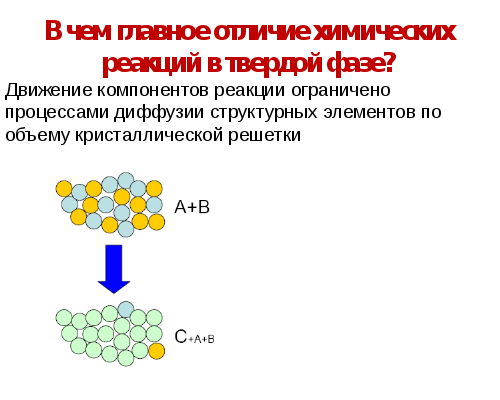
Типичная особенность твердофазных реакций - протекание на границе раздела фаз, то есть на поверхности твердых частиц. Скорость твердофазных реакций зависит от многих факторов: температуры, структуры и дефектности кристалла, гомогенности реакционной смеси. Применительно к задачам синтеза веществ наибольший интерес вызывают реакции, ведущие к образованию одного продукта, в противном случае возникает проблема разделения твердых продуктов синтеза.
22. Способы инициирования реакций Механохимия. Трибохимия
Механохимия.Трибохимия.
Многие процессы металлургии, переработки минерального сырья и получения строительных материалов, химического синтеза широкого круга материалов, предполагают использование твердого вещества в измельченном состоянии. В связи с этим актуально изучение физико-химических закономерностей протекания химических реакций в твердой фазе, измельчения и механической активации, исследование процесса накопления избыточной энергии неорганическими дисперсными веществами в мельницах.
Для интенсификации химических процессов с участием твердых веществ очень часто используется их механическая обработка. Поскольку эту операцию проводят, применяя аппаратуру, обычно предназначенную для измельчения, то и химические последствия предварительной механической обработки обычно связывают с измельчением и диспергированием твердых веществ, то есть с тривиальным изменением соотношения между поверхностью кристалла и его объемом. Однако опыт показал, что во многих случаях это не так, и что из общего количества энергии, запасаемой твердым телом и увеличивающей его реакционную способность, с увеличением поверхности связано всего несколько процентов. Остальное же приходится на накопление в кристаллах дефектов.
Если мы хотим создать дефекты в кристалле механическим воздействием, то аппаратом, в котором будет проводиться механическая активация, должна быть не "обычная" мельница, а специальная машина, "активатор", которая позволяла бы изменять количество и скорость подведения к твердому веществу энергии, а также характер механического воздействия, определяемого соотношением между давлением и сдвигом, чтобы получить именно те дефекты, к которым данная реакция в наибольшей степени чувствительна.

