
- •Учебно-методические материалы для лабораторных занятий по курсу «Технология изготовления современных ис, мэмс и нэмс»
- •Критерии применимости фоторезистов
- •Лабораторная работа № 2 «Термическое окисление кремния»
- •Механизм роста и кинетика окисления
- •Факторы, влияющие на скорость термического окисления
- •Определение толщины оксидного слоя
- •Структура и дефекты оксидной пленки
- •Методы осуществления диффузии
- •Лабораторное задание
- •Порядок выполнения работы
- •Требования к отчету
- •Контрольные вопросы
- •Лабораторная работа 4 «Изучение процесса плазмохимического травления»
- •Совмещение
- •Лабораторное задание
- •1. Изучение подложек гис
- •2. Изучение конструкций гис
Определение толщины оксидного слоя
Определение толщины пленки является важной технологической операцией при изготовлении полупроводниковых интегральных схем, так как от толщины слоя оксида зависят его маскирующая способность, диэлектрические свойства, а также целый ряд электрических характеристик изготавливаемых интегральных схем. Для измерения толщины оксидных пленок может быть использовано несколько методов, основные из которых:
методы двухлучевой и многолучевой интерференции;
метод цветовых оттенков;
метод шарового шлифа;
метод конденсатора;
эллипсометрия.
Кроме перечисленных методов, существуют и другие, например метод микробалансового взвешивания, расчетный и фотометрический методы. Однако они в практике производства ИС почти не применяются. Наиболее широкое применение получил метод цветовых оттенков. Главное достоинство метода - быстрота определения толщины оксидного слоя. Метод основан на наблюдении интерференционных цветов в отраженном свете, возникновение которых обусловлено двойным отражением и преломлением белого света, проходящего через прозрачную пленку и отражающегося от непрозрачной подложки. Цветность пленок зависит только от их толщины х и показателя преломления п:
∆= 2 n x sinα,
где ∆- разность хода лучей; α - угол отражения.
Для определения толщины пленки оксида составлена таблица цветов. Так как цвета повторяются, необходимо знать порядок цвета. Для этого на пластине-спутнике стравливают часть оксида на клин. Таким образом, становится видна вся серия цветовых оттенков, причем зеленые полосы служат для отметки порядка цвета. Относительная ошибка при этом методе в большинстве случаев составляет меньше 5 % от исходной толщины, однако точность определения цвета сильно зависит от индивидуальных особенностей наблюдателя.
Структура и дефекты оксидной пленки
Диоксид кремния, термически выращенный на поверхности полупроводника, в большинстве своем либо аморфен, либо имеет структуру стекла. Стекло обладает упорядоченной структурой в пределах некоторых областей зерен, т.е. соблюдается ближний порядок и нарушается лишь дальний. Кварцевое стекло построено не из молекул SiO2 , а из атомов кремния, связанных через атомы или ионы кислорода таким образом, что они образуют сетчатую структуру. В такой структуре кислород, окружающий кремний, расположен в виде тетраэдра. Однако в стекле тетраэдры ориентированы не закономерно, как в кристаллических модификациях, а совершенно беспорядочно.
В оксиде имеется множество разнообразных электрически заряженных дефектов, оказывающих значительное отрицательное влияние. Можно выделить несколько видов таких дефектов. Первый вид - это примесные (положительные) ионы металлов, второй - это центры заряда (в большинстве случаев положительные), основанные не микроструктурных дефектах в окрестности границы Si – SiО2. К дефектам атомного размера можно отнести: кислородные вакансии и другие анионы в междоузлиях решетки. Преобладающую роль по сравнению с дефектами атомного размера играют более крупные дефекты структуры: поры границы кристаллов и микроканалы. Основные причины их возникновения: структурные нарушения подложки, загрязнение поверхности полупроводника, механические напряжения на границе раздела и т.д.
Дефекты атомного размера приводят к возникновению в слое оксида объемного положительного заряда, обусловливают его нестабильность, влияют на процессы проводимости через слой диэлектрика. Макродефекты структуры могут приводить к нарушению маскирующих свойств оксида при диффузии, возникновению электрических закороток между металлизированной разводкой и полупроводниковой подложкой, нарушению защитных функций оксида от воздействия окружающей среды и т.д.
Для определения плотности макродефектов в слое оксида разработан ряд методов.
Метод хлорного травления сводится к обработке окисленного кремния в парах хлора при температуре около 900 °С в течение 3-5 мин. Проникая сквозь мельчайшие поры в оксиде, хлор растравливает поверхность кремния; плотность полученных ямок подсчитывается с помощью микроскопа.
При электрохимическом контроле на пластину кремния наносят капля электролита, например воду. На пластину подают отрицательный относительно электролита потенциал, происходит диссоциация воды (НгОН+ +0Н-), при этом наблюдают выделение пузырьков водорода в местах дефектов оксида.
Электрографический метод контроля заключается в том, что пластину кремния с оксидом зажимают между двумя электродами, к которым подается смещение. Между диэлектрическим слоем и положительным электродом помещают фотобумагу, смоченную водой, и пропускают ток в течение 3 - 60 с. В результате водород, выделяющийся в месте дефекта, восстанавливает бромистое серебро до металла, на фотобумаге запечатлеваются четкие увеличенные изображения проводящих дефектов. Метод электрографии позволяет выявлять дефекты размером 0,1 - 0,3 мкм.
Лабораторное задание
Определить время процесса линейного роста оксида при окислении в сухом кислороде и парах воды для данной температуры.
Оценить толщину оксида, соответствующую линейному участку роста оксида при окислении в сухом кислороде и парах воды.
Рассчитать и построить зависимость х(t) для параболического участка роста оксида при окислении в сухом кислороде и парах воды.
Определить константы параболического роста В для окисления в сухом кислороде и парах воды.
Провести процесс окисления в сухом кислороде. Построить зависимость x(t) . Определить экспериментально величину В.
Провести процесс окисления во влажном кислороде. Построить зависимость константы параболического роста В от парциального давления воды.
Определить плотность макродефектов N электрохимическим и электрографическим методами.
Порядок выполнения работы
1. Определить
время процесса линейного роста оксида
из условия (9);
Определить
время процесса линейного роста оксида
из условия (9);
2. Оценить толщину оксида, соответствующую линейному участку роста из соотношения (10).
Построить теоретическую зависимость толщины оксида от времени термического окисления x(t) для сухого кислорода и паров воды, пользуясь эмпирическими соотношениями (13) и (14).
После проведения эксперимента построить экспериментальный и теоретический графики x(t). Сравнить теоретические и экспериментальные зависимости.
Провести окисление в сухом кислороде. Для этого:
включить подачу кислорода и продуть трубу в течение 5-10 мин. Расход 100 л/ч;
пинцетом загрузить пластины в кварцевую лодочку;
поставить лодочку с пластинами в начало печи и с помощью кварцевого крючка продвинуть в рабочую зону;
выдержать пластины в рабочей зоне печи 30 мин;
- медленно выдвинуть лодочку с пластинами из рабочей зоны к краю трубы и дать остыть в течение 5-10 мин;
- взять пинцетом одну пластину и положить на кварцевую подставку. Дать ей остыть в течение 5 - 10 мин;
повторить указанные операции для всех пластин;
определить толщину слоя оксида на всех пластинах цветовым методом;
построить зависимость x(t);
определить экспериментальную величину В.
5. Провести окисление во влажном кислороде. Для этого:
включить электроплитку и довести температуру води в водяной бане до 40 °С;
включить подачу кислорода через барботер и продуть трубу в течение 5-10 мин;
пинцетом загрузить одну пластину в кварцевую лодочку;
поставить лодочку с пластиной в начало печи и с помощью кварцевого крюка продвинуть в рабочую зону;
выдержать пластину в рабочей зоне печи 15 мин;
медленно выдвинуть лодочку с пластиной из рабочей зоны к краю трубы и дать остыть (5 - 10 мин);
взять пинцетом пластину и положить на кварцевую подставку;
выключить подачу кислорода;
изменить положение задатчика контактного термометра, довести температуру воды в водяной бане до температуры 60 °С;
повторить указанные операции для второй пластины;
изменив положение задатчика контактного термометра, довести температуру воды в водяной бане до 80 °С;
повторить указанные операции для третьей пластины;
довести температуру воды в водяной бане до 95 °С;
-повторить указанные операции для четвертой пластины.
Определить толщину слоя оксида для всех пластин цветовым методом.
Построить зависимость константы параболического роста В oт парциального давления паров вода.
При построении графика пользоваться табл. 1.
Таблица 1 - Зависимость давления водяного пара от температуры
|
Температура, °С |
0 |
5 |
10 |
15 |
20 |
25 |
30 |
35 |
|
Давление, Па |
6,1.102 |
8,7.102 |
1,2.102 |
1,7.103 |
2,3.103 |
3,2.103 |
4,2.103 |
5,6.103 |
|
Температура, °С |
40 |
45 |
60 |
65 |
80 |
85 |
100 |
105
|
|
Давление, Па |
7,4.103 |
12,1.103 |
19,8.103 |
30.103 |
47.103 |
70.103 |
100.103 |
142.103 |
Требования к отчету
Отчет должен содержать:
цель работы;
краткие сведения из теории;
исходные уравнения, режимы процесса окисления и результаты расходов (tхар, xхар, x(t)) для сухого кислорода и паров воды;
экспериментальные результаты в виде таблиц и графиков: x(t) для сухого кислорода, B(Р) для влажного кислорода; значения N для сухого и влажного кислорода;
выводы.
Контрольные вопросы
Назначение оксидных слоев SiO2, в планарной технологии.
Методы получения слоев SiO2.
Рост оксида в атмосфере сухого кислорода.
Рост оксида в атмосфере водяного пара.
Кинетика процесса окисления.
Условия получения линейной зависимости x(t).
Условия получения параболической зависимости x(t).
Практические методы термического окисления.
Влияние давления пара, ориентации подложки и концентрации примеси в подложке на скорость роста оксида кремния.
Методы определения толщины оксида.
Структура оксидной пленки на кремнии.
Макродефекты и метода определения их плотности в слое на кремнии.
Рекомендуемая литература
1. Королев М.А., Ревелева М.А. Технологии и конструкции интегральных микросхем. Ч.1 М. МИЭТ. 2000. 120 с.
2. Зи С. Технология СБИС М. Мир. 1986. 404 с.
3. Готра З.Ю. Технология микроэлектронных устройств: Справочник / М.: Радио и связь. 1991. – 528 с.
Лабораторная работа № 3 «Изучение процесса термической диффузии примесей в кремний»
Цель работы: I) ознакомиться о методами проведения диффузионных процессов и контролем легированных слоев в производстве полупроводниковых интегральных схем; 2) освоить инженерные методы выбора технологических режимов процесса диффузии.
Теоретические сведения
Диффузией называется направленное движение атомов, возникающее под действием градиента концентрации или температуры. В объеме монокристаллического твердого тела при высоких температурах повышается концентрация точечных дефектов таких, как вакансии и межузельные атомы. Механизм диффузии, когда атом примеси или собственный атом кристалла мигрирует на место вакансии, называется вакансионным. Если легирующий атом является собственным атомом, то процесс диффузии называется самодиффузией, а если примесным - примесной диффузией, или гетеродиффузией. Энергия связи для примесного атома в решетке кристалла всегда меньше, чем для собственных атомов, поэтому образование вакансий около примесных атомов облегчается, вследствие чего диффузия часто происходит в виде движения комплекса атом примеси - вакансия.
Кроме вакансионного механизма диффузии примеси в полупроводнике существует возможность перемещения атомов по междоузлиям. Реализация этого механизма наиболее вероятна в случае диффузии атомов малых размеров. Поскольку им приходится преодолевать меньшие потенциальные барьеры, то диффузия этих элементов происходит с большей скоростью. Установлено, что в кремнии диффузия элементов III и V групп периодической системы происходит в основном по вакансионному механизму, а элементы I и VIII групп относятся к быстро диффундирующим примесям.
При низкой концентрации примесей (более 1019 см-3) и низкой плотности дислокаций процесс диффузии может быть описан феноменологической теорией диффузии с использованием закона диффузии Фика с постоянным значением коэффициента диффузии.
Первый закон Фика предполагает, что локальная скорость переноса растворенного вещества (локальная скорость диффузии) через сечение единичной площади за единицу времени пропорциональна градиенту концентрации растворенного веществе, а в качестве коэффициента пропорциональности выступает коэффициент диффузии растворенного вещества (примеси). При одномерном направлении потока уравнение Фика имеет вид
 (1)
(1)
где F - поток атомов, представляющий собой векторную величину, численно равную количеству вещества, пересекающего в единицу времени единичную площадку, перпендикулярную вектору потока, г/(см2с); N - концентрация растворенного вещества, зависящая от х и t , см-3; х - ось координат, совпадающая с направлением потока вещества, см; t - время, с; D - коэффициент диффузии вещества, см2/с.
Знак "минус" в правой части уравнения (1) означает, что процесс переноса вещества происходит в направлении уменьшения концентрации растворенного вещества. Из закона сохранения вещества следует, что изменение концентрации растворимого вещества со временем должно быть равно уменьшению диффузионного потока в том же объеме, где произошло изменение концентрации, то есть
 (2)
(2)
Подстановка уравнения (1) в уравнение (2) приводит ко второму закону Фика для одномерного случая:
 (3)
(3)
Коэффициент диффузии D зависит от температуры, энергии связи примесных атомов в решетке, концентрации вакансий в кристалле, постоянной кристаллической решетки, частот колебаний атомов решетки и некоторых других величин. С ростом температуры в твердых телах коэффициент диффузии резко возрастает, изменяясь по экспоненциальному закону:
 ,
,
где D0 - постоянная, численно равная коэффициенту диффузии при бесконечно большой температуре; ∆E - энергия активации диффузии.

Рис.1. Зависимости коэффициентов диффузии примесей в кремнии от температуры.
На рис.1 приведены графики температурной зависимости коэффициентов диффузии в кремнии некоторых элементов. Энергия активации процесса диффузии большинства элементов в кремнии составляет 3,5 - 4,3 эВ. Уравнение (3) часто называют простым диффузионным уравнением Фика. Решение этого уравнения при различных начальных и граничных условиях позволяет определить распределение примеси для конкретных случаев диффузии. Практический интерес представляют следующие случаи диффузии: в полубесконечное тело (так как обычно глубина диффузии невелика по сравнению с толщиной полупроводниковой пластины) из бесконечного (постоянного) источника и из конечного (ограниченного) источника примеси.
Диффузия из бесконечного источника предполагает, что примесь непрерывно поступает через поверхность кристалла (х = 0) из внешнего источника с целью введения в полупроводник точно контролируемого количества примеси Q и поток ее все время одинаков.
Начальные условия при t = 0 для этого случая можно записать так:

Граничные условия можно представить в виде

То есть считается, что до начала процесса в объеме кристалла примесь отсутствует, а во время процесса на поверхности x = 0 концентрация примеси в любой, момент времени постоянная и равна No. Тогда решение уравнения (3), которое удовлетворяет условиям (4) и (5), можно записать как
 (6)
(6)
где NQ - поверхностная концентрация; t - длительность диффузионного процесса, c; х - расстояние по оси координат с учетом, что х = 0 находится на поверхности кремниевой подложки, см; erfc - дополнительная функция ошибок ( erfc y = 1- erfy;
 - функция
ошибок Гаусса).
- функция
ошибок Гаусса).
Из (6) видно, что при t ∞ распределение примеси в полупроводнике стремится к постоянной величине, то есть

На рис.2 показано распределение примеси при различных временах диффузии из бесконечного источника.

Рис. 2. Распределение примеси при различных временах диффузии из бесконечного источника (загонка).
В выражение (6)
входит величина
 ,
имеющая размерность длины. Ее называют
длиной диффузии. При постоянной
поверхностной концентрации величина
,
имеющая размерность длины. Ее называют
длиной диффузии. При постоянной
поверхностной концентрации величина определяет количество примесиQ.
, введенное
в полупроводник за все время диффузии
через площадку в I
см2.
Из первого закона Фика (1) следует, что
определяет количество примесиQ.
, введенное
в полупроводник за все время диффузии
через площадку в I
см2.
Из первого закона Фика (1) следует, что
 (7)
(7)
На стадии загонки величину No, как правило, выбирают равной максимально допустимой, т.е. предельной растворимости примеси при выбранной температуре диффузии. В этом случае поверхностная концентрация не зависит от времени процесса диффузии, что дает возможность получения диффузионных параметров с допустимыми значениями разбросов (порядка 50 %). Зависимость предельных растворимостей основных легирующих примесей в кремнии от температуры приведена на рис.З.

Рис.З. Зависимость растворимостей примесей в кремнии от температуры.
Диффузию из ограниченного источника на практике часто называют разгонкой примеси, целью которой является получение заданного распределения примеси. Сформированный на стадии загонки высоколегированный поверхностный слой полупроводника служит источником примеси с количеством ее Q , определенным выражением (7). Причем приток примеси извне и испарение ее в окружающее пространство отсутствуют, т.е. отсутствует поток примеси через поверхность (x = 0). Поэтому граничное условие можно записать как
 (8)
(8)
Будем считать, что все количество примеси, введенное на этапе загонки, сосредоточено в приповерхностном слое толщиной h, а распределение примеси N(x,t) в этом слое равномерное, т.е. площадь, ограниченная прямоугольником на рис. 4, должна быть равна площади кривой, описываемой выражением (6),при данных N0, x и t.

Рис.4. Графическое изображение граничного условия для случая диффузии из ограниченного источника.
Тогда полное количество примеси, введенное в полупроводник, будет равно
Q=N0h ,
а начальные условия для решения уравнения (3) могут быть записаны в этом случае как,
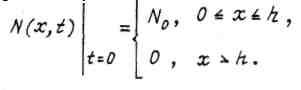 (9)
(9)
Решение уравнения (3) с учетом условий (8) и (9) имеет вид
 (10)
(10)
Если толщина h
мала по сравнению с длиной диффузии
примесных атомов
 ,
то может выполняться условие х<Dt/h
, тогда t>h2/D.
В этом случае уравнение (10) приводится
к виду
,
то может выполняться условие х<Dt/h
, тогда t>h2/D.
В этом случае уравнение (10) приводится
к виду
 (II)
(II)
Выражение (II) представляет собой распределение Гаусса по х.
Поверхностная концентрация примеси Ns (t) в момент времени t определяется выражением
 (12)
(12)
т.е. с течением времени она уменьшается. Распределение примеси для различных значений времени разгонки изображено на рис.5. Обычно этап разгонки проводят в окислительной среде. Это делается по нескольким причинам. Образующаяся оксидная пленка предохраняет введенную примесь от испарения. При проведении разгонки в инертной атмосфере на поверхности кремния возникают эрозионные ямки, которые могут пересекать неглубокие диффузионные слои и шунтировать р-п переход. Кроме того, проведение разгонки в окислительной среде сокращает общее 'гасло высокотемпературных операций в технологическом процессе, так как одновременно с разгонкой создается маскирующий слой оксида для последующих операций диффузии.

Рис.5. Распределение примеси при различных временах диффузии из ограниченного источника (разгонка).
Выражение (2) для распределения примеси при диффузии из ограниченного источника было получено при допущении, что величина Q остается постоянной. Однако оно часто не выполняется, так как в процессе термического окисления происходит перераспределение примеси между оксидной пленкой и полупроводником. Растущая в глубь кремния оксидная пленка перераспределяет примесные атомы в соответствии с величиной коэффициента сегрегации примеси m на поверхности раздела оксид - кремний.
m = Равновесная концентрация примеси в кремнии / Равновесная концентрация примеси в диоксиде кремния,
Если т
 1,это означает,
что оксид оттесняет примесь и увеличивает
ее концентрацию в кремнии вблизи
поверхности раздела оксид - кремний.
Если
m<1,
происходит поглощение примеси оксидной
пленкой и соответственно обеднение
примесью приповерхностных слоев
полупроводника.
1,это означает,
что оксид оттесняет примесь и увеличивает
ее концентрацию в кремнии вблизи
поверхности раздела оксид - кремний.
Если
m<1,
происходит поглощение примеси оксидной
пленкой и соответственно обеднение
примесью приповерхностных слоев
полупроводника.
Для основных примесей в кремнии т имеет следующие значения: для бора - 0,3; для фосфора, мышьяка, сурьмы - 10.
Перераспределение примеси на границе раздела оксид - кремний зависит также от отношения коэффициента диффузии примеси в кремнии к коэффициенту диффузии той же примеси в диоксиде кремния.
При расчете режима диффузии исходными являются параметры диффузионных областей: концентрация примесей на поверхности Ns, глубина залегания p-п. перехода Xj , а также функция распределения исходной примеси в подложке Nп . Поясним это на примере, когда в равномерно легированную подложку p-типа с помощью диффузии вводится акцепторная примесь.

Рис.6. Распределение концентрации примесей в р-п переходе.
Поверхностная концентрация акцепторов NsА должна значительно превышать концентрацию донорных примесей N.dn в исходном материале. При этих условиях акцепторная примесь, диффундируя в глубь проводника, перекомпенсирует донорную примесь и создает полупроводник дырочного типа проводимости от поверхности пластины до некоторой глубины xj (рис.6). Глубина залегания р-п. перехода xj ; определяется условием
![]() (13)
(13)
Можно показать согласно (II), что
 (14)
(14)
где Nxj - концентрация примеси на расстоянии xj от поверхности.
В данном частном случае согласно (13) Nxj численно равна Ndп.
