
ОСНОВЫ ОРГАНИЧЕСКОЙ ХИМИИ ФАРМАЦИЯ
.pdf
Монозы существуют в двух формах – линейной (или оксоформе) и циклической, для описания их строения используют проекции Фишера (для линейной формы) и проекции Хеуорса (для циклической формы).
Линейные формы моноз
Описывают D и L – ряды моноз. Принадлежность к ряду определяют, сравнивая конфигурации последнего хирального центра в нижней части монозы с конфигурацией D- и L – глицериновых альдегидов.
|
C |
O |
|
C |
O |
|
H |
|
H |
||
|
|
|
|
||
H |
|
OH |
HO |
|
H |
|
CH2OH |
|
CH2OH |
||
D-глицериновый |
L-глицериновый |
||||
альдегид |
|
альдегид |
|
||
Линейные формы альдо- и кетотетроз, альдо- и кетопентоз, альдо- и кетогексоз D-ряда приведены ниже.
Таблица. Ряд D-альдоз
206

Таблица. Ряд D-кетоз
Строение альдогексоз Линейные формы альдогексоз
Линейные формы альдогексоз являются стетеоизомерами пентаоксигексаналя, имеющего четыре асимметрических атомов углерода.
Общая формула:
6 |
5 |
4 |
3 |
2 |
|
1 |
O |
||||
|
|
|
|
|
|
|
|||||
|
CH2-CH-CH-CH-CH-C |
H |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
OH OH OH OH OH |
|
||||||||||
В ряду альдогексоз всего имеется 24=16 стереоизомеров, 8 D,L (энантиомерных) пар, или 8 диастереомеров (см. таблицу альдогексоз). Наиболее распространенной в природе альдогексозой является D-глюкоза.
207

|
|
1 C |
O |
|
|
1 C |
O |
|||||
|
|
H |
|
|
H |
|||||||
|
|
|
|
2 |
|
|||||||
|
|
2 |
|
|
|
|
||||||
H |
|
|
OH |
|
HO |
|
|
|
H |
|||
|
|
|
|
|
|
|
||||||
|
|
|
|
3 |
|
|
|
|||||
3 |
|
|
|
H |
|
|
|
OH |
||||
|
|
|
|
|
|
|
|
|
||||
HO |
|
|
|
H |
|
|
|
|
|
|||
|
|
|
|
|
4 |
|
|
|
||||
|
4 |
|
|
|
HO |
|
|
|
H |
|||
|
|
|
|
|
|
|
|
|
||||
H |
|
|
OH |
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
||
H |
5 |
|
|
OH |
|
HO |
5 |
|
H |
|||
|
|
|
||||||||||
6 |
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
||||
|
|
CH2OH |
|
|
6 |
|
|
|
||||
|
|
|
|
CH2OH |
||||||||
|
|
|
|
|
|
|
|
L-глюкоза |
||||
|
|
D-глюкоза |
|
|
||||||||
По конфигурации пятого асимметрического атома углерода С5 - определяют принадлежность альдогексозы к D- или L-рядам, сравнивая с конфигурацией D- или L- глицеринового альдегида. D- и L-глюкозы являются
энантиомерами.
Кроме D-глюкозы, в природе наиболее часто встречаются D-манноза и D- галактоза, которые являются диастереомерами.
|
1 C |
O |
|
|
1 C |
O |
||||
|
|
H |
|
|
H |
|||||
|
2 |
|
|
2 |
|
|||||
|
|
|
|
|
||||||
HO |
|
|
|
H |
H |
|
|
|
OH |
|
|
|
|
|
|
|
|||||
|
|
|||||||||
|
3 |
|
|
|
3 |
|
|
|
||
HO |
|
|
|
H |
HO |
|
|
|
H |
|
|
|
|
|
|
|
|||||
|
|
|||||||||
|
4 |
|
|
|
4 |
|
|
|
||
H |
|
|
|
OH |
HO |
|
|
|
H |
|
|
|
|
|
|
|
|||||
|
|
|
||||||||
|
5 |
|
|
|
5 |
|
|
|
||
H |
|
|
|
OH |
H |
|
|
|
OH |
|
|
|
|
|
|
|
|||||
|
|
|
||||||||
|
|
|
|
6 |
|
|
||||
|
6 |
CH2OH |
CH2OH |
|||||||
|
D-манноза |
D-галактоза |
||||||||
Диастереомеры, способные к взаимному превращению, называются эпимерами. Эпимеры отличаются по конфигурации у второго асимметричного атома углерода, следовательно D-глюкоза и D-манноза – эпимеры.
Циклические формы альдогексоз
Полиоксиальдегиды (полиоксикетоны), содержащие пять, шесть и семь атомов углерода способны к внутримолекулярной циклизации. Циклизация происходит за счет взаимодействия карбонильной и одной из доступных для циклизации гидроксильных групп, при этом получаются пяти-, шести- и семичленные циклические полуацетали (см. тему “Альдегиды, кетоны”).
208
|
-δ |
|
|
|
|
OH |
||
+δ O |
+δ |
-δ |
||||||
|
|
|||||||
R-C |
|
+ H |
|
OR1 |
|
|
|
|
H |
|
H+ |
R-CH-OR1 полуацеталь |
|||||
|
|
|
|
|||||
R,R1 - алкилы
Сначала рассмотрим, как происходит циклизация исходя из проекций Фишера. Напоминаем, что карбонильная группа плоская, следовательно возможны два варианта атаки гидроксильной группы и образование двух соединений (см. также циангидридный синтез в теме “Оксикислоты”).
|
|
+δ |
|
-δ |
|
|
|
O |
|||
|
|
1 C |
|
H |
|
|
|
2 |
|
|
|
H |
|
|
OH |
||
3 |
|
|
|||
HO |
|
|
|
H |
|
|
|
|
|
||
|
4 |
|
|
||
H |
|
|
OH |
||
|
|
|
|||
5 |
|
|
|||
H |
|
|
O |
||
|
|
|
|||
|
|
6 |
|
|
-δ |
|
|
|
|
||
|
|
CH2OH |
|||
|
|
D-глюкоза |
|||
полуацетальный H гидроксил
+δ
|
|
|
|
полуацетальный |
|
1 * |
|
гидроксил |
|
H |
OH |
|
||
|
C |
|
||
H |
2 |
|
OH |
|
|
|
|
||
HO |
3 |
|
H |
|
|
|
O |
||
|
4 |
|
|
|
H |
|
OH |
|
|
|
|
|
||
H |
5 |
|
|
|
|
|
|
|
|
|
6 |
CH2OH |
α-аномер |
|
HO |
1 * |
H |
|
|
|
C |
|
||
H |
2 |
|
OH |
|
|
|
|
||
HO |
3 |
|
H |
O |
|
|
|||
H |
4 |
OH |
|
|
|
|
|
||
H |
5 |
|
|
|
|
|
|
|
|
|
6 |
CH OH |
β-аномер |
|
|
|
|||
|
|
|
2 |
|
В образовавшихся циклических формах (α- и β-) атом углерода С-1 становится асимметрическим атомом углерода, следовательно при наличии пяти С* существует 25=32 циклические формы альдогексоз D- и L – рядов. α и β- Формы одной монозы являются диастереомерами и имеет собственное название - аномеры. У α-аномера полуацетальный гидроксил и связь С5-О располагаются в цис-конфигурации , а у β-аномера – в транс-конфигурации.
Для того чтобы перейти от изображения циклической формы в виде проекции Фишера к более современному изображению в виде проекций Хеуорса, необходимо выполнить следующее преобразование: произвести две
209

перестановки у пятого С так, чтобы гидроксильная группа оказалась в нижней части проекции Фишера (конфигурация этого асимметрического атома углерода при этом сохраняется). Далее образовать α- и β-циклы.
Проекции Хеуорса изображают в виде шестичленного кольца, нумеруя асимметрические атомы углерода так, как показано на схеме. Заместители располагаются на вертикалях. Те заместители, которые находятся слева от вертикали в проекции Фишера, будут располагаться наверху в проекции Хеуорса.
|
|
O |
|
|
O |
H |
|
OH |
|
|
1 C |
|
1 C |
|
|
C |
|||
|
H |
|
H |
|
|
||||
|
2 |
|
|
2 |
|
2 |
|
||
H |
OH |
H |
OH |
H |
OH |
||||
3 |
|
|
|||||||
HO |
H |
две перестановки |
3 |
|
HO |
3 |
H |
||
|
у С5 HO |
|
H |
|
|||||
|
4 |
|
|
4 |
|
|
4 |
O |
|
H |
OH |
H |
OH |
H |
OH |
||||
|
|
|
|||||||
H |
5 |
OH |
6CH |
5 |
H |
CH2 |
5 |
H |
|
|
|||||||||
|
|
|
2 |
|
|
|
|
|
|
|
6 CH2OH |
OH |
OH |
|
OH |
6 |
|
||
α,β-циклы  - два варианта расположения Н и ОН
- два варианта расположения Н и ОН
|
|
H |
|
OH |
|
|
полуацетальный -ОН |
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
C |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
2 |
|
|
|
|
|
|
|
6 CH OH |
|
|
|
|
|
|||||||
|
H |
|
|
|
|
|
|
OH |
|
|
|
H |
5 |
2 |
|
|
|
H |
|
H H |
||
|
3 |
|
|
|
|
|
|
O |
|
|
||||||||||||
|
HO |
|
|
H |
|
|
переход к |
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
O |
4 |
|
OH |
H |
|
|
1 |
|
|
||||||
4 |
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
H |
|
|
OH |
проекции |
|
|
|
|
|
|
2 |
|
|
|
O |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
Хеуорса |
|
|
|
3 |
|
|
|
|
α |
|
|||
6 |
|
5 |
|
|
|
|
|
OH |
|
|
|
|
OH |
4H-пиран |
||||||||
CH2 |
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
OH |
полуацетальный ОН |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
α-D-глюкопираноза
наверху в проекции Хеуорса
В α-аномере полуацетальный гидроксил расположен под циклом, в β- аномере – над циклом. Шестичленный кислородсодержащий цикл называется пираном, отсюда название α- и β-форм – пиранозы (похожи на пиран). Название α- и β-аномеров для D-глюкозы - α-D-глюкопираноза и β-D-
210

глюкопираноза соответственно; для D-маннозы - α-D- и β-D-маннопиранозы и для D-галактозы – α-D и β-D-галактопиранозы.
Кроме шестичленного возможно образование пятичленного – фуранозного цикла (фуран – пятичленный кислородосодержащий цикл). При этом в циклизации участвует гидроксил при С*-4. Ниже приведены соответствующие преобразования для D-маннозы.
|
1 C |
O |
|
|
1C |
O |
|
|
H |
|
OH |
|
|
H |
|
|
H |
|
|
1 C |
|
|
|||
|
2 |
|
|
2 |
|
|
|
|
|
|||
HO |
H |
|
HO |
H |
|
|
|
2 |
|
|
||
|
|
|
|
HO |
|
H |
|
|||||
HO |
3 |
H |
две перестановки |
HO |
3 |
|
|
|
|
|
||
H |
|
|
|
|
|
|
||||||
|
у С4 |
|
циклизация |
HO |
|
3 |
H |
O |
||||
H |
4 |
OH |
6 |
H 5 |
4 |
|
|
|
|
|
||
H2C |
H |
6 |
5 H |
|
4 |
|
|
|||||
H |
5 |
OH |
OH |
OH |
OH |
|
H2C |
|
|
|
H |
|
|
|
OH |
OH |
|
|
|
||||||
|
CH2OH |
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
||
D-манноза |
|
|
|
|
|
наверху в проекции |
|
|||||
|
|
|
|
|
|
|
|
|||||
|
6 CH |
OH |
|
|
6 |
CH |
OH |
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
HO |
5 |
|
2 |
|
H |
|
|
HO |
|
5 |
|
|
|
H |
|
|
|
OH |
|
||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
O |
H |
|
|
|
|
|
|
|
O |
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
|
||||||
|
|
|
|
|
|
|
1 |
|
4 HO |
|
OH |
O |
|||||||||
|
4 |
HO |
OH |
|
|
||||||||||||||||
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
2 |
H |
фуран |
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3 |
|
|
|||||
|
H |
3 |
2 |
OH |
|
|
|
|
|
||||||||||||
|
|
|
|
H |
|
|
|||||||||||||||
|
|
|
|
|
H |
H |
|
|
|
|
|
H |
|
|
|
||||||
|
|
|
α-D-маннофураноза |
|
|
|
|
β- D-маннофураноза |
|
||||||||||||
Строение альдопентоз
Линейные формы альдопеннтоз являются стереоизомерами тетраоксипентаналя, имеющего три асимметрических атома углерода.
Общая формула:
5 |
4 |
3 |
2 |
1 |
O |
||
|
|
|
|
|
|||
CH2- |
CH-CH-CH-C |
|
|||||
|
|
H |
|||||
OH |
|
|
|
|
|
||
OH OH |
OH |
|
|
||||
В ряду альдопентоз всего имеется 23=8 стереоизомеров, четыре D,L-пары, четыре диастереоизомера. Строение линейных форм альдопентоз в виде проекций Фишера приведено в общей таблице. Циклические формы
211

альдопентоз являются преимущественно фуранозными. Ниже представлены линейная и две циклические формы D-рибозы.
|
1 C |
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
2 |
|
|
|
CH2OH |
|
H |
|
|
CH2OH |
|
|
OH β |
||||
H |
|
|
OH |
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
O |
||||||||||
|
3 |
|
|
|
|
|
H |
O |
1 |
|
H |
1 |
|||||
H |
|
|
OH |
4 |
|
H |
4 |
H |
|||||||||
|
|
|
|
||||||||||||||
4 |
|
|
|||||||||||||||
H |
|
|
OH |
H |
|
|
|
|
2 OH α |
H |
|
|
|
2 |
|
||
|
|
|
|
|
3 |
|
|
3 |
|
H |
|||||||
|
|
|
|||||||||||||||
|
5 |
|
|
|
|
HO |
OH |
|
|
HO |
OH |
|
|||||
|
CH OH |
|
|
|
|
||||||||||||
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
D-рибоза |
|
|
α-D-рибофураноза |
|
|
β- D-рибофураноза |
||||||||||
Строение кетогексоз
Линейные формы кетогексоз являются стереоизомерами пентаоксигексанона-2, имеющего три асимметрических атома углерода. Общая формула:
6 |
5 |
4 |
3 |
2 |
1 |
|
|
|
|
|
|
CH2-CH-CH-CH-C-CH2
OH OH OH OH O OH
В ряду кетогексоз всего имеется 23=8 стереоизомеров, четыре D,L-пары, четыре диастереоизомера. Проекции Фишера кетогексоз приведены в общей таблице.
Циклические формы кетогексоз, главным образом, являются фуранозными, хотя возможны и пиранозные. Ниже приведены линейная и две циклические формы D-фруктозы.
|
1 |
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H2C |
6 |
|
|
1 |
6 |
|
|
|
|
|
||||||
|
2 C |
|
|
|
|
|
|
|
|
|
|||||||
|
|
O |
|
CH2OH |
|
CH2OH |
|
CH2OH |
O |
OH β |
|||||||
|
|
||||||||||||||||
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|||
HO |
3 |
|
|
H |
5 |
|
H |
|
OH 2 |
5 |
|
H |
|
OH |
2 |
||
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|||||||||||||
4 |
|
|
H |
|
|
|
3 OH α |
H |
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||
H |
|
|
OH |
4 |
|
4 |
3 |
CH2OH |
|||||||||
|
|
|
|
||||||||||||||
|
|
|
|||||||||||||||
|
5 |
|
|
|
|
|
HO |
|
H |
|
|
HO |
|
H |
1 |
||
H |
|
|
OH |
|
|
|
|
|
|
|
|||||||
6 |
|
|
|
|
α-D-фруктофураноза |
|
|
β-D-фруктофураноза |
|||||||||
|
|
|
|
|
|
|
|
||||||||||
|
CH2OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
D-фруктоза |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
212

Цикло-цепная таутомерия моноз
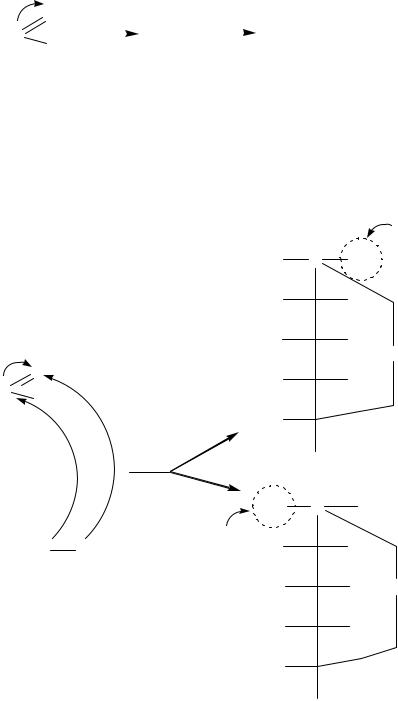
Все монозы в кристаллическом состоянии имеют циклическое строение (α- или β-). При растворении в воде циклический полуацеталь разрушается, превращаясь в линейную (оксо) форму. Линейная форма, в свою очередь циклизуется, образуя α и β – циклы. Линейная форма и обе циклические формы взаимно превращаются и находятся в состоянии динамического равновесия, то есть являются таутомерами, отсюда термин – цикло-цепная таутомерия (или аномеризация – превращение α- или β-аномера через линейную (оксо) форму).
Оптическим проявлением этого процесса является мутаротация – изменение удельного угла вращения плоскополяризованного света в водных растворами моноз (и восстанавливающих биоз) до постоянного. Ниже приведены схемы цикло-цепной таутомерии для альдо- и кетогексоз.
Альдогексозы
|
6 |
CH2OH |
|
|
|
|
|
|
6 |
CH2OH |
|
|
|
|
|
|
|
6 |
CH2OH |
|
|
|||||||||
H |
5 |
|
O |
H |
|
|
|
|
H |
5 |
|
-δ +δ |
|
H |
5 |
|
O |
OH |
||||||||||||
|
|
|
|
|
|
|
|
|
OH |
|
O |
|
|
|
H |
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
4 |
|
H |
|
1 |
|
|
|
4 |
|
H |
4 |
|
|
1 |
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
C 1 |
|
|
|
|
|
|
|||||||||||||
|
|
|
OH |
H |
|
|
|
|
|
|
OH |
H |
|
|
|
|
|
|
|
OH |
H |
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
3 |
|
|
2 O H |
|
|
|
|
|
|
3 |
|
|
2 |
|
H |
|
|
|
|
3 |
|
|
2 H |
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
OH |
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|||||||||
|
|
H |
|
OH |
|
|
|
|
|
|
H |
|
OH |
|
|
|
|
|
|
|
H |
OH |
|
|||||||
α-D-глюкопираноза |
|
|
|
линейная или оксо-форма |
|
β-D-глюкопираноза |
||||||||||||||||||||||||
(или α-D-глюкоза) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(или β-D-глюкоза) |
||||||||||||||
|
|
[α] = + 1100 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
[α] = - 190 |
|
|||||||
|
|
36% |
|
|
|
|
|
|
|
0,02% |
= + 530 |
|
|
|
|
|
|
|
64% |
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
[α] |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
раствора |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
Кетогексозы
6 CH2OH |
|
|
1 |
CH2OH |
6 CH |
OH |
|
1 |
|
6 CH OH |
|
||
|
O |
|
|
2 |
|
OH |
CH2OH |
2 |
O |
OH |
|||
5 H |
|
OH |
|
|
5 H |
|
5 |
||||||
|
|
|
|
|
OH C |
|
H |
OH |
|||||
|
|
|
2 |
|
H |
|
|
|
2 |
O |
|
|
2 |
H 4 |
|
3 |
O |
H 4 |
|
3 |
|
|
H 4 |
3 |
1CH2OH |
||
|
H |
|
|
|
|
|
|||||||
HO |
|
|
|
|
HO |
|
H |
|
HO |
H |
|||
α-D-фруктофураноза |
|
линейная или оксо-форма |
β-D-фруктофураноза |
||||||||||
(или α-D-фруктоза) |
|
|
|
|
|
|
(или β-D-фруктоза) |
||||||
Следует отметить, что содержание линейной формы в мутаротированном растворе, как правило, менее 1%.
213

Пространственное строение циклических и линейных форм гексоз
Пиранозные циклы имеют кресловидную конформацию, гидроксильные группы и атомы водорода расположены экваториально или аксиально (см. тему “Циклоалканы”). Наиболее устойчивы β-аномеры, в которых полуацетальный гидроксил занимает экваториальное положение. Самой стабильной из альдогексоз является β-D-глюкоза, в которой все гидроксильные группы расположены экваториально.
|
H 6 |
|
|
|
|
|
|
|
|
H 6 |
|
|
|
|
|
|
|
|
HO |
6 |
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
4 |
|
CH |
OH H |
|
|
|
|
4 |
CH |
OH |
|
|
|
4 |
CH2OH H |
|
|
|
|
|
||||||||||||||
|
|
|
|
2 5 |
|
|
O |
|
|
|
|
2 |
|
5 |
OHO |
|
H |
|
|
5 |
|
O |
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
HO |
|
|
|
|
|
|
|
|
|
|
|
|
HO |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
HO 3 |
|
|
H |
2 |
OH |
|
1 |
OH |
HO |
3 |
|
H |
2 |
H |
|
1 |
OH |
HO |
3 |
|
H 2 |
OH |
|
|
1 |
OH |
||||||||
|
|
|
|
|
|
|
||||||||||||||||||||||||||||
|
|
|
|
|||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
|
|
H |
|
|
|
|
H |
|
|
|
H |
|
|
|
|
H |
|
|
H |
|
|
|
|
H |
||||||||||
β-D-глюкоза |
|
|
|
|
|
β-D-манноза |
|
|
|
|
β-D-галактоза |
|||||||||||||||||||||||
Форма линейных молекул является зигзагообразной, за счет образования водородных связей между гидроксильными группами происходит дополнительное закрепление конформации.
|
OH |
OH |
|
1 O |
|
|
5 |
|
|
||
|
|
|
C |
||
6 |
4 |
3 |
2 |
||
H |
|||||
CH2 |
|
|
|
||
OH |
......... OН .......OH |
|
|||
Реакционная способность
Для химических свойств моноз характерны две группы реакций – по линейной (оксо-) форме и циклическим формам.
I. Реакции по оксо-форме моноз
Эти реакции проходят в полярных растворителях (часто в водных растворах), при этом за счет цикло-цепной таутомерии циклической формы моноз образуют оксо-формы. Взаимодействие реагентов с оксо-формами приводит к смещению таутомерного равновесия в сторону оксо-формы. В реакциях, где происходят превращения оксо-формы принято писать только проекцию Фишера, подразумевая, что оксо-форма появляется из циклической формы.
214
1. Окисление
а)
|
|
|
|
O |
Ag(NH3)2OH (реактив Толенса) * |
O |
|||||||||
|
|
C |
|
|
|
|
|
|
|
C |
|
OH |
|||
|
|
|
H |
- Ag |
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
||||||
H |
|
|
|
OH |
Cu2+ (реактив Фелинга) * |
H |
|
|
|
OH |
|||||
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
HO |
|
|
|
|
H |
- Cu2O |
|
HO |
|
|
|
|
H |
||
|
|
|
|
|
|
|
|||||||||
H |
|
|
|
OH |
p. HNO3 |
|
H |
|
|
|
OH |
||||
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
H |
|
|
|
OH |
- NO2 |
H |
|
|
|
OH |
|||||
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
CH OH |
|
|
CH2OH |
|||||||||
|
|
|
|
2 |
|
|
Br2 / H2O |
|
|
|
|
|
|
||
D-глюкоза |
D-глюконовая кислота |
||||||||||||||
|
|
||||||||||||||
SrCO
-HBr3 качественные реакции
Вреакциях окисления монозы играют роль восстановителей. При окислении моноз с помощью выше приведенных реагентов происходит окисление только карбонильной группы и образуется ряд гликоновых (оновных, альдольных) кислот.
из D-маннозы |
D-манноновая кислота |
|
из D-галактозы |
D-галактоновая кислота |
|
Для получения |
гликоновых кислот обычно используют |
Br2/H2O в |
присутствии солей Sr2+ и Ca2+. При этом образующиеся гликоновые кислоты превращаются в соответствующие соли, например в глюконат кальция при окислении D-глюкозы.
|
|
|
O |
|
|
C |
O 2 Ca |
H |
|
OH |
|
|
|||
HO |
|
H |
|
|
|||
H |
|
OH |
|
|
|||
H |
|
OH |
|
|
|||
CH2OH
глюконат кальция
215
