
- •1.Основные понятия и законы химии
- •2.Основные понятия и законы химии
- •3.Основные понятия и законы химии
- •4.Основные понятия и законы химии
- •5.Основные понятия и законы химии
- •6.Строение и св-ва атомов
- •7.Строение и св-ва атомов
- •8.Строение и св-ва атомов
- •9.Строение и св-ва атомов
- •10.Строение и св-ва атомов
- •11.Химическая связь и строение молекул
- •12.Химическая связь и строение молекул
- •13.Химическая связь и строение молекул
- •14.Химическая связь и строение молекул
- •15.Химическая связь и строение молекул
- •16.Энергетика химических процессов
- •17.Энергетика химических процессов
- •18.Энергетика химических процессов
- •19.Энергетика химических процессов
- •21.Химическая кинетика и химическое равновесие
- •23.Химическая кинетика и химическое равновесие
- •24.Химическая кинетика и химическое равновесие
- •25.Химическая кинетика и химическое равновесие
- •27.Растворы. Дисперсные системы.
- •28.Растворы. Дисперсные системы.
- •29.Вопрос: Осмос, осмотическое давление. Закон Вант-Гоффа для бесконечно разбавленных растворов неэлектролитов.
- •30.Растворы. Дисперсные системы.
- •31.Растворы. Дисперсные системы.
- •32.Растворы. Дисперсные системы.
- •33.Растворы. Дисперсные системы.
- •34.Растворы. Дисперсные системы.
- •35.Растворы. Дисперсные системы.
- •36.Растворы. Дисперсные системы.
- •41.Окислительно-восстановительные реакции. Электрохимические системы.
- •42.Окислительно-восстановительные реакции. Электрохимические системы.
- •43.Окислительно-восстановительные реакции. Электрохимические системы.
- •44.Окислительно-восстановительные реакции. Электрохимические системы.
- •45.Окислительно-восстановительные реакции. Электрохимические системы.
- •46.Окислительно-восстановительные реакции. Электрохимические системы.
- •47.Окислительно-восстановительные реакции. Электрохимические системы.
- •48.Окислительно-восстановительные реакции. Электрохимические системы.
- •49.Окислительно-восстановительные реакции. Электрохимические системы.
- •50.Окислительно-восстановительные реакции. Электрохимические системы.
- •51.Полимерные органические материалы
- •52.Полимерные органические материалы
- •53.Полимерные органические материалы
- •54.Полимерные органические материалы
- •55.Полимерные органические материалы
- •56.Полимерные органические материалы
- •57.Полимерные органические материалы
- •58.Полимерные органические материалы
35.Растворы. Дисперсные системы.
Вопрос: Ионные реакции, смещение ионного равновесия.
Ионные реакции — реакции между ионами в растворе. Например, реакцию
AgNO3 + NaCl = NaNO3 + AgCl
можно представить в ионном виде (реакция расписывается на ионы, не расписываются осадки, газы, вода, слабые кислоты и основания, а также малорастворимые и нерастворимые соединения) например AgClнерастворим в воде и на ионы не расписывается:
Ag+ + NO3− + Na+ + Cl− = AgCl + Na+ + NO3−
Одинаковые ионы сокращаются и получается сокращенное ионное уравнение. Так как взаимодействие произошло между ионами Ag+ и ионами Cl−, то выражение
Ag+ + Cl− = AgCl
и есть ионное уравнение рассматриваемой реакции. Оно проще молекулярного и в то же время отражает сущность происходящей реакции.
Ионное равновесие, как и любое другое, смещается при изменении концентрации одного из ионов. Например, если в раствор уксусной кислоты, диссоциирующей по уравнению
CH3COOHH+ + CH3COO–
ввести какую-либо соль этой кислоты и тем самым увеличить концентрацию ионов CH3COO–, то в соответствии с принципом Ле-Шателье * равновесие смещается влево. Отсюда следует, что введение в раствор слабого электролита * одноименных ионов (т.е. ионов, одинаковых с одним из ионов электролита) уменьшает степень диссоциации * этого электролита.
Аналогично нарушается равновесие в случае малорастворимого электролита (соли). Например, если к насыщенному раствору сульфата кальция CaSO4 добавить другой, хорошо растворимый сульфат (K2SO4), то вследствие увеличения концентрации ионов SO42– равновесие сместится в сторону образования кристаллов (образуется осадок CaSO4). Этот процесс прекратится, когда произведение концентраций [Ca2+] и [SO42–] станет равно произведению растворимости *, т.е. установится новое состояние равновесия.
На основании рассмотренных примеров можно сделать следующий вывод: реакции в растворах электролитов всегда идут в сторону образования наименее диссоциированных или наименее растворимых веществ. Из этого, в частности, следует, что сильные кислоты вытесняют слабые из растворов их солей:
CH3COONa + HCl = CH3COOH + NaCl
Суть этой реакции более точно отражается ионно-молекулярным уравнением, где формулы слабых электролитов записаны в виде молекул, а сильных – в виде ионов:
CH3COO– + Na+ + H+ + Cl– = CH3COOH + Na+ + Cl–
или в сокращенном виде:
CH3COO– + H+ = CH3COOH
Аналогично протекают реакции между сильными основаниями и солями слабых оснований. Например:
FeSO4 + 2 NaOH = Na2SO4 + Fe(OH)2
Fe2+ + SO42– + 2 Na+ + 2 OH– = SO42– + 2 Na+ + Fe(OH)2
Fe2+ + 2 OH– = Fe(OH)
36.Растворы. Дисперсные системы.
Вопрос: Гидролиз солей. Константа и степень гидполиза.
Гидролиз солей – это взаимодействие ионов соли с водой с образованием малодиссоциирующих частиц.
Гидролиз, дословно, - это разложение водой. Давая такое определение реакции гидролиза солей, мы подчеркиваем, что соли в растворе находятся в виде ионов, и что движущей силой реакции является образование малодиссоциирующих частиц (общее правило для многих реакций в растворах).
Всегда ли ионы способны образовывать с водой малодиссоциирующие частицы? Разбирая этот вопрос с учениками, отмечаем, что катионы сильного основания и анионы сильной кислоты таких частиц образовать не могут, следовательно, в реакцию гидролиза не вступают.
Какие типы гидролиза возможны? Поскольку соль состоит из катиона и аниона, то возможно три типа гидролиза:
-гидролиз по катиону (в реакцию с водой вступает только катион);
-гидролиз по аниону (в реакцию с водой вступает только анион);
-совместный гидролиз (в реакцию с водой вступает и катион, и анион);
Гидролиз по катиону приводит к образованию гидроксокатионов и ионов водорода (среда раствора кислая).
Отмечаем, что только иногда, при n=1, вместо гидроксокатионов получаем молекулы слабого основания.
А может ли гидроксокатион вступить в реакцию со следующей молекулой воды? Сообщаем, что это будет вторая ступень гидролиза, и что каждая следующая ступень протекает в тысячи раз слабее, чем предыдущая, что даже первая ступень протекает обычно на доли процента. Поэтому, как правило, рассматривается только первая ступень гидролиза.
Гидролиз по аниону разбираем аналогично, записываем уравнение:
Ann– + H-OH « HAn(n-1)– + OH–
Гидролиз по аниону приводит к образованию гидроанионов и гидроксид-ионов (среда раствора щелочная).
Совместный гидролиз. Из самого названия следует, что в этом случае в растворе протекают две выше рассмотренные реакции. Предлагаем школьникам проанализировать их и сделать вывод о реакции среды. Опровергаем (можно экспериментом) представление о том, что среда будет нейтральной. Одинаковое число ионов водорода и гидроксид-ионов только на бумаге. На самом деле здесь протекают две независимые обратимые реакции, и каких ионов в растворе окажется больше, зависит от степени протекания каждой реакции. А это, в свою очередь, зависит от того, что слабее, кислота или основание. Если слабее основание, то в большей степени будет протекать гидролиз по катиону и среда раствора будет кислой. Если слабее основание – наоборот. Как исключение, возможен случай, когда среда будет почти нейтральной, но это только исключение.
---Если соль образована катионом сильного основания и анионом слабой кислоты (S2-, CO32-, CN- и др.), то происходит гидролиз по аниону.
Например, карбонат натрия Na2CO3в растворе подвергается гидролизу по аниону, так как соль образована слабой угольной кислотой (CO32- - анион от слабого электролита).
---Если соль образована катионом слабого основания и анионом сильной кислоты, то происходит гидролиз по катиону.
Примером служит процесс взаимодействия с водой нитрата меди (II) Сu(NO3)2. Гидролиз в этом случае обусловлен образованием малодиссоциирующих частиц (CuOH)+. В результате равновесие электролитической диссоциации воды смещается и в растворе появляется избыток ионов водорода, поэтому реакция среды становится кислой (рН<7). Очевидно, чем слабее основание, тем полнее идет гидролиз.
---Гидролиз солей, образованных слабым основанием и слабой кислотой протекает достаточно глубоко (практически полностью).
Гидролиз некоторых солей, образованных очень слабыми основаниями и кислотами, является практически необратимым процессом
---Соли, образованные сильным основанием и сильной кислотой,гидролизу не подвергаются. В этом случае равновесие диссоциации воды в присутствии ионов соли почти не нарушается. Поэтому растворы таких солей практически нейтральную реакцию среды.
NaCl– гидролиз не протекает, так как соль образована сильным основанием и сильной кислотой. Среда нейтральная, рН = 7
Степень гидролиза – это отношение числа молекул, подвергшихся гидролизу (N)к общему числу молекул в растворе ( N0 ).
h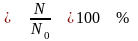 Степень
гидролиза изменяется в пределах от 0
до 100%. Другой количественной характеристикой
процесса гидролиза является константа
гидролиза,
характеризующая собой равновесия
процесса гидролиза.
Степень
гидролиза изменяется в пределах от 0
до 100%. Другой количественной характеристикой
процесса гидролиза является константа
гидролиза,
характеризующая собой равновесия
процесса гидролиза.
Если соль образована слабой кислотой, то константа гидролиза равна отношению константы воды и константы диссоциации слабой кислоты (см. табл. приложении).
 Если
соль образована слабым основанием, то
константа гидролиза равна отношению
константы воды и константы диссоциации
слабого основания.
Если
соль образована слабым основанием, то
константа гидролиза равна отношению
константы воды и константы диссоциации
слабого основания.
 Если
соль образована слабым основанием и
слабой кислотой, то константа гидролиза
равна отношению: в числителе – константа
воды, а в знаменателе - произведение
констант диссоциации слабой кислоты
и слабого основания.
Если
соль образована слабым основанием и
слабой кислотой, то константа гидролиза
равна отношению: в числителе – константа
воды, а в знаменателе - произведение
констант диссоциации слабой кислоты
и слабого основания.
 Из
приведенных формул следует, что чем
слабее электролит, образовавший соль,
тем больше значение константы гидролиза,
и тем глубже протекает процесс гидролиза.
Из
приведенных формул следует, что чем
слабее электролит, образовавший соль,
тем больше значение константы гидролиза,
и тем глубже протекает процесс гидролиза.
37.Растворы. Дисперсные системы.
Вопрос: Общие понятия о дисперсных системах.

 38.Растворы.
Дисперсные системы.
38.Растворы.
Дисперсные системы.
Вопрос: Коллоидные растворы и методы их получения.




39.Растворы. Дисперсные системы.
Вопрос: Оптические и электрические св-ва коллоидных растворов.



40.Растворы. Дисперсные системы.
Вопрос: Коагуляция, седиментация и пептизация.



Седиментация (от лат. sedimentum — оседание), оседание или всплывание частиц дисперсной фазы (твёрдых крупинок, капелек жидкости, пузырьков газа) в жидкой или газообразной дисперсионной среде в гравитационном поле или поле центробежных сил. С. происходит, если направленное движение частиц под действием силы тяжести или центробежной силы преобладает над хаотическим тепловым движением частиц (см. Броуновское движение, Диффузия). Скорость С. зависит от массы, размера и формы частиц, вязкости и плотности среды, а также ускорения, возникающего при действии на частицы сил поля. Для мелких не взаимодействующих между собой сферических частиц скорость С. определяется по Стокса формуле. С. в дисперсных системах (особенно с газовой дисперсионной средой) часто сопровождается укрупнением седиментирующих частиц вследствие коагуляции или коалесценции.
Пептизация, самопроизвольный распад агрегатов (комочков, хлопьев, сгустков), образованных скоплением слипшихся коллоидных частиц, на агрегаты меньших размеров или отдельные первичные частицы. Особенно наглядна П. студенистых осадков (коагелей), возникающих вследствие коагуляции золей и высокодисперсных суспензий. При П. происходит "коллоидное растворение" осадка — из коагулята вновь образуется золь. Внешнее сходство этого явления с растворением белков, расщепленных ферментом пепсином, определило происхождение термина. П. можно наблюдать при повышении температуры, удалении коагулирующих реагентов (см. Коагулянты) промыванием осадка. Наиболее характерна П. при введении в дисперсионную среду пептизаторов — веществ, способствующих дезагрегированию, то есть разъединению слипшихся частиц. Пептизаторами могут быть электролиты и поверхностно-активные вещества, вызывающие лиофилизацию (см. Лиофильность и лиофобность) поверхности частиц дисперсной фазы. Так, П. геля гидроокиси железа в водной среде возможна при добавлении небольших количеств хлорного железа, а каолин пептизируется гуминовыми кислотами. Перемешивание обычно ускоряет П. Процессы рекристаллизации и коалесценции, которые часто протекают в коллоидных осадках при старении, препятствуют П., так как приводят к сращиванию частиц. Затруднена также П. осадков, выпавших при коагулировании золей поливалентными ионами и полиэлектролитами.
П. используют для получения жидких дисперсных систем из порошков или паст в химической и пищевой технологии. Важная роль принадлежит П. в совокупности процессов, определяющих моющее действие, формирование и разрушение различных дисперсных структур. Иногда П. вредна, например при водоочистке, осветлении вин и др.
