
- •Введение
- •1. Динамика рафинирования стали от примеси
- •2.Оценка равновесной концентрации водорода и азота в стали
- •3.Оценка равновесной концентрации серы в стали
- •4.Примеры расчетов
- •4.1.Десульфурация металла в открытом процессе
- •1) Постановка задачи
- •2) Исходные данные
- •3) Расчет
- •3.1) Расчет ионной доли анионов кислорода в шлаке
- •3.2) Расчет сульфидной емкости шлака
- •3.3) Расчет окислительного потенциала системы
- •3.4) Расчет коэффициента активности серы в металле
- •3.6) Расчет коэффициента распределения серы
- •3.7) Расчет равновесной концентрации серы
- •3.8) Расчет удельной мощности перемешивания
- •3.9) Расчет коэффициента объемного массопереноса
- •3.10) Расчет динамики десульфурации
- •4.2.Десульфурация металла при вакуум-шлаковой обработке
- •1) Постановка задачи
- •2) Исходные данные
- •3) Расчет
- •3.1) Расчет ионной доли анионов кислорода в шлаке
- •3.2) Расчет сульфидной емкости шлака
- •3.3) Расчет окислительного потенциала системы
- •3.4) Расчет коэффициента активности серы в металле
- •3.6) Расчет коэффициента распределения серы
- •3.7) Расчет требуемой кратности шлака
- •4.3.Удаление водорода при ковшевом вакуумировании
- •1) Постановка задачи
- •2) Исходные данные
- •3) Расчет
- •3.1) Расчет равновесной концентрации водорода
- •3.3) Расчет коэффициента объемного массопереноса
- •3.4) Расчет времени вакуумирования металла в ковше, необходимого для снижения содержания водорода до заданного уровня.
- •4.4.Удаление азота при ковшевом вакуумировании
- •1) Постановка задачи
- •2) Исходные данные
- •3) Расчет
- •3.1) Расчет равновесной концентрации азота
- •3.2) Расчет доли свободной поверхности
- •3.4) Расчет коэффициента объемного массопереноса
- •3.5) Расчет динамики удаления азота
- •Список использованных источников
3.2) Расчет сульфидной емкости шлака
Расчет константы равновесия реакции десульфурации
½{S2} + (O2-) = (S2-) + ½{O2}
Исходя из соотношения (27)
![]()
Соответственно, К (S) = 0,0048.
Расчет сульфидной емкости шлака
Согласно соотношениям (25) и (28)
![]()
3.3) Расчет окислительного потенциала системы
Расчет окисленности металла
Металл раскислен алюминием. Процесс открытый. В связи с этим окисленность металла определяем исходя из равновесия с алюминием.
Расчет логарифма константы равновесия обратной реакции
В соответствии с соотношение (39)
![]()
Оценка активности продукта раскисления
Расчет активности Al2O3 проводим, исходя из представлений о полимерной теории строения жидких шлаков, по соотношению (40).
И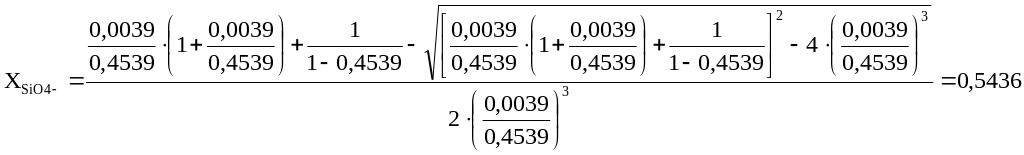 онная
доля
согласно
соотношению (41) равна
онная
доля
согласно
соотношению (41) равна
Для расчета ионной доли AlO+ определяем число грамм-ионов катионов.
Катион |
Ca2+ |
Mg2+ |
Mn2+ |
Fe2+ |
AlO+ |
сумма |
n, грамм-ион |
1,107 |
0,100 |
0,007 |
0,007 |
0,167 |
1,388 |
Тогда ионная доля AlO+ равна
![]()
В![]() соответствии с выражением (40) активность
Al2O3
равна
соответствии с выражением (40) активность
Al2O3
равна
Расчет окисленности металла
Согласно соотношению (38)
![]()
Соответственно, [O] = 3,3·10-5 %.
Расчет окислительного потенциала системы
Исходя из соотношения (36)
![]() атм.
атм.
3.4) Расчет коэффициента активности серы в металле
Для расчета необходимы справочные данные по параметрам взаимодействия
Параметры взаимодействия первого порядка esi * 102
C |
Si |
Mn |
Cr |
Ni |
Mo |
11 |
6,3 |
-2,6 |
-1,1 |
0 |
0,27 |
V |
Ti |
Al |
P |
S |
Cu |
-1,6 |
-7,2 |
3,5 |
29 |
-2,8 |
-0,84 |
Используя соотношение (24), получаем
lg ɣs = 0,0149;
ɣs = 1,0348.
3.5) Расчет константы равновесия реакции ½{S2} = [S]
Согласно соотношению (23)
![]()
Тогда K[S] = 350,49.
3.6) Расчет коэффициента распределения серы
В соответствии с соотношением (21)
![]()
.
3.7) Расчет равновесной концентрации серы
Согласно соотношению (19)
![]()
3.8) Расчет удельной мощности перемешивания
Расчет удельной интенсивности продувки
Результаты расчета с использованием соотношения (11) представлены в таблице
Q, л/мин |
100 |
300 |
600 |
G, м3/(кг·с) |
1,67·10-8 |
5,00·10-8 |
1,00·10-7 |
Расчет удельной мощности перемешивания
Результаты расчета по соотношению (10) для различных расходов инертного газа представлены в таблице
Q, л/мин |
100 |
300 |
600 |
ɛ, Вт/кг |
0,024 |
0,071 |
0,141 |
