
- •Введение
- •1. Динамика рафинирования стали от примеси
- •2.Оценка равновесной концентрации водорода и азота в стали
- •3.Оценка равновесной концентрации серы в стали
- •4.Примеры расчетов
- •4.1.Десульфурация металла в открытом процессе
- •1) Постановка задачи
- •2) Исходные данные
- •3) Расчет
- •3.1) Расчет ионной доли анионов кислорода в шлаке
- •3.2) Расчет сульфидной емкости шлака
- •3.3) Расчет окислительного потенциала системы
- •3.4) Расчет коэффициента активности серы в металле
- •3.6) Расчет коэффициента распределения серы
- •3.7) Расчет равновесной концентрации серы
- •3.8) Расчет удельной мощности перемешивания
- •3.9) Расчет коэффициента объемного массопереноса
- •3.10) Расчет динамики десульфурации
- •4.2.Десульфурация металла при вакуум-шлаковой обработке
- •1) Постановка задачи
- •2) Исходные данные
- •3) Расчет
- •3.1) Расчет ионной доли анионов кислорода в шлаке
- •3.2) Расчет сульфидной емкости шлака
- •3.3) Расчет окислительного потенциала системы
- •3.4) Расчет коэффициента активности серы в металле
- •3.6) Расчет коэффициента распределения серы
- •3.7) Расчет требуемой кратности шлака
- •4.3.Удаление водорода при ковшевом вакуумировании
- •1) Постановка задачи
- •2) Исходные данные
- •3) Расчет
- •3.1) Расчет равновесной концентрации водорода
- •3.3) Расчет коэффициента объемного массопереноса
- •3.4) Расчет времени вакуумирования металла в ковше, необходимого для снижения содержания водорода до заданного уровня.
- •4.4.Удаление азота при ковшевом вакуумировании
- •1) Постановка задачи
- •2) Исходные данные
- •3) Расчет
- •3.1) Расчет равновесной концентрации азота
- •3.2) Расчет доли свободной поверхности
- •3.4) Расчет коэффициента объемного массопереноса
- •3.5) Расчет динамики удаления азота
- •Список использованных источников
3) Расчет
3.1) Расчет ионной доли анионов кислорода в шлаке
Содержание SiO2 в шлаке больше 10%, поэтому расчет ионной доли О2- в шлаке проводим, исходя из полимерной теории строения жидких шлаков.
Расчет мольных долей компонентов шлака
Результаты представим в виде таблицы.
Компонент |
CaO |
MgO |
MnO |
FeO |
SiO2 |
Al2O3 |
сумма |
мас.% |
62 |
5 |
0 |
0 |
16 |
17 |
100 |
М, г/моль |
56 |
40 |
71 |
72 |
60 |
102 |
|
n, моль |
1.107 |
0.125 |
0.000 |
0.000 |
0.267 |
0.167 |
1.665 |
X, доли |
0.665 |
0.075 |
0.000 |
0.000 |
0.160 |
0.100 |
1 |
Расчет констант полимеризации компонентов бинарных расплавов
Расчет проводим с использованием справочных данных по изменению энтальпии и энтропии для соответствующих реакций полимеризации.
Oxid |
Hп |
SSiO2 |
SAl2O3 |
CaO |
76200 |
-12,8 |
0,6 |
MgO |
76200 |
10,0 |
16,6 |
MnO |
13200 |
-6,8 |
-3,0 |
FeO |
13200 |
7,0 |
7,0 |
Расчет изменений энергии Гиббса для соответствующих реакций полимеризации компонентов бинарных расплавов
ΔGi - q = ΔHi - q – T · ΔSi - q
Oxid |
SiO2 |
Al2O3 |
CaO |
100254,3 |
74997,3 |
MgO |
57446,4 |
45167,9 |
MnO |
25862,4 |
18749,3 |
FeO |
0,0 |
0,0 |
Расчет натуральных логарифмов констант полимеризации компонентов бинарных расплавов
Ln Kпi –q = - ΔGi – q / (RT)
Oxid |
SiO2 |
Al2O3 |
CaO |
-6,438 |
-4,816 |
MgO |
-3,689 |
-2,901 |
MnO |
-1,661 |
-1,204 |
FeO |
0,000 |
0,000 |
Расчет логарифма константы полимеризации многокомпонентного расплава
И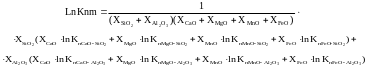 сходя
из соотношения (31)
сходя
из соотношения (31)
После подстановки получаем
Ln (Kпm) = -5,568.
Расчет константы полимеризации многокомпонентного расплава
Kпm = 0,0038.
Расчет обобщенной степени полимеризации
Исходя из соотношений (30) и (32)
где
После подстановки получаем
α = 0,0044.
Расчет ионной доли анионов кислорода
Исходя из соотношения (29)
После подстановки получаем
X (O2-) = 0,4612.
