
- •Химия, ч. 2. Органическая химия
- •1. Информация о дисциплине
- •Предисловие
- •Место дисциплины в учебном процессе.
- •Содержание дисциплины и виды учебной работы
- •Содержание дисциплины по гос
- •Объем дисциплины и виды учебной работы
- •Раздел 1. Общие вопросы теоретической органической химии
- •1.2. Основные понятия органической химии
- •Раздел 2. Углеводороды
- •2.1. Алифатические углеводороды
- •2.2. Циклические углеводороды
- •Раздел 3. Важнейшие классы производных углеводородов (28 часов)
- •3.1. Гомофункциональные соединения
- •3.2. Гетероциклические и элементоорганические соединения
- •Раздел 4. Высокомолекулярные соединения
- •4.1. Общие представления о высокомолекулярных соединениях (вмс)
- •4.2. Методы синтеза высокомолекулярных соединений
- •4.3. Промышленные органические полимеры
- •Заключение
- •2.2. Тематический план дисциплины
- •2.2.1. Тематический план дисциплины для студентов очной формы обучения
- •2.2.2. Тематический план дисциплины
- •2.2.3. Тематический план дисциплины
- •При использовании информационно-коммуникационных технологий
- •2.5. Практический блок Лабораторные работы
- •3. Информационные ресурсы дисциплины
- •3.1. Библиографический список
- •3.2. Опорный конспект Введение
- •Раздел 1 Общие вопросы теоретической органической химии
- •Основные сырьевые источники органических соединений
- •1.2. Основные понятия органической химии
- •1. Циклоалканы
- •2. Циклоалкены, циклоалкины
- •Вопросы для самопроверки
- •Раздел 2
- •2.1. Алифатические углеводороды
- •Циклические углеводороды
- •Вопросы для самопроверки
- •Раздел 3 Важнейшие классы производных углеводородов
- •3.1. Гомофункциональные соединения
- •Свойства спиртов
- •Простые и сложные эфиры
- •Классификация аминов
- •3.2. Гетероциклические и элементоорганические соединения
- •Вопросы для самопроверки
- •Раздел 4 Высокомолекулярные соединения
- •4.1. Общие представления о высокомолекулярных соединениях
- •4.2. Методы синтеза высокомолекулярных соединений
- •4.3. Промышленные органические полимеры
- •Характеристика некоторых клеев и клеевых композиций представлена в разделе 4.1.1. (пример 7). Вопросы для самопроверки
- •Заключение
- •3.3. Глоссарий
- •3.4. Методические указания к выполнению лабораторных работ предисловие
- •3.4.1. Общие указания
- •3.4.2. Охрана труда и техника безопасности правила техники безопасности при работе в лаборатории оказание первой помощи при несчастных случаях
- •Первая помощь при ожогах и отравлениях
- •Растворители, применяемые для приготовления охлаждающих смесей с твердой углекислотой
- •Методы очистки и выделения органических соединений
- •Определение основных физических констант органических веществ
- •3.4.4. Лабораторные синтезы органических соединений
- •Отчет №
- •6. Выводы по работе. Синтезы азокрасителей
- •Получение полимеров реакцией полимеризации
- •Мономеры и вспомогательные вещества
- •Винилацетат (с4н6о2)
- •Пероксид бензоила (с14н10о4)
- •Получение полимеров реакцией поликонденсации
- •Мономеры и вспомогательные вещества
- •4. Блок контроля освоения дисциплины
- •4.1. Задания на контрольную работу и методические указания к ее выполнению
- •Распределение задач по шифрам для студентов специальности 150501.65
- •Контрольная работа
- •4.1.1. Примеры решения контрольных задач
- •Свойства отечественных полиэпоксидных смол
- •Свойства эпоксидных клеевых соединений в зависимости от природы отвердителя
- •4.2. Текущий контроль
- •Каменноугольная смола является источником…
- •Правильные ответы на тренировочный тест рубежного контроля
- •4.3. Итоговый контроль
- •Приложения
- •1. Основные сырьевые источники органических соединений
- •2. Углеводороды и радикалы (алкилы)
- •6. Краткая характеристика наиболее типичных полимеров, получаемых реакцией поликонденсации и методом полимераналогичных превращений
- •7. Полимерные композиционные материалы, свойства, области применения
- •О8. Свойства исходных соединений, применяемых в синтезах
Получение полимеров реакцией поликонденсации
ПОЛИКОНДЕНСАЦИЯ – ступенчатый процесс образования полимеров из би- или полифункциональных веществ (мономеров), элементарные акты этого процесса представляют собой реакции замещения. Поликонденсация сопровождается выделением низкомолекулярного продукта (воды, хлористого водорода), что существенно отличает этот процесс от полимеризации.
Если в поликонденсации участвуют молекулы одного мономера, имеющего разнородные, способные к взаимодействию между собой функциональные группы, то процесс называют гомополиконденсацией. Если в поликонденсации участвуют молекулы двух мономеров, каждый из которых содержит однородные функциональные группы, не способные реагировать между собой, но способные реагировать с функциональными группами второго мономера, то процесс называют гетерополиконденсацией.
При использовании бифункциональных мономеров поликонденсацию называют линейной (работа 7). Линейная поликонденсация приводит к образованию полимеров линейного строения. Если в процессе участвуют мономеры с функциональностью больше двух, то поликонденсацию называют трехмерной; такая поликонденсация приводит к образованию сетчатых полимеров (работа 8).
Поликонденсационные полимеры отличаются, как правило, узким молекулярно-массовым распределением. При линейной поликонденсации молекулярная масса полимера зависит от соотношения количеств мономеров, максимальное значение молекулярной массы достигается при строгой эквивалентности их количеств. Кроме того, для получения полимера высокой молекулярной массы низкомолекулярный продукт необходимо удалять из зоны реакции.
Процесс поликонденсации часто осложняется параллельно протекающими побочными реакциями. К ним относятся реакции деструкции концевых групп, например:
реакции декарбоксилирования:
– R– C – OH – R – H + CO2
║
O
реакции дегидратации:
–О – СН2 – СН2 – ОН – О – СН=СН2 + Н2О
реакции окисления спиртовых групп до альдегидных:
– О – СН2 – СН2 – ОН + 0,5 О2 – О – СН2 – СНО + Н2О
образование простых эфирных связей:
– R – OH + OH – R –– R – O – R – + Н2О
Процессы деструкции концевых групп усиливаются с ростом температуры и в присутствии кислорода и ведут к снижению молекулярной массы полимера.
К поликонденсационным полимерам относятся, например, феноло-формальдегидные смолы. Еще в 70-х годах прошлого века было установлено, что при нагревании фенола с формалином образуются смолообразные вещест-
ва. В 1902 году были получены первые искусственные смолы (новолаки), получившие применение для производства быстропрессующихся пресс-порошков, вспененных материалов и лаков.
Новолаки представляют собой продукты поликонденсации фенола или его гомологов с формальдегидом в кислой среде. Фенольный компонент берут в избытке, отношение фенол : формальдегид составляет обычно 1,10 1,25 моль/моль. В качестве катализатора используют соляную, щавелевую, реже – серную кислоты. Средняя степень полимеризации новолаков п = 48.
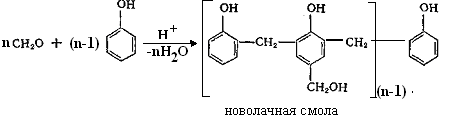
Новолаки – термопласты, способные многократно плавиться при повышении температуры и затвердевать при охлаждении. Они растворимы в водных растворах щелочей, фенолах и многих органических растворителях.
В 1907 году были получены твердые смолы типа бакелита.
При взаимодействии фенола с формальдегидом сначала получаются фенолоспирты, которые при дальнейшей конденсации образуют более сложные высокомолекулярные вещества линейного строения (резолы):
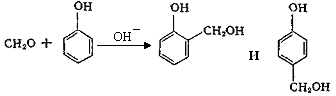
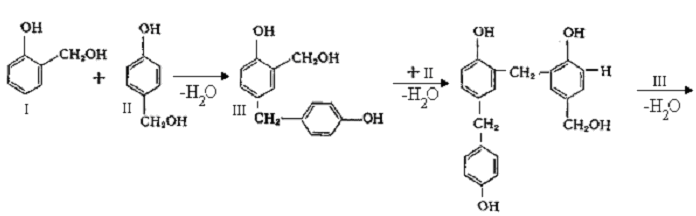

Изменяя условия реакции поликонденсации (повышая рН или понижая температуру), можно приостановить процесс на какой-либо промежуточной стадии. Когда полимер предполагается использовать в производстве изделий, клеев, лаков, реакцию целесообразно прервать на начальной стадии поликонденсации (молекулярная масса 700—1000). Смесь олигомеров со средней степенью полимеризации около 7 представляет собой твердую, очень хрупкую, прозрачную аморфную массу янтарного цвета. При 60—90 оС смесь переходит в жидкое состояние, легко растворяется в спирте, ацетоне, бензоле. Такую смесь олигомеров называют резолом.
Резольные олигомеры (резольные смолы, резолы) получают конденсаци-
ей фенола с формальдегидом в щелочной среде. Фенольный компонент берут в недостатке. При синтезе резолов отношение фенол : формальдегид берут в пре-
делах 0,770,91 моль/моль. Резолы представляют собой смесь линейных и разветвленных олигомеров.В качестве щелочных катализаторов конденсации используют едкий натр или аммиачную воду. Резольные олигомеры раствори-
мы в водных растворах щелочей и во многих органических растворителях.
Резолы термореактивны – при нагревании они отверждаются – переходят в неплавкое, нерастворимое состояние. При этом полимер переходит из вязкотекучего в высокоэластическое состояние, утрачивает растворимость, но еще сохраняет способность сильно набухать в органических растворителях. При дальнейшем нагревании частота сшивок возрастает, и полимер превращается в твердый, нерастворимый резит.
Резолы получают в виде твердых смол, лаков и водных эмульсий.
