
- •Глава 5. Адсорбция газов и паров на поверхности твердых тел. Адсорбция из растворов на поверхности твердых тел
- •1.Уравнение Лэнгмюра
- •В некоторых случаях применяется уравнение Ленгмюра вида:
- •2. Уравнение изотермы адсорбции теории бэт
- •3.Уравнение изотермы адсорбции Фрейндлиха
- •4.Уравнение Никольского.
- •Площадь, занимаемую молекулой бензола, примите равной 0,49 нм2.
- •Площадь занимаемая одной молекулой азота в адсорбционном слое 0,16 нм2.
3.Уравнение изотермы адсорбции Фрейндлиха
Уравнение Фрейндлиха для адсорбции газа имеет вид:
![]() (11)
(11)
K и 1/n –постоянные уравнения Фрейндлиха.
Чаще всего это уравнение применяется в логарифмической форме:
![]() (12)
(12)
Уравнение в такой форме позволяет построить линейную зависимость lnA от lnp и графически определить оба постоянных параметра.
Логарифмическое уравнение Фрейндлиха для адсорбции из раствора имеет вид:
![]() (13)
(13)
Графически определяем постоянные параметры по линейной зависимости lnA от lnC.(рис.2)
Отрезок, отсекаемый на оси ординат равен lg k, а тангенс угла наклона прямой
равен 1/n.
Р ис.2.
Изотерма адсорбции в координатах
логарифмического уравнения.
ис.2.
Изотерма адсорбции в координатах
логарифмического уравнения.
4.Уравнение Никольского.
При ионообменной адсорбции происходит стехиометрический обратимый обмен ионов между объемом раствора электролитов и адсорбентом.
Процессы ионного обмена на твердой поверхности характеризуются уравнением Б.П.Никольского:
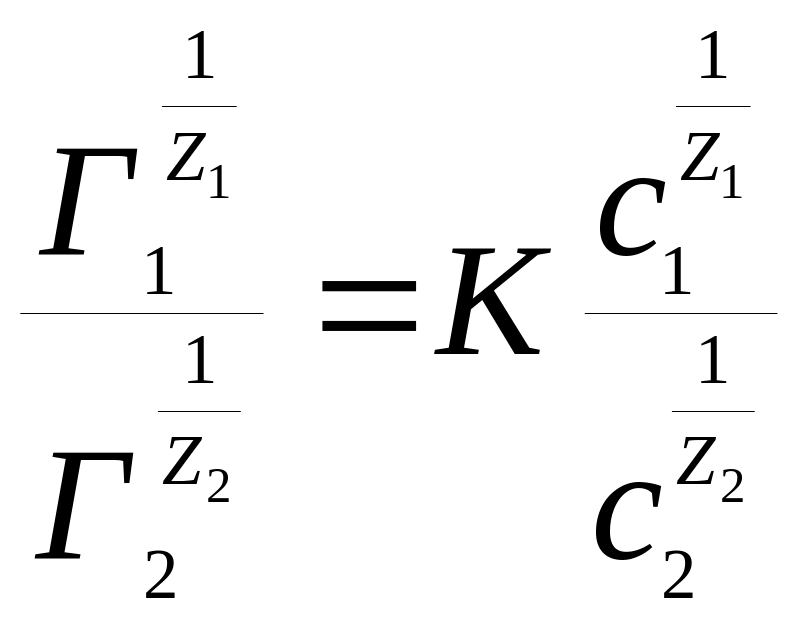 (14)
(14)
где
![]() и
и
![]() - количество ионов, поглощенных
поверхностью сорбента (кмоль/кг),
- количество ионов, поглощенных
поверхностью сорбента (кмоль/кг),
![]() и
и
![]() - равновесные концентрации ионов в
растворе (кмоль/
- равновесные концентрации ионов в
растворе (кмоль/![]() ),
К – константа обмена, зависящая от
способности ионов к адсорбции на данном
сорбенте.
),
К – константа обмена, зависящая от
способности ионов к адсорбции на данном
сорбенте.
Графически уравнение Б.П.Никольского изображается прямой, тангенс угла наклона которой и представляют величину константы К.
Примеры решения задач:
1. Рассчитать удельную поверхность адсорбента по изотерме адсорбции бензола на его поверхности. Площадь, занимаемая молекулой бензола, S0=49·10-20 м2.
p P/PS |
0.024 |
0.08 |
0.14 |
0.20 |
0.27 |
0.35 |
0.46 |
a·103, моль/кг |
14,9 |
34,8 |
47,2 |
56,8 |
66,3 |
79.3 |
101.0 |
Решение. Проверяют применимость к экспериментальным данным теории БЭТ. С этой целью рассчитывают абсциссу и ординату уравнения изотермы адсорбции БЭТ в линейной форме, т.е.
![]() и
и
![]()
Результаты вычислений сводят в таблицу 1 и строят график зависимости y=f(x)
Таблица 1.
p/ps |
y, кг/моль |
p/ps |
y, кг/моль |
0,024 |
1,650 |
0,27 |
5,466 |
0,08 |
2,499 |
0,35 |
6,790 |
0,14 |
3,449 |
0,46 |
8,343 |
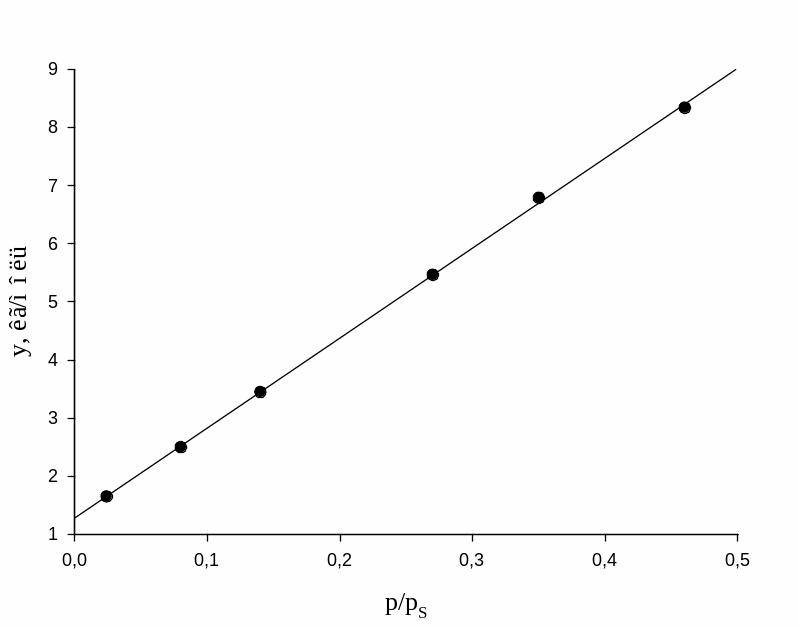
Рис.1 изотерма адсорбции в координатах линейной формы уравнения БЭТ.
Для определения адсорбционной емкости монослоя аm по графику зависимости у=f(x) находят константы уравнения прямой линии: отрезок, отсекаемый на оси ординат при p/ps=0, b0=1.24 кг/моль, и угловой коэффициент прямой b1=15.8 кг/моль. Для сравнения вычисляют b0 и b1
методом наименьших квадратов. Данные для расчёта b0 и b1 приведены в таблице 2.
Таблица 2.
n |
x |
y, кг/моль |
xy, кг/моль |
x2 |
1 |
0,024 |
1,650 |
0,0396 |
5,76·10-4 |
2 |
0,080 |
2,499 |
0,2000 |
6,4·10-3 |
3 |
0,140 |
3,499 |
0,4830 |
1,96·10-2 |
4 |
0,200 |
4,400 |
0,8800 |
4,00·10-2 |
5 |
0,270 |
5,466 |
1,4550 |
7,08·10-2 |
6 |
0,350 |
6,790 |
2,3765 |
0,123 |
7 |
0,460 |
8,434 |
3,8778 |
0,212 |
k=13,65 и am=0,0489 моль/кг.
По величине аm рассчитывают удельную поверхность адсорбента:
S=S0amNA=49·10-20·0,0489·6,02·1023=14,4·103 м2/кг.
2. Вычислить предельный адсорбционный объём активированного угля БАУ по изотерме адсорбции бензола (таблица 3). Молярный объём бензола vm=89·10-6 м3/моль.
Таблица 3.
p/ps |
a, моль/кг |
p/ps |
a, моль/кг |
p/ps |
a, моль/кг |
1,33·10-6 |
0,50 |
1,63·10-2 |
2,25 |
0,327 |
2,86 |
2,13·10-5 |
0,85 |
3,77·10-2 |
2,39 |
0,460 |
3,00 |
1,21·10-4 |
1,18 |
9,47·10-2 |
2,56 |
0,657 |
3,19 |
5,60·10-4 |
1,55 |
0,201 |
2,74 |
0,847 |
4,47 |
Решение.
Проверяют применимость уравнения
(II.15) к экспериментальным
данным. С этой целью вычисляют lg
a и
![]() (таблица
4) и строят график зависимости
(таблица
4) и строят график зависимости
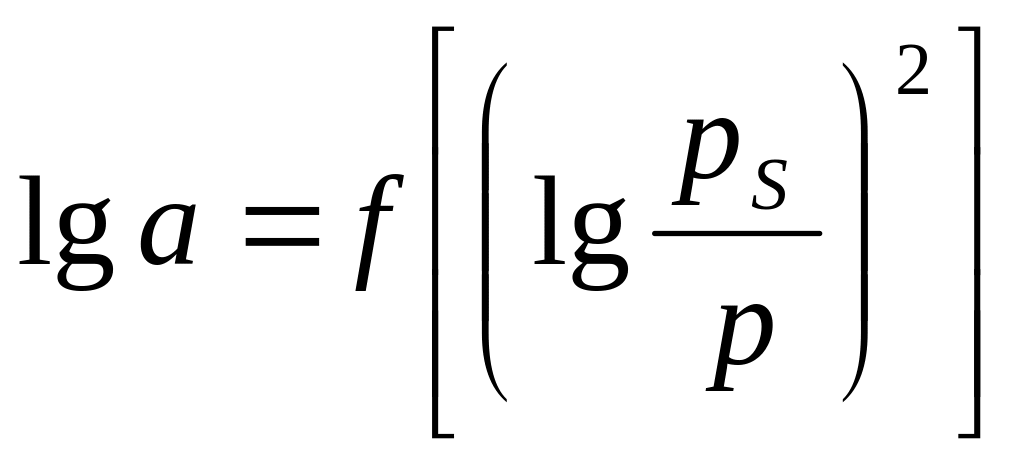 (Рис. II.2)
(Рис. II.2)
Таблица 4.
|
lg a |
|
lg a |
|
lg a |
34,52 |
-0,3010 |
3,19 |
0,3522 |
0,230 |
0,4564 |
21,82 |
-0,0706 |
2,03 |
0,3784 |
0,113 |
0,4771 |
15,34 |
0,0719 |
1,05 |
0,4082 |
0,033 |
0,5038 |
10,58 |
0,1903 |
0,48 |
0,4378 |
0,005 |
0,6503 |
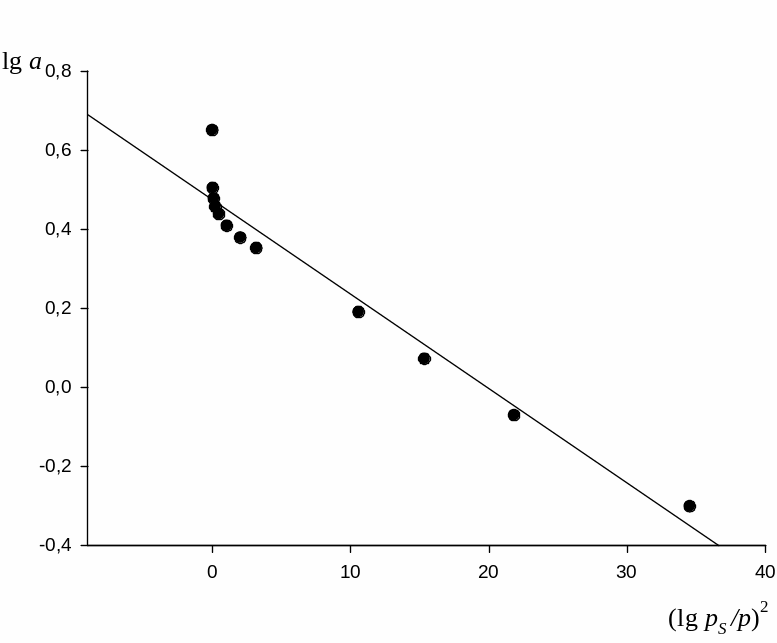
Рис.2 Изотерма адсорбции в координатах линейной формы уравнения М.М.Дубинина.
Как видно из рис.2, экспериментальные точки с хорошим приближением укладываются на прямую линию и, следовательно, уравнение (15) применимо к адсорбции бензола на активированном угле БАУ.
По отрезку,
отсекаемому па оси lg a
при
=0,
находят
![]() =0,435
и
=0,435
и
V0=0,239·10-3м3/кг.
3. По экспериментальным данным сорбции паров воды на активированном угле при Т = 293 К построить кривую капиллярной конденсации. Показать наличие гистерезиса и, используя ветвь десорбции, построить интегральную и дифференциальную кривые распределения пор по радиусам.
P/PS •••••••• 0,1 0,2 0,4 0,6 0,8 0,9 0,98
аадс ·103,моль/кг.... 3,75 5,3 6;2 8,75 10,4 12, 5 13 ,4
адес·103, моль/кг . . .. 3,75 7,0 7,9 10,0 11,5 13,0 13,4
Vm=18·10 -3м3/моль, σ= 72,5-10-3 Дж/м2.'
Решение. Строят изотерму капиллярной конденсации в соответствии с условием задачи. Выбирают ряд точек на ветви десорбции (не менее шести—восьми), соответствующих определенным значениям p/pS, и рассчитывают объем пор, заполненных конденсатом, по уравнению V=aVm. Затем для этих же значений по уравнению
![]()
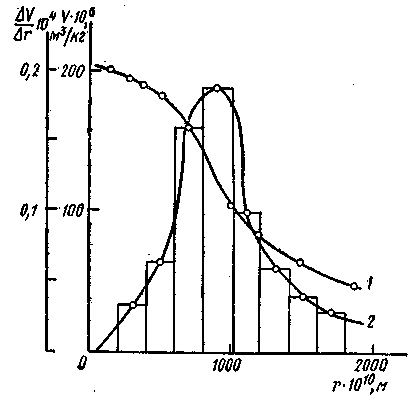
рассчитывают максимальный радиус пор, заполненных конденсатом при соответствующих давлениях p/ps. Полученные данные записывают в табл. 5 и строят структурную кривую адсорбента в координатах V=f(r). Из кривой находят ряд значений ΔV/Δr (табл.6) и строят дифференциальную кривую распределения объёма пор по радиусам в координатах ΔV/Δr=f(r)
Таблица.5 Данные для построения интегральной кривой распределения объёма пор по радиусам.
№ точки |
P/PS |
aдес·103,моль/кг |
V·106,м3/кг |
r·1010,м |
1 2 3 4 5 6 7 8 |
0,05 0,1 0,2 0,4 0,6 0,8 0,9 0,98 |
0,5 3,7 7,0 7,9 9,0 10,0 10,9 11,5 |
0,9 66,6 126,0 142,0 162,0 180,0 196,0 207,0 |
2,2 4,6 6,6 8,5 11,6 15,5 20,2 26,3 |
Таблица.6 Данные для построения дифференциальной кривой распределения объёма по радиусам.
ΔV/Δr·10-4,м2/кг |
Δr·1010,м |
ΔV/Δr·10-4,м2/кг |
Δr·1010,м |
ΔV/Δr·10-4,м2/кг |
Δr·1010,м |
5 16 30 15 |
2 2 2 2 |
7 5 5 4 |
2 2 2 2 |
3 3 1,5 0,5 |
2 2 2 2 |
Рис.3 Интегральная(1) и дифференциальная(2) кривые распределения.
Задачи
1. Ниже приведены экспериментальные данные по адсорбции азота на TiO2 (рутиле) при 75 К:
P·102 Па……….60,94 116,41 169,84 218,65 275,25
А, моль/кг……...0,367 0,417 0,467 0,512 0,567
Постройте график
соответствующий линейному уравнению
БЭТ. Найдите константы
![]() и k. Рассчитайте
удельную поверхность адсорбента.
Давление насыщенного пара азота при
указанной температуре Рs=78300
Па, площадь,
и k. Рассчитайте
удельную поверхность адсорбента.
Давление насыщенного пара азота при
указанной температуре Рs=78300
Па, площадь,
занимаемая одной молекулой азота S0=0,16 нм2.
2. Окись углерода адсорбируется на слюде; данные при 90 К представлены ниже. Определите, какой изотерме – Лэнгмюра или Фрейндлиха – лучше соответствуют эти данные? Каково значение К для адсорбционного равновесия? Взяв общую поверхность равной 6200см2, рассчитайте площадь, занимаемую каждой адсорбированной молекулой.
Vа, см3……………..0,130 0,150 0,162 0,166 0,175 0,180
Р, мм. рт. cт.………...100 200 300 400 500 600.
3.При измерении адсорбции газообразного азота на активном угле при 194.4К были получены следующие данные:
р·10-3, Па……………….1,86 6,12 17,96 33,65 68,89
А·103, м3/кг…………..…5,06 14,27 23,61 32,56 40,83
Значения А даны для азота при нормальных условиях.
Рассчитайте, постоянные в уравнение Лэнгмюра и удельную поверхность активированного угля, принимая плотность газообразного азота равной
1,25 кг/м3, а площадь занимаемую одной молекулой азота на поверхности адсорбента, равной 0,16 нм2 .
4.При измерении адсорбции азота на активированном угле при 273 К были получены следующие данные:
А,см3/г…………..……0,987 3,04 5,08 7,04 10,31
Р, мм. рт. ст…….……3,93 12,98 22,94 34,01 56,23
Построить график в координатах, в которых происходит спрямление уравнения изотермы Лэнгмюра, и определить константы этого уравнения.
5.Определите константы эмпирического уравнения Фрейндлиха, используя следующие данные об адсорбции диоксида углерода на активном угле при 293 К:
Р·10-3, Па…………1,00 4,48 10,0 14,4 25,0 45,2
А·102, кг/кг……….3,23 6,67 9,62 11,72 14,5 17,7.
6.Используя уравнение БЭТ, построить изотерму адсорбции бензола по нижеуказанным данным и рассчитайте удельную поверхность адсорбента по изотерме адсорбции бензола (варианты 1-4):
1. P/Ps.………..0,04 0,08 0,16 0,22 0,27 0,36 0,46
А, моль/кг……....0,348 0,483 0,624 0,724 0,805 0,928 0,13
2. Р/Рs………... 0,05 0,12 0,19 0,26 0,34 0,44 0,50
А, моль/кг ……. 0,31 0,593 0,795 0,99 1,21 1,525 1,77
3. Р/Рs……….…0,03 0,07 0,12 0,17 0,24 0,31 0,38
А, моль/кг……... 0,196 0,301 0,373 0,423 0,488 0,52 0,625
4. Р/Рs…………. 0,02 0,05 0,11 0,19 0,25 0,3 0,36
А, моль/кг……....0,104 0,196 0,298 0,387 0,443 0,488 0,55
