
Эффект Джоуля-Томпсона.
В опытах Джоуля и Томсона измерялась температура в двух сечениях непрерывного и стационарного потока газа (до и после пористой перегородки).
В результате трения газа при прохождении перегородки скорость газового потока была малой и кинетическая энергия практически не изменялась.
Газ, первоначально занимавший объем V1 при давлении Р1, перетекает сквозь перегородку, занимая объем V2 при давлении Р2 (рис. 5.14).
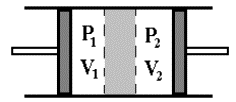
Рис. 5.14
Целью опытов Джоуля и Томсона было обнаружение сил межмолекулярного взаимодействия газа.
При прохождении газом перегородки происходит замедление теплового движения его молекул и температура понижается. Расширение газа в условиях адиабатического дросселирования не меняет его внутренней энергии, но вызывает увеличение потенциальной энергии взаимодействия молекул (расстояние между молекулами увеличивается) за счет кинетической энергии.
При этом над системой совершается работа
А = Р1V1 - P2V2. (5.22)
В адиабатическом процессе эта работа идет на изменение его внутренней энергии (первое начало термодинамики, DQ=0), т.е.
U2 - U1 = Р1V1 - P2V2. (5.23)
Следовательно,
U1+Р1V1=U2+Р2V2=Н=сonst, (5.24)
где Н - энтальпия .
Поэтому, зная уравнение состояния газа и выражение для энтальпии Н, можно найти DТ. Для идеального газа внутренняя энергия и энтальпия зависят только от температуры. Из формулы (5.24) следует равенство температур, т.е. для идеального газа DТ=0. Эффект Джоуля-Томсона считают положительным, если газ в процессе дросселирования охлаждается (DТ<0), и отрицательным, если газ нагревается (DТ>0). Например, при перепаде давления на дросселе, равном атмосферному, измеренная разность температур для воздуха DТ= - 0,250 С (опыт проводился при комнатной температуре).
Для водорода и углекислого газа в тех же условиях, разность температур составила, соответственно:ΔTH2 = +0,02 °С; ΔTCO2 = -1,25°С.
В зависимости от условий протекания сквозь перегородку один и тот же газ может как нагреваться, так и охлаждаться.
Температура Тi, при которой разность DТ, переходя через нулевое значение, меняет знак, называется температурой инверсии эффекта Джоуля-Томсона.
Совокупность точек температуры инверсии на диаграмме Р-Т называют кривой инверсии. Для точек на самой кривой эффект равен нулю. На рис. 5.15 приведена кривая инверсии азота.

Рис. 5.15
Из условия постоянства энтальпии (5.17) следует, что эффект Джоуля-Томсона характеризуется небольшими изменениями температуры при малых перепадах давления.
Поэтому дифференциальный эффект можно описать формулой
, (5.25)
где - теплоемкость газа при постоянном давлении; Н - энтальпия.
Кривая инверсии реального газа соответствует уравнению
RTbV2 = 2a(V - b)2. (5.26)
Так как эффект Джоуля-Томсона является необратимым процессом, энтропия газа возрастает.
Эффект Джоуля-Томсона является одним из способов получения низких температур в комбинации с адиабатическим расширением при сжижении газов.
На практике при больших перепадах давления на дросселе температура газа может изменяться довольно значительно (интегральный эффект Джоуля-Томсона).
Например, при дросселировании от 200 атм до 1 атм и начальной температуре 17 С воздух охлаждается на 35 С.
