
- •Эндоцитоз.
- •Экзоцитоз.
- •Диацитоз.
- •Накопительную
- •Секреторную
- •Агрегационную
- •8) Пероксисомы. Строение и функции.
- •9) Митохондрии. Энергетический обмен в клетке.
- •1. Сократительного белка актина
- •2. Миозина
- •11) Ядро клетки. Строение и функции.
- •Хроматин.
- •Ядерный сок (кариолимфа).
- •Ядрышко.
- •Образование связей между основаниями
- •Химические модификации оснований
- •Повреждение днк
- •Суперскрученность
- •Структуры на концах хромосом
- •Биологические функции
- •Химический состав и модификации мономеров
- •Структура
- •Сравнение с днк
- •]Типы рнк
- •Участвующие в трансляции
- •Участвующие в регуляции генов
- •В процессинге рнк
- •[Править]Ретровирусы и ретротранспозоны
- •Гипотеза рнк-мира
- •Роль в организме
- •Пути синтеза
- •15) Строение хромосом. Кариотип человека.
- •Первичная перетяжка
- •Вторичные перетяжки
- •Типы строения хромосом
- •Спутники (сателлиты)
- •Зона ядрышка
- •Хромонема
- •Хромосомные перестройки
- •Гигантские хромосомы
- •Политенные хромосомы
- •Хромосомы типа ламповых щёток
- •Бактериальные хромосомы
- •Хромосомы человека
- •Определение кариотипа
- •Процедура определения кариотипа
- •Классический и спектральный кариотипы
- •Анализ кариотипов
- •Аномальные кариотипы и хромосомные болезни
- •Уровни организации
- •Окружение белков
- •Образование и поддержание структуры белков в живых организмах
- •Синтез белков Химический синтез
- •Биосинтез белков
- •Универсальный способ: рибосомный синтез
- •Нерибосомный синтез
- •19) Митоз и его биологическое значение. Митоз, его фазы, биологическое значение
- •Нетипичные формы митоза
- •20) Апоптоз
- •Причины апоптоза
- •Патогенез апоптоза:
- •Морфологические проявления апоптоза
- •Сжатие клетки
- •Конденсация хроматина
- •Формирование апоптотических телец
- •Фагоцитоз
- •Значение апоптоза
- •21) Молекулярные основы канцерогенеза
Уровни организации
![]()
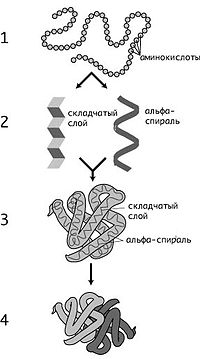
Уровни структуры белков: 1 — первичная, 2 — вторичная, 3 — третичная, 4 — четвертичная
Кроме последовательности аминокислот полипептида (первичной структуры), крайне важна третичная структура белка, которая формируется в процессефолдинга (от англ. folding, «сворачивание»). Третичная структура формируется в результате взаимодействия структур более низких уровней. Выделяют четыре уровня структуры белка[14]:
Первичная структура — последовательность аминокислот в полипептидной цепи. Важными особенностями первичной структуры являютсяконсервативные мотивы — сочетания аминокислот, играющих ключевую роль в функциях белка. Консервативные мотивы сохраняются в процессеэволюции видов, по ним часто удаётся предсказать функцию неизвестного белка.
Вторичная структура — локальное упорядочивание фрагмента полипептидной цепи, стабилизированное водородными связями. Ниже приведены самые распространённые типы вторичной структуры белков:
α-спирали — плотные витки вокруг длинной оси молекулы, один виток составляют 3,6 аминокислотных остатка, и шаг спирали составляет 0,54 нм[15] (так что на один аминокислотный остаток приходится 0,15 нм), спираль стабилизирована водородными связями между H и O пептидных групп, отстоящих друг от друга на 4 звена. Спираль построена исключительно из одного типа стереоизомеров аминокислот (L). Хотя она может быть как левозакрученной, так и правозакрученной, в белках преобладает правозакрученная. Спираль нарушают электростатические взаимодействия глутаминовой кислоты, лизина, аргинина. Расположенные близко друг к другу остатки аспарагина, серина, треонина и лейцинамогут стерически мешать образованию спирали, остатки пролина вызывают изгиб цепи и тоже нарушают α-спирали.
β-листы (складчатые слои) — несколько зигзагообразных полипептидных цепей, в которых водородные связи образуются между относительно удалёнными друг от друга (0,347 нм на аминокислотный остаток[15]) в первичной структуре аминокислотами или разными цепями белка, а не близко расположенными, как имеет место в α-спирали. Эти цепи обычно направлены N-концами в противоположные стороны (антипараллельная ориентация). Для образования β-листов важны небольшие размеры боковых групп аминокислот, преобладают обычно глицин и аланин.
π-спирали;
310-спирали;
неупорядоченные фрагменты.
Третичная структура — пространственное строение полипептидной цепи (набор пространственных координат составляющих белок атомов). Структурно состоит из элементов вторичной структуры, стабилизированных различными типами взаимодействий, в которых гидрофобные взаимодействия играют важнейшую роль. В стабилизации третичной структуры принимают участие:
ковалентные связи (между двумя остатками цистеина — дисульфидные мостики);
ионные связи между противоположно заряженными боковыми группами аминокислотных остатков;
водородные связи;
гидрофильно-гидрофобные взаимодействия. При взаимодействии с окружающими молекулами воды белковая молекула «стремится» свернуться так, чтобы неполярные боковые группы аминокислот оказались изолированы от водного раствора; на поверхности молекулы оказываются полярные гидрофильные боковые группы.
Четвертичная структура (или субъединичная, доменная) — взаимное расположение нескольких полипептидных цепей в составе единого белкового комплекса. Белковые молекулы, входящие в состав белка с четвертичной структурой, образуются на рибосомах по отдельности и лишь после окончания синтеза образуют общую надмолекулярную структуру. В состав белка с четвертичной структурой могут входить как идентичные, так и различающиеся полипептидные цепочки. В стабилизации четвертичной структуры принимают участие те же типы взаимодействий, что и в стабилизации третичной. Надмолекулярные белковые комплексы могут состоять из десятков молекул.
