
- •Синтез шиффовых оснований из 2-амино-6-нитро-метилбензтиазола
- •Содержание
- •Введение
- •1. Шиффовы основания
- •1.1. История открытия, определение и физические свойства
- •1.2. Получение шиффовых оснований
- •1.3. Химические свойства
- •1.4. Применение
- •2. Экспериментальная часть
- •2.1. Синтез 2-амино-6-метилбензтиозола с альдегидами ароматического ряда
- •2.2 Очистка полученных соединений
- •2.3. Определение температуры плавления
- •2.4. Регистрация ик спектров
- •Заключение
- •Список литературы
1.3. Химические свойства
Характерные свойства Шиффовых оснований связаны с полярностью группы –C=N-, строение которой может быть описано резонансом структур, это свидетельствует о том, что у группы –C=N- два центра: нуклеофильный и электрофильный:
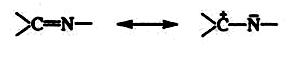
(3)
Электрофильные реагенты реагируют с Основаниями Шиффа по атому азота. С сильными кислотами и алкилгалогенидами образуются иминиевые соли (реакцию проводят в безводной среде из-за быстрого гидролиза последних); с хлорангидридами и ангидридами кислот - продукты присоединения, которые в присутствии триэтиламина превращаются в азетидиноны:
(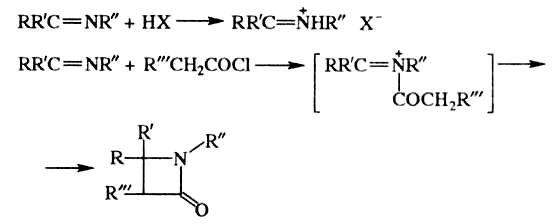 4)
4)
(5)
Реакции с нуклеофилами протекают по атому углерода. В присутствии разбавленных кислот основания Шиффа гидролизуются до аминов и кетонов; в щелочной среде большинство устойчиво; присоединяют амины; с реактивами Гриньяра и литийорганическими соединениями реагируют аналогично карбонильным соединениям:
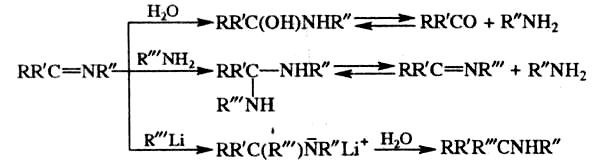
(6)
Для Шиффовых оснований характерны реакции циклоприсоединения. Так, с карбенами образуются азиридины (реакция 1), с кетенами -лактамы (2), с илидами фосфора (реакция протекает по типу реакции Виттига) - алкены и иминофосфораны (3), с 1,3-диполярными соединениями- пятичленные циклопродукты (4, 5):

(7)
(8)
(9)
(10)
(11)
Окисление Шиффовых оснований приводит к образованию карбонильных соединений, при низкой температуре может быть получены оксазиридины:
(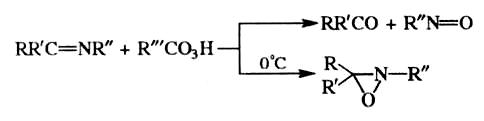 12)
12)
Шиффовы основания восстанавливаются до соответствующих аминов и при действии муравьиной кислоты. Полагают, что такого рода восстановление азометинов является ключевой стадией синтетически важного восстановительного алкилирования аммиака и аминов альдегидами и кетонами в присутствии муравьиной кислоты (реакции Лейкарта) или муравьиной кислоты в сочетании с формальдегидом (реакция Эшвайлера-Кларка). [5]
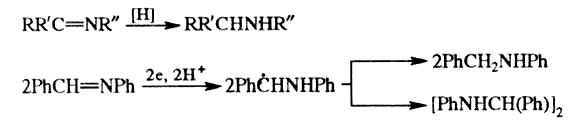
(13)
(14)
1.4. Применение
Шиффовы основания используют в органическом синтезе, главным образом для получения гетероциклических соединений и вторичных аминов; для защиты альдегидной группы, например, при циклизации терпенов; в аналитической химии - для идентификации альдегидов и первичных аминов. Основания Шиффа, известные как азометиновые красители, применяются для крашения ацетатного и синтетических волокон, а также используются в цветной фотографии для понижения светочувствительности фотографической эмульсии. [6]
2. Экспериментальная часть
2.1. Синтез 2-амино-6-метилбензтиозола с альдегидами ароматического ряда
Согласно методике, описанной выше (стр. 5) мы ставили синтезы 2-амино-6-метилбензтиозола с альдегидами ароматического ряда:
1) Синтез 2-(бензилиденамино)-6-метилбензтиозола.
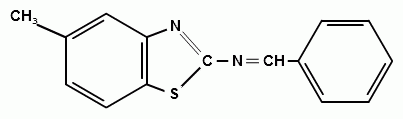
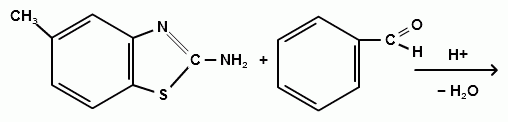
(15)
В колбу ёмкостью 50 мл к 0,13 г бензальдегида мы прибавляли 0,2 г 2-амино-6-метилбензтиозола. К получившейся смеси добавляли минимальный объем этилового спирта (95%) для полного её растворения (смеси необходимо хорошо перемешивать стеклянной палочкой), затем нагревали и охлаждали льдом. Кристаллизация начиналась через несколько минут, выпадал кристаллический осадок темно-жёлтого цвета (для очистки полученного соединения его перекристаллизовывали стр. 16), его отфильтровывали (на воронке Шотта) и сушили на воздухе. По результатам ИК – спектроскопии данный синтез прошел успешно.
Расчет выхода:
Молекулярная масса 2-амино-6-метилбензтиозола – 164 г/моль.
Молекулярная масса бензальдегида –106 г/моль.
Молекулярная масса 2-(бензилиденамино)-6-метилбензтиозола – 252 г/моль.
По
уравнению реакции (15) рассчитываем
избыток и недостаток исходных продуктов:

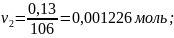
Получается, что 2-амино-6-метилбензтиозол в недостатке, по нему ведем расчет теоретического выхода продукта.
Выход в соответствии с уравнением реакции:
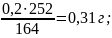
Практический выход 2-(бензилиденамино)-6-метилбензтиозола составил –0,12г. (38,19%)
2) Синтез 2-(4-нитробензилиденамино)-6-метилбензтиозола.
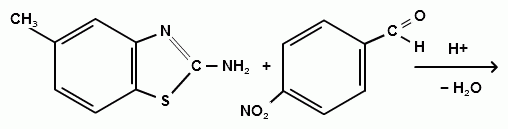
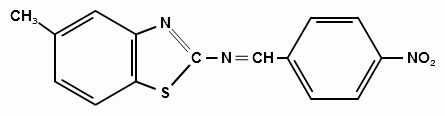
(16)
В колбу ёмкостью 50 мл к 0,18 г п-нитробензальдегида мы прибавляли 0,2 г 2-амино-6-метилбензтиозола. К получившейся смеси добавляли минимальный объем этилового спирта (95%) для полного её растворения (смеси необходимо хорошо перемешивать стеклянной палочкой), затем нагревали и охлаждали льдом. Кристаллизация начиналась через несколько минут, выпадал кристаллический осадок ярко-жёлтого цвета (для очистки полученного соединения его перекристаллизовывали стр. 16), его отфильтровывали (на воронке Шотта) и сушили на воздухе. По результатам ИК – спектроскопии данный синтез прошел успешно.
Расчет выхода:
Молекулярная масса п-нитробензальдегида –151 г/моль.
Молекулярная масса 2-(4-нитробензилиденамино)-6-метилбензтиозола – 297 г/моль.
По
уравнению реакции (16) рассчитываем
избыток и недостаток исходных продуктов:
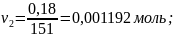
Получается, что п-нитробензальдегид в недостатке, по нему ведем расчет теоретического выхода продукта.
Выход в соответствии с уравнением реакции:
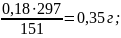
Практический выход 2-(4-нитробензилиденамино)-6-метилбензтиозола составил –0,18г. (51,43%)
3) Синтез 2-(4-хлорбензилиденамино)-6-метилбензтиозола.
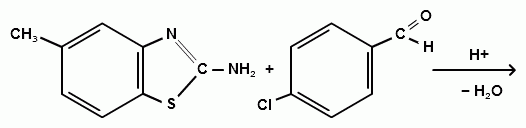
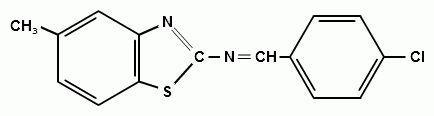
(17)
В колбу ёмкостью 50 мл к 0,17 г п-хлорбензальдегида мы прибавляли 0,2 г 2-амино-6-метилбензтиозола. К получившейся смеси добавляли минимальный объем этилового спирта (95%) для полного её растворения (смеси необходимо хорошо перемешивать стеклянной палочкой), затем нагревали и охлаждали льдом. Кристаллизация начиналась через несколько минут, выпадал кристаллический осадок бледно-лимонного цвета (для очистки полученного соединения его перекристаллизовывали стр. 16 ), его отфильтровывали (на воронке Шотта) и сушили на воздухе. По результатам ИК – спектроскопии данный синтез не прошел.
4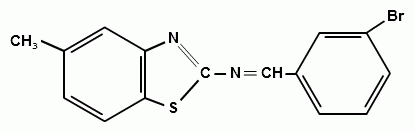 )
Синтез 2-(3-бромбензилиденамино)-6-метилбензтиозола.
)
Синтез 2-(3-бромбензилиденамино)-6-метилбензтиозола.

(18)
В колбу ёмкостью 50 мл к 0,30 г м-бромбензальдегида мы прибавляли 0,27 г 2-амино-6-метилбензтиозола. К получившейся смеси добавляли минимальный объем этилового спирта (95%) для полного её растворения (смеси необходимо хорошо перемешивать стеклянной палочкой), затем нагревали и охлаждали льдом. Кристаллизация начиналась через несколько минут, выпадал кристаллический осадок бледно-жёлтого цвета (для очистки полученного соединения его перекристаллизовывали стр. 16), его отфильтровывали (на воронке Шотта) и сушили на воздухе. По результатам ИК – спектроскопии данный синтез прошел успешно.
Расчет выхода:
Молекулярная масса м-бромбензальдегида –184,9 г/моль.
Молекулярная масса 2-(3-бромбензилиденамино)-6-метилбензтиозола – 330,9 г/моль.
По
уравнению реакции (18) рассчитываем
избыток и недостаток исходных продуктов:
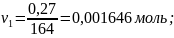
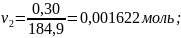
Получается, что м-бромбензальдегид в недостатке, по нему ведем расчет теоретического выхода продукта.
Выход в соответствии с уравнением реакции:

Практический выход 2-(3-бромбензилиденамино)-6-метилбензтиозола составил –0,28г. (51,85%)
5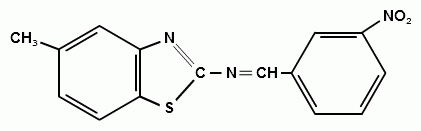 )
Синтез 2-(3-нитробензилиденамино)-6-метилбензтиозола.
)
Синтез 2-(3-нитробензилиденамино)-6-метилбензтиозола.
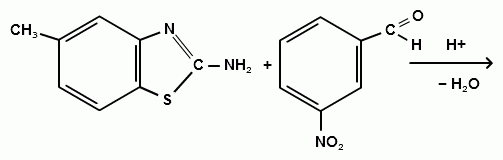
(19)
В колбу ёмкостью 50 мл к 0,18 г м-бромбензальдегида мы прибавляли 0,2 г 2-амино-6-метилбензтиозола. К получившейся смеси добавляли минимальный объем этилового спирта (95%) для полного её растворения (смеси необходимо хорошо перемешивать стеклянной палочкой), затем нагревали и охлаждали льдом. Кристаллизация начиналась через несколько минут, выпадал кристаллический осадок жёлтого цвета (для очистки полученного соединения его перекристаллизовывали стр. 16), его отфильтровывали (на воронке Шотта) и сушили на воздухе. По результатам ИК – спектроскопии данный синтез прошел успешно.
Расчет выхода:
Молекулярная масса м-нитробензальдегида –151 г/моль.
Молекулярная масса 2-(3-нитробензилиденамино)-6-метилбензтиозола – 297 г/моль.
По уравнению реакции (19) рассчитываем избыток и недостаток исходных продуктов:
Получается, что м-нитробензальдегид в недостатке, по нему ведем расчет теоретического выхода продукта.
Выход в соответствии с уравнением реакции:
Практический выход 2-(3-нитробензилиденамино)-6-метилбензтиозола составил –0,16г. (45,71%)
6) Синтез 2-(4-оксибензилиденамино)-6-метилбензтиозола.
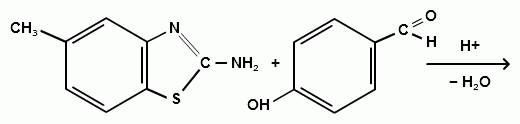
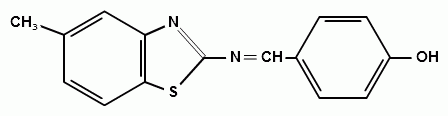
(20)
В колбу ёмкостью 50 мл к 0,15 г п-оксибензальдегида мы прибавляли 0,2 г 2-амино-6-метилбензтиозола. К получившейся смеси добавляли минимальный объем этилового спирта (95%) для полного её растворения (смеси необходимо хорошо перемешивать стеклянной палочкой), затем нагревали и охлаждали льдом. Кристаллизация начиналась через несколько минут, выпадал кристаллический осадок коричневого цвета (для очистки полученного соединения его перекристаллизовывали стр. 16), его отфильтровывали (на воронке Шотта) и сушили на воздухе. По результатам ИК – спектроскопии данный синтез прошел успешно.
Расчет выхода:
Молекулярная масса п-оксибензальдегида –122 г/моль.
Молекулярная масса 2-(4-оксибензилиденамино)-6-метилбензтиозола – 268 г/моль.
По
уравнению реакции (20) рассчитываем
избыток и недостаток исходных продуктов:
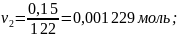
Получается, что 2-амино-6-метилбензтиозол в недостатке, по нему ведем расчет теоретического выхода продукта.
Выход в соответствии с уравнением реакции:
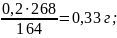
Практический выход 2-(4-оксибензилиденамино)-6-метилбензтиозола составил –0,2г. (60,61%)
7) Синтез 2-(тиофенамино)-6-метилбензтиозола.
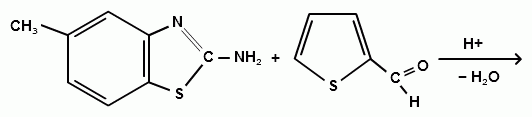
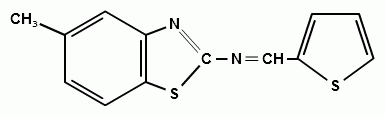
(21)
В колбу ёмкостью 50 мл к 0,22 г тиофенового альдегида мы прибавляли 0,3 г 2-амино-6-метилбензтиозола. К получившейся смеси добавляли минимальный объем этилового спирта (95%) для полного её растворения (смеси необходимо хорошо перемешивать стеклянной палочкой), затем нагревали и охлаждали льдом. Кристаллизация начиналась через несколько минут, выпадал кристаллический осадок коричнево-жёлтого цвета (для очистки полученного соединения его перекристаллизовывали стр. 16 ), его отфильтровывали (на воронке Шотта) и сушили на воздухе. По результатам ИК – спектроскопии данный синтез прошел успешно.
Расчет выхода:
Молекулярная масса тиофенового альдегида–112,06 г/моль.
Молекулярная масса 2-(тиофенамино)-6-метилбензтиозола – 240 г/моль.
По
уравнению реакции (20) рассчитываем
избыток и недостаток исходных продуктов:
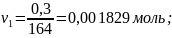
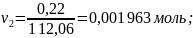
Получается, что 2-амино-6-метилбензтиозол в недостатке, по нему ведем расчет теоретического выхода продукта.
Выход в соответствии с уравнением реакции:
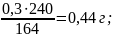
Практический выход 2-(4-оксибензилиденамино)-6-метилбензтиозола составил –0,19г. (43,18%)
