
- •Раздел 3
- •Занятие 27
- •1. Построение градуировочного графика
- •Цель занятия
- •1. Что из перечисленного не используется в атомно-абсорбционной спектроскопии?
- •2. Что из перечисленного ниже верно?
- •3. При измерении оптической плотности раствора аскорбиновой кислоты при 245 нм:
- •4. Ниже приведены спектры поглощения двух органических соединений. Какие из перечисленных утверждений, касающихся данных спектров, истинные?
- •1. Построение градуировочного графика
- •2. Определение массы этония в пробе
- •1. Построение градуировочного графика
- •2. Определение массы новокаина в пробе
- •Занятие 29
- •Цель занятия
- •1. Что из перечисленного используется в аэс?
- •2. Что из перечисленного верно?
- •9. Эффект Шпольского - это:
- •10. Флуориметрия является более чувствительным методом анализа, чем фотометрия, потому что:
- •1. Построение градуировочного графика
- •2. Определение массы рибофлавина в пробе
- •Занятие 30
- •Цель занятия
- •1. Что из перечисленного ниже верно?
- •9. Исправленное время удерживания вещества а составляет 150 секунд, а вещества b - 100 секунд. Коэффициент разделения веществ а и в равен:
- •10. Для двух компонентов анализируемой смеси величина rs равна 1,8. Что из перечисленного ниже верно?
- •Занятие 31
- •Цель занятия
- •Занятие 32
- •Цель занятия
- •1. Ниже приведены значения Rf для пяти компонентов анализируемой смеси. Пятно, соответствующее какому компоненту, будет находиться ближе всего к линии фронта растворителя?
- •2. Ниже приведены значения коэффициентов распределения для пяти компонентов анализируемой смеси. Пятно, соответствующее какому компоненту, будет находиться ближе всего к линии старта?
- •3. Найдите выражения, в которых имеются ошибки:
- •4. Двухмерная тсх отличается от одномерной тем, что:
- •Цель занятия
- •1. Настройка прибора и измерение рН раствора
- •2. Потенциометрическое титрование смеси фосфата и гидрофосфата натрия
- •Цель занятия
2. Потенциометрическое титрование смеси фосфата и гидрофосфата натрия
Потенциометрическое титрование смеси фосфата и гидрофосфата натрия раствором HCl основано на регистрации изменения рН раствора в процессе добавления титранта
Определение проводится по следующей методике. Точную навеску (около 0,2 г) препарата Na3PO412H2O, содержащего в качестве примеси некоторое количество Na2HPO4, растворяют в воде в мерной колбе вместимостью 100,0 мл и доводят водой до метки. Затем 20,0 мл приготовленного раствора переносят в стеклянный стаканчик, устанавливают на активатор магнитной мешалки. Вносят в раствор магнитную вертушку, включают магнитную мешалку и устанавливают оптимальную скорость вращения вертушки. Затем в раствор опускают электроды, и после установления равновесия считывают значение рН раствора с табло прибора. С помощью автоматической пипетки к титруемому раствору порциями по 0,10 мл прибавляют 0,1000 М HCl, фиксируя значение рН после добавления каждой порции титранта. Титрование продолжают до тех пор, пока не будет пройден второй скачок титрования. Результаты вносят в следующую таблицу:
V, мл |
V’, мл |
pH |
pH/V |
V/pH |
0,10 |
|
|
|
|
|
0,15 |
|
|
|
0,20 |
|
|
|
|
|
0,25 |
|
|
|
0,30 |
|
|
|
|
|
|
|
|
|
По полученным экспериментальным данным строят кривую титрования (зависимость рН от VHCl). Рассчитывают значения pH/V и строят график зависимости этого отношения от объёма добавленного титранта (первую производную кривой титрования). Объём титранта, относящийся к каждому значению pH/V, равен среднему арифметическому тех объёмов, для которых рассчитывалась данная величина pH.
Примерный вид кривой титрования и её первой производной показан на рис. 33.3.
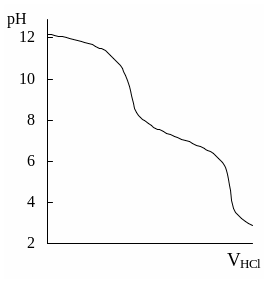
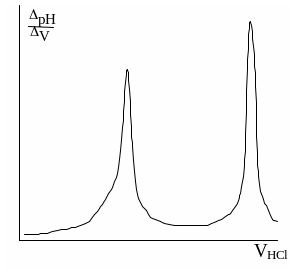
Рис. 33.3. Интегральная (слева) кривая потенциометрического титрования фосфата натрия и её первая производная (справа)
Кривая титрования имеет два скачка: первый соответствует превращению фосфата в гидрофосфат, а второй – гидрофосфата в дигидрофосфат. Для нахождения конечных точек титрования из кривой титрования для каждого скачка проводят две параллельные касательные к верхней и нижней пологим частям кривой и соединяют их прямой так, чтобы точка её пересечения с кривой титрования находилась в середине полученного отрезка. Конечным точкам титрования на дифференциальной кривой титрования соответствуют точки максимума пиков.
Рекомендуется также провести обнаружение конечных точек титрования методом Грана, для чего строят график зависимости V/pH от среднего объёма титранта. Конечным точкам титрования соответствуют точки пересечения полученных прямых (рис. 33.4).
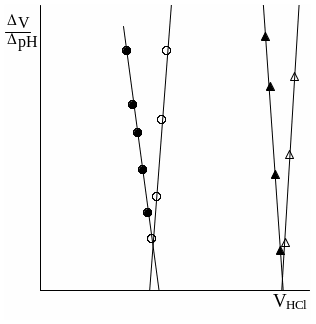
Рис. 33.4. Обнаружение конечной точки потенциометрического титрования фосфата натрия методом Грана
Массовые доли фосфата и гидрофосфата натрия в образце рассчитывают по следующим формулам:
![]()
![]()
где V1 – объём титранта (мл), добавленный для достижения первой конечной точки титрования, V2 – объём титранта (мл), добавленный для достижения второй конечной точки титрования.
ЗАНЯТИЯ 35
![]()
