
- •1. Электрохимия
- •1.1. Гальванические элементы
- •1.2. Механизм возникновения э.Д.С.
- •Определение величины электродного потенциала
- •2. Поверхностные явления и дисперсные системы
- •2.1. Поверхностные явления и адсорбция
- •Измерение поверхностного натяжения на границе раздела жидкость/жидкость
- •Обработка полученных результатов
- •2.2. Пены. Получение и свойства
- •2.3. Эмульсии и их свойства
- •2.4. Мицеллярные растворы iiab
- •2.5. Вязкость дисперсных систем.Структурная вязкость
- •2.6. Электрические свойства дисперсных систем
- •2.7. Седиментационный анализ суспензий и эмульсий
- •Практикум по курсу “Физическая и коллоидная химия”
- •Отдел оперативной полиграфии издательства *Нефть и газ"
- •11991 Гсп-1 Ленинский проспект, д.65
Определение величины электродного потенциала
а. Определение, величины электродного потенциала цинкового электрода.
Для определения электродного потенциала цинкового электрода составляют следующую гальваническую цепь:
(-)Zn|ZnSO4|| KClнасыщ.|| KCl, Hg2Cl2| Hg (+)
состоящую из цинкового и каломельного электродов. С помощью потенциометра Р-307 измеряют величину э.д.с. этой цепи. Потенциал цинкового электрода определяют из выражения:
![]() ,
,
где
![]() - электродный потенциал каломельного
электрода, который рассчитывается
для данной температуры по уравнению
- электродный потенциал каломельного
электрода, который рассчитывается
для данной температуры по уравнению
![]() В,
В,
![]() - электродный
потенциал цинкового электрода, Результаты
измерений и вычислений заносят в табл.
2.
- электродный
потенциал цинкового электрода, Результаты
измерений и вычислений заносят в табл.
2.
Таблица 2.
№ п/п |
Гальванический элемент |
Еизм, В |
|
|
|
1 |
(-)Zn|ZnSO4||KCl||KClнасыщ.||Hg2Cl2|Hg (+)
|
|
|
|
|
2 |
(-)Hg|Hg2Cl2, KCl|| KClнасыщ.||CuSO4| Cu (+) |
|
|
|
|
Б. Определение величины электролного потенциала медного электрода
Составляют цепь из медного и каломельного электродов:
(-)Hg | Hg2Cl2, KCl || KClнасыщ. || CuSO4 | Cu (+)
Медно-калсмельный элемент подключают к зажимам X1 или Х2 потенциометра Р-307 и определяют э.д.с. цепи Еизм, В. Электродный потенциал медного электрода раосчитывают по уравнению:
![]()
где - электродный потенциал медного электрода,
- электродный потенциал каломельного электрода. Полученные результаты заносят в табл. 2, представленную в разделе А.
По полученным величинам электродных потенциалов и вычисляют э.д.с. элемента Даниэля-Якоби. Э.д.с. элемента рассчитывают, вычитая из электродного потенциала положительного электрода электродный потенциал отрицательного. Э.д.с., рассчитанную по величине электродных потенциалов, сравнивают с непосредственно измеренной и рассчитанной по уравнению Нернста.
Потенциометрический метод измерения рН растворов
Для растворов слабых электролитов и растворов с малой концентрацией ионов водорода рН выражаот через концентрацию ионов H+:
pН = -lgCH+.
Потенциометрический метод определения рН растворов основан на измерении э.д.с. гальванического элемента, в котором потенциал одного из электродов зависит от концентрации ионов водорода. На этом методе основано действие различных лабораторных рН-метров. Многие рН-метры имеют две шкалы: в милливольтах и единицах рН.
Для измерения рН составляют гальванический элемент из индикаторного электрода, потенциал которого определяется концентрацией водородных ионов, и электрода сравнения с известные потенциалом.
В качестве индикаторных электродов применяются водородный, стеклянный, сурьмяный и некоторые другие. Электродами сравнения, как правило, являются каломельный или хлорсеребряный электроды.
Стеклянный электрод
Стеклянный электрод представляет собой стеклянную трубку, оканчивающуюся тонкостенным стеклянным шариком. Внутрь шарика. залит стандартный раствор с определенным значением рН, а в раствор погружен металлический электрод. Часто применяют 0,1 н раствор соляной кислоты и серебряный электрод, покрытый слоем хлорида серебра (рис. 9). Стеклянный электрод опускают в исследуемый раствор, рН которого требуется определить, и измеряют потенциал этого электрода относительно каломельного электрода сравнения. Общая схема химической цепи для определения рН при помощи стеклянного электрода имеет вид:
Pt| Аg | AgCl; 0,1н HCl | стекло | исследуемый р-р || КСl, Hg2Cl2| : Hg | Pt
Так как концентрация ионов водорода во внутреннем растворе сохраняется постоянной, уравнение Нернста для этой цепи может быть записано следующим образом:
,![]()
где
![]() -
стандартный
потенциал для данного стеклянного
электрода, определяемый калибровкой
электрода при помощи растворов с
известными значениями рН.
-
стандартный
потенциал для данного стеклянного
электрода, определяемый калибровкой
электрода при помощи растворов с
известными значениями рН.
Э
Рис.
3. Стеклянный
электрод:
1 - стеклянный
шарик со стандартным
раствором, 2 - серебряная
проволока, 3 - солевой
мостик, ведущий к стандартному
электроду сравнения,
4 -сосуд
с исследуемым раствором

Металлооксидные электроды
Эти электроды являются электродами второго рода. Такие электроды составляют из металла и насыщенного раствора труднорастворимого окисла (или гидроокиси) этого металла и электролита, содержащего ионы гидроксила. Для электрода данного вида можно использовать сурьму, висмут, вольфрам, молибден, серебро, ртуть, свинец и др. металлы, покрытые пленкой своего окисла или гидроокиси, которая трудно растворяется в исследуемом растворе. Наиболее изучены и чаще всего применяются сурьмяный и висмутовый электроды.
Сурьмяный электрод характеризуется следующей электродной реакцией:
Sb2O3 + 3 H2O + 6e 2Sb + 6 OH или
Sb(OH)3 + 3e Sb + 3OH.
При помощи сурьмяного электрода определяют рH растворов в пределах 1,0-12,0. Однако следует учитывать, что потенциал электрода при рH 59 неустойчив. Точность измерений составляет 0,20,3 pH. Сурьмяный электрод используют для определения рН растворов спиртов, аммиака; биологических жидкостей, почв, флотационных суспензий, растворов с примесями сульфидов и цианидов, Нельзя применять электрод для определения рН в растворах, содержащих легко адсорбируемые вещества, сильные окислители и вещества, образующие с сурьмой комплексные соединения.
Лабораторная работа 2. ОПРЕДЕЛЕНИЕ рН РАСТВОРА С ПОМОЩЬЮ СУРЬМЯНОГО ЭЛЕКТРОДА
Для определения рН раствора с помощью сурьмяного электрода собирают цепь, используя в качестве электрода сравнения каломельный электрод:
(-) Sb,Sb2O3 | исследуемый раствор || KClнасыщ.|| Hg2Cl2, KCl | Hg (+)
c неизвестным pH
Потенциал сурьмяного электрода является линейной функцией pH:
![]() .
.
Ход работы
1. Осторожно зачищают поверхность сурьмяного электрода наждачной бумагой, промывают дистиллированной водой и ополаскивают тем раствором, с которым будет проводиться измерение.
2. Для определения рН исследуемого раствора предварительно строят калибровочный график зависимости э.д.с. составленного элемента от рН раствора (рис. 10).
С
Рис. 10. Калибровочный
график зависимости э.д.с. от pH
раствора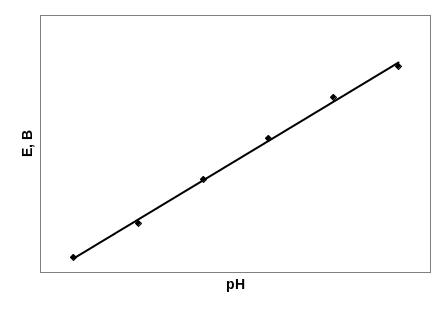
3, По полученным значениям э.д.с. строят график зависимости э.д.с. гальванического элемента от рH раствора,
4. Проводят измерение э.д.с. гальванического элемента, заполнив сурьмяный электрод раствором с неизвестным значением рH. Раствор получают у лаборанта, По измеренной величине э.д.с. с помощью калибровочного графика определяют рH исследованного раствора.
Результаты измерений сводят в таблицу 3.
Таблица 3.
Электрическая цепь |
рН р-ра |
Еизм, В |
(-) Sb,Sb2O3 | исследуемый раствор|| KClнасыщ.||Hg2Cl2,KCl|Hg (+) c неизвестным pH
|
|
|
Роль рН среды в нефтепромысловой практике
В нефтепромысловой практике широко применяется нагнетание воды в скважины для поддержания пластового давления в залежи, а также при вторичных методах добычи нефти. Основными требованиями, предъявляемыми к закачиваемой воде, являются стабильность и пассивность ее в отношении материла труб, то есть такие свойства, которые обеспечивают невыпадение твердых осадков при нагнетании воды в пласт и минимальное воздействие на арматуру.
Важным показателем, позволяющим оценивать качество воды для заводнения пластов, является концентрация водородных ионов. Так, например, карбонатное равновесие в воде есть функция рH. Только зная рН воды, можно при известном химическом составе ее судить о степени насыщенности воды той или иной малорастворимой солью и, следовательно, о возможности образования осадка и коррозионной активности.
Величина рН воды регулируется путем введения определенных количеств химических реагентов (кислоты, щелочи). Комбинирование рH-метра с дозаторами реагентов позволяет автоматизировать подготовку воды па нефтепромыслах.
Величина рН - важнейший показатель, определяющий рабочие качества глинистого раствора, используемого для бурения скважин. В частности рН определяет тиксотропные свойства глинистого бурового раствора.
На установках обезвоживания и обессоливания нефти иногда приходится измерять рH отделенной от нефти воды. Здесь величина рН показывает степень обессоливания нефти.
. рН-метрия используется также при изучении вопросов происхождения нефти.
