
- •И. В. Целинский, с.Ф.Мельникова теоретические основы электрофильного нитрования
- •1 Общие вопросы электрофильного нитрования
- •2 Электронное строение ароматических соединений
- •(Черным цветом обозначены отрицательные доли ао).
- •3 Эффекты заместителей в ряду ароматических углеводородов
- •4 Классификация заместителей
- •5 Стерические эффекты в электрофильном замещении
- •Нитровании толуола, близкое к структуре переходного состояния
- •6 Нитрующие системы. Минеральные кислоты
- •6.1 Нитрование в концентрированной и разбавленной водной азотной кислоте.
- •6.1.1 Состояние концентрированной hno3.
- •6.1.2 Состояние водных растворов hno3
- •6.1.3 Состояние азотной кислоты в растворах серной кислоты
- •6.2 Функции кислотности и развитие теории нитрования
- •7 Другие кислотные нитрующие смеси
- •7.1 Трансферное нитрование
- •7.2 Нитрование смесями hno3 с фторсульфоновой и трифторметансульфоновой кислотами
- •7.3 Нитрование на сульфированных полимерных смолах
- •7.4 Нитрование солями нитрония
- •7.4.1 Строение и реакционная способность нитроний-иона
- •8 Кинетика и механизм нитрования ароматических соединений
- •Ароматического замещения
- •8.1 Переходное состояние и селективность электрофильного ароматического замещения
- •8.2 Кинетика нитрования в гомогенных условиях
- •8.3 Кинетика нитрования в гетерогенных условиях
- •9 Ориентация электрофильного замещения и реакционная способность замещенных бензолов
- •9.1 Изомерные σ-комплексы. Ипсо-нитрование
- •Процесс носит название «деалкилирующего нитрования»
- •9.2 Ориентация как отражение свойств σ-комплекса
- •9.3 Факторы парциальных скоростей. Факторы селективности
- •9.4 Ориентация при наличии в кольце нескольких заместителей
- •9.5 Влияние сольватации и комплексообразования на региоселек- тивность нитрования
- •10 Нитрование через нитрозирование и побочные процессы при нитровании аренов
- •10.1 Нитрование через нитрозирование
- •Влияние азотистой кислоты на нитрование аренов нитроний-
- •10.3 Побочные процессы, сопровождающие нитрование
- •11 Нитрование оксидами азота
- •11.1 Нитрование азотным ангидридом
- •11.2 Нитрование тетраоксидом диазота, n2o4
- •Процессы одноэлектронного переноса в электрофильном ароматическом нитровании. Нитрование, катализируемое азотистой кислотой
- •Цеолитные и алюмосиликатные катализаторы.
- •12.2 Металлоксидные катализаторы
- •Катализаторы на основе твердых носителей, модифицирован- ных кислотами
- •Нитрование в ионных жидкостях
- •13 Особенности нитрования различных аренов
- •13.2 Динитронафталин и другие нитропроизводные нафталина
- •13.3 Нитропроизводные хлорбензола
- •13.5 Нитропроизводные ароматических аминов
- •Текст лекций Теоретические основы электрофильного нитрования
4 Классификация заместителей
В начале XX века голландский химик Голлеман разделил все заместители по ориентирующему влиянию на две большие группы. Ориентанты I рода ориентируют входящую группу преимущественно в орто- и пара-положения. Ориентанты II рода - преимущественно в мета-положение.
К![]() ориентантам I рода
относятся алкильные группы (-СR3),
функционально замещенные
метильные группы (-CH2Cl,
-CH2NH2,
-CH2OH,
-СH2COOH),
галогены (-F, –Cl,–Br,
–I), гидрокси-,
алкокси- и ацилоксигруппы (-OH,
-OR, -OCOR),
аминогруппа и замещенные амины (алкил-
и ациламины), азо-группа сульфанильная
и алкилсульфанильная группы (-SH
и –SR).
ориентантам I рода
относятся алкильные группы (-СR3),
функционально замещенные
метильные группы (-CH2Cl,
-CH2NH2,
-CH2OH,
-СH2COOH),
галогены (-F, –Cl,–Br,
–I), гидрокси-,
алкокси- и ацилоксигруппы (-OH,
-OR, -OCOR),
аминогруппа и замещенные амины (алкил-
и ациламины), азо-группа сульфанильная
и алкилсульфанильная группы (-SH
и –SR).
К ориентантам II рода относятся группы –SO3H, -SO2R, -NO, -NO2, -COOH, -COOR, -COR, -CHO, -COCl, -CONH2, - CN, -CF3,
![]()
Существуют и группировки атомов промежуточного характера, обуславливающие смешанную ориентацию
(-CH2NO2,-CH2F,-CHCl2, -CH2CH2NO2, -CH2CH2N+R3) и др.
Кинетическими методами было установлено, что все мета-ориентанты обладают дезактивирующим действием по сравнению с незамещенным бензолом. Например, нитробензол нитруется до динитробензола в 10 млн. раз медленнее бензола. Это обусловлено главным образом сильным –М -эф -фектом нитрогруппы.
Все ориентанты Голлемана I рода, за исключением галогенов, обладают активирующим влиянием по сравнению с водородом. Самый сильный эффект проявляют отрицательно заряженные оксид- и фенолят-ионы
![]()
Сильное активирующее влияние оказывают группы -NH2, -NR2, -OH, -OR, -SR.
Слабым активирующим влиянием обладают все алкильные группы. Галогены проявляют слабое дезактивирующее действие, но ориентируют в орто- и пара- положения. Это обусловлено тем, что галогены обладают противоположными по знаку индукционным (-I) и мезомерным (+М) эффектами (схема 4.1).
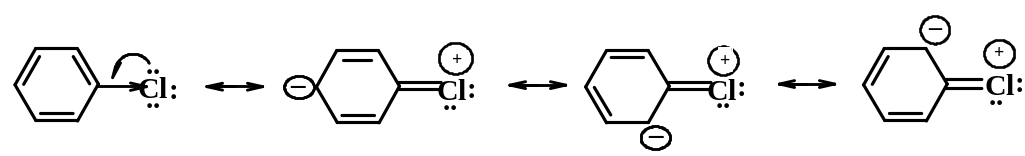
Схема 4.1
С учетом этого обстоятельства сейчас галогены выделяют в третью группу как дезактивирующие орто-пара-ориентанты.
5 Стерические эффекты в электрофильном замещении
Влияние электронных эффектов заместителей на реакционную способность ароматических соединений может быть изменено или даже исключено под влиянием пространственных, или стерических факторов, обусловленных взаимодействием непосредственно не связанных атомов и групп как внутри молекулы, так и вне ее при атаке молекулы субстрата реагентом.
Обычно стерические эффекты подразделяются на следующие типы:
1. Пространственные препятствия атаке реагента;
2. Пространственные препятствия сопряжению (характерны для ароматических и других плоских мезомерных структур);
3. Пространственные препятствия сольватации реагента, субстрата или переходного состояния (этот эффект не будет рассматриваться в данном курсе).
Первый тип стерического эффекта иллюстрируется изменением соотношения орто- и пара-изомеров при мононитровании алкилбензолов азотной кислотой в уксусном ангидриде (табл.1).
Таблица 1- Выход алкилнитробензолов при нитровании
алкилбензолов RC6H5
R |
Выход алкилнитробензолов |
||
орто- |
мета- |
пара- |
|
CH3 |
63 |
3 |
34 |
C2H5 |
48 |
5 |
47 |
CH(CH3)2 |
24 |
8 |
68 |
C(CH3)3 |
11 |
10 |
79 |
Как показано выше, все алкильные группы относятся к I группе заместителей (орто-пара-ориентанты) вследствие +I–эффекта и гиперконьюгации. Поэтому содержание мета-нитропроизводных мало и не превышает 12%. Однако соотношение орто/пара-нитропродуктов растет при увеличении объема заместителя в бензольном кольце.
Поскольку в алкилбензолах имеются 2 орто-положения и только одно пара-положение, в случае отсутствия пространственного эффекта содержание орто-нитропродукта должно вдвое превышать содержание пара-изомера. Учитывая все возрастающий объем заместителя при переходе от метильной к трет-бутильной группе, приведенный изомерный состав продуктов можно объяснить пространственным затруднением атаки реагентом (нитроний-ионом или его аналогом) орто-положений цикла (рис.6).
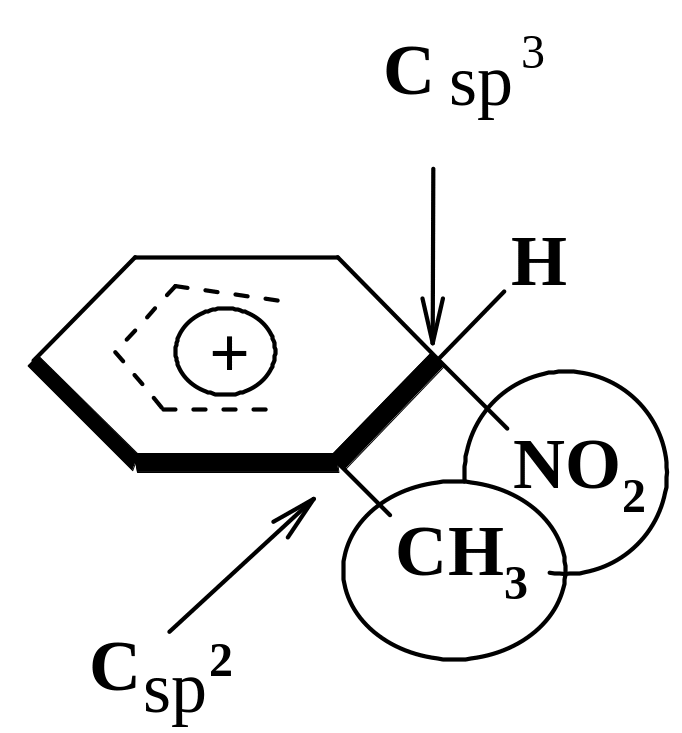
Рисунок 6. Примерное строение σ-комплекса при орто-
