
- •Практикум 3 біохімії для студентів технологічних спеціальностей
- •Частина і
- •Київ нухт 2003
- •1. Вуглеводи та ліпіди: властивості та кількісне визначення.
- •1.1. Йодометричний метод визначення глюкози.
- •1.2. Йодометричний метод визначення лактози.
- •1.3. Визначення крохмалю поляриметричним методом за Еверсом.
- •1.4. Визначення йодного числа.
- •1.5. Визначення кислотного числа.
- •2. Властивості амінокислот, методи їх кількісного визначення.
- •2.1. Визначення амінокислот методом тонкошарової хроматографії (тшх)/
- •2.2. Визначення азоту амінних груп методом формольного титрування
- •3. Властивості білків, методи їх кількісного визначення.
- •3.1. Ізоелектрична точка білків.
- •3.2. Кількісне визначення білка на основі біуретової реакції.
- •3.3. Осадження білків.
- •3.4. Визначення відновленого глутатіону.
- •Відновлена форма – Гл–sh
- •Окислена форма Гл–s–s–Гл
- •4. Якісне та кількісне визначення вітамінів.
- •4.1. Кількісне визначення каротинів.
- •4.2. Якісне визначення вітаміну д2 (ергокальциферолу).
- •4.3. Якісне визначення рибофлавіну.
- •4.4. Кількісне визначення вітаміну с у рослинній сировині.
- •4.5. Визначення вітаміну с в молоці.
- •5. Ферменти: специфічність та активність дії.
- •5.1. Визначення специфічності дії ферментів
- •5.2. Визначення залежності дії ферментів від температури і рН середовища
- •5.3. Вплив активаторів та інгібіторів на активність амілази.
- •5.4. Якісне визначення β-фруктофуранозидази.
- •5.5. Визначення амілолітичної активності.
- •Розрахунок амілолітичної активності (амілолітичної здатності – а3)
- •5.6. Визначення протеолітичної активності.
- •5.7. Визначення активності каталази (за о.М.Бахом та о.І.Опаріним).
- •5.8. Визначення активності пероксидази.
3.4. Визначення відновленого глутатіону.
Г лутатіон
один із найбільш поширених природних
пептидів, який знайдено майже у всіх
клітинах рослин, тварин, а також у
бактеріях і дріжджах. Він складається
з трьох амінокислот – глутамінової
кислоти, цистеїну і гліцину. Глутатіон
виконує роль коферменту в деяких реакціях
внутрішньо молекулярного перенесення
водню та ізомеризації; функціонально
активною групою є сульфгідрильна група
цистеїну. Відновлена форма глутатіону
(Гл – SH) легко окислюється, наприклад
молекулярним киснем у присутності
металів або йодом, утворюючи окислену
форму (Гл–S–S–Гл).
лутатіон
один із найбільш поширених природних
пептидів, який знайдено майже у всіх
клітинах рослин, тварин, а також у
бактеріях і дріжджах. Він складається
з трьох амінокислот – глутамінової
кислоти, цистеїну і гліцину. Глутатіон
виконує роль коферменту в деяких реакціях
внутрішньо молекулярного перенесення
водню та ізомеризації; функціонально
активною групою є сульфгідрильна група
цистеїну. Відновлена форма глутатіону
(Гл – SH) легко окислюється, наприклад
молекулярним киснем у присутності
металів або йодом, утворюючи окислену
форму (Гл–S–S–Гл).
Відновлена форма – Гл–sh
Окислена форма Гл–s–s–Гл
Окислення може відбуватися також ферментативно за участю глутатіондегідрогенази, а також, дегідроаскорбінової кислоти.
Глутатіон бере участь у багатьох фізіологічних процесах в організмі, йому належить велика роль а оборотних перетвореннях дисульфідних груп білків в сульфгідрильні. Зокрема, відновлена форма глутатіону підвищує активність тіолових ферментів, які містять в активному центрі сульфгідрильну групу. До тіолових ферментів належить протеолітичний фермент рослинного походження папаїн. Папаїн міститься у борошні, і підвищення його активності призводить до розпаду білків борошна і дріжджів, що знижує якість харчових продуктів. Для запобігання руйнування клейковини під впливом папаїну відновлений глутатіон окислюють, наприклад, (KBrO3) або дегідроаскорбіновою кислотою.
Мета роботи: засвоєння методу визначення відновленого глутатіону.
Завдання на виконання роботи: провести кількісне визначення відновленого глутатіону у борошні чи дріжджах.
Апаратура: лабораторна центрифуга, шутель-апарат, годинник.
Лабораторний посуд: мірні колби на 100 мл; мірні циліндри на 100 мл; піпетки на 5 мл; конічні колби на 100 мл; скляні палички.
Матеріали та реактиви: 1. 1 М розчин сульфосаліцилової кислоти; 2. 4%–й розчин сульфосаліцилової кислоти; 3. 0,005 н. розчин КJOз; 4. 0,001 н. розчин KJO3; 5. 5%–й розчин KJ; 6. 1%–й розчин крохмалю; 7. 5%-й розчин сульфату кадмію.
Принцип методу оснований на окисленні відновленого глутатіону йодом у кислому середовищі;
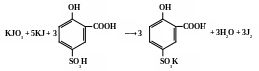
Хід роботи. У мірну колбу на 100 мл вносять 10 г дослідного матеріалу (борошно або дріжджі). Поступово, перемішуючи, доливають 80 мл дистильованої води. Колбу з сумішшю поміщають на шутель–апарат і перемішують протягом 10 хв. Потім, повільно перемішуючи, додають 5 мл 1 М розчину сульфосаліцилової кислоти, залишають на 30 хв., після цього доводять водою до мітки і знову інтенсивно перемішують. Суміш переносять у центрифужні пробірки і центрифугують. У центрифугаті визначають загальну кількість SH–груп, перераховуючи на відновлений глутатіон.
У конічну колбу на 100–150 мл піпеткою вносять 25 мл центрифугату (що відповідає 2,5 г наважки), додають 25 мл дистильованої води і, перемішуючи,вносять по 2,5 мл 4%–го розчину сульфосаліцилової кислоти і 5%–го розчину KІ. Додають 10 краплин 1%–го розчину крохмалю і титрують 0,001 н. розчином KІO3 до появи синього забарвлення. Для контролю чистоти реактивів в аналогічних умовах титрують 50 мл дистильованої води.
Розрахунок кількості сульфгідрильних сполук у перерахунку на відновлений глутатіон проводять за формулою;
![]() ,
,
де А – кількість сульфгідрильних сполук, мг%; a і b – об’єми 0,001 н. розчину KJO3 , які пішли на титрування, відповідно до проби і контролю, мл; 12,28 – коефіцієнт перерахунку на відновлений глутатіон.
Для визначення кількості відновленого глутатіону піпеткою Мора відбирають 50 мл центрифугату (5 г не важки) в мірну колбу на 100 мл. Додають 40 мл 5%-го розчину сульфату кадмію і 4 мл 1 н. розчину гідроксиду натрію. Суміш ретельно перемішують, доводять дистильованою водою до мітки і залишають стояти протягом 30 хв. Потім суміш центрифугують,
У конічну колбу на 100–150 мл вносять 50 мл центрифугату (2,5 г наважки) і визначають кількість SH –сполук, що залишилися в розчині, за допомогою описаної вище методики;
![]() ,
,
де B – кількість SH–сполук, мг%; a1, і b1 – об'єми 0,001 н. розчину KJO3, які пішли на титрування, відповідно до проби і контролю, мл.
Кількість відновленого глутатіону в наважці визначають за різницею між загальною кількістю сульфгідрильних сполук і кількістю, що залишилась після осадження відновленого глутатіону сульфатом кадмію:
![]()
