
- •Конспект лекций для подготовки по направлению
- •220700 Автоматизация технологических процессов и производств
- •1. Введение
- •2.2. Горение оксида углерода(II) и водорода
- •2.4. Горение твердого углерода
- •3. Диссоциация и образование химических соединений
- •Рассмотрим вопрос на примере диссоциации оксида Ме(II) по реакции
- •В качестве примера рассмотрим влияние плавления Ме и МеО на упругость диссоциации МеО.
- •3.3. Диссоциация оксидов и сульфидов, образующих растворы
- •Из выражения (18) находим , проводим преобразования полученной зависимости с учетом закона Генри и ее анализ.
- •3.4. Механизм и кинетика диссоциации соединений
- •4.1. Окисление твердых сульфидов Термодинамика процесса
- •Кинетика окисления твердых сульфидов
- •4.2. Взаимодействие сульфидов с оксидами
- •5. Процессы восстановления оксидов металлов
- •5.1. Газовое восстановление свободных оксидов нелетучих металлов
- •5.2. Газовое восстановление оксида летучего металла
- •5.3. Газовое восстановление оксида металла из расплава
- •6. Металлургические расплавы
- •7. Потери цветных металлов со шлаками
- •7.1. Электрохимические потери
- •7.2. Механические потери цветных металлов со шлаками
- •8. Процессы, основанные на ликвации, испарении и конденсации
- •8.1. Ликвационные процессы
- •8.2. Процессы, основанные на испарении и конденсации
- •9. Выщелачивание
- •10.1. Основы экстракционных процессов
- •10.2. Основы ионообменных процессов
- •10.3. Выделение металлов из растворов в виде труднорастворимых соединений
- •10.4. Выделение металлов из водных растворов водородом.
- •10.5. Выделение металлов цементацией
- •10.6. Основы процессов кристаллизации из растворов
- •11. Электролиз водных растворов
- •Рекомендательный библиографический список
- •Содержание
7. Потери цветных металлов со шлаками
По современным представлениям о формах нахождения цветных металлов в промышленных шлаках можно выделить два вида потерь металлов со шлаками:
электрохимические потери, обусловленные ошлакованием оксидов цветных металлов и некоторым растворением некоторой части в шлаке сульфидов или металлов;
механические потери, обусловленные механическим запутыванием в шлаке взвешенных мельчайших капель сульфидов или металлов.
7.1. Электрохимические потери
Переход металла или сульфида при соприкосновении двух жидких фаз: штейна (или металла) и шлака может иметь место в следующих случаях:
1. Металл или сульфид переходят в шлаковый расплав в форме незаряженных атомов или молекул:
![]() (41)
(41)
2. Из чернового металла или штейна в шлак переходят одновременно катионы и анионы, например, по реакциям:
![]() (42)
(42)
![]() (43)
(43)
3. При обменной реакции между катионами штейновой или металлической и шлаковой фазы. Например. По реакциям:
![]() (44)
(44)
![]() (45)
(45)
4. В случае перезарядки поливалентных ионов шлаковой фазы. Примеры реакций:
![]() (46)
(46)
![]() (47)
(47)
Me – цветной металл.
Если рассматривать переход цветного металла в шлак по реакциям (44-47), то записав константы равновесия этих реакций, можно затем рассмотреть факторы, от которых зависит содержание цветных металлов в шлаковой фазе.
Константы равновесия реакций (44-47):
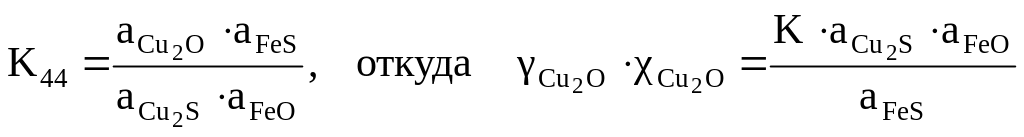 (48)
(48)
![]() (49)
(49)
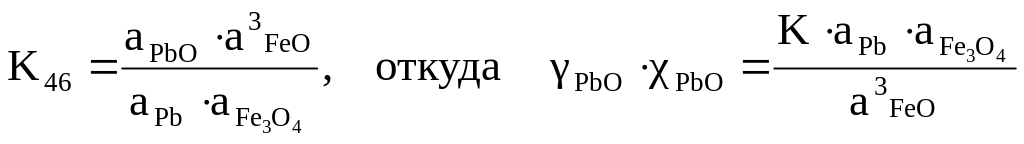 (50)
(50)
Уравнения
(48-50) показывают, что равновесные
содержания ()
металлов, растворенных в шлаке в форме
катиона МеZ+
при заданной температуре будут зависеть
от состава шлаковой фазы (![]() ,
,
![]() и др.) и от состава штейновой или
металлической фазы (
и др.) и от состава штейновой или
металлической фазы (![]() ).
Активности оксидов металлов связаны с
).
Активности оксидов металлов связаны с
![]() газовой фазы, а активности сульфидов
металлов с
газовой фазы, а активности сульфидов
металлов с
![]() (или
(или
![]() ).
).
В итоге можно заключить, что величина растворимости цветных металлов (электрохимических потерь) подчиняется сложной нелинейной зависимости:
![]() (51)
(51)
Привести данные А.В. Ванюкова и В.Я. Зайцева о соотношении электрохимических и механических потерь металлов в шлаках некоторых процессов из металлургического производства тяжелых цветных металлов.
7.2. Механические потери цветных металлов со шлаками
Механические потери представлены каплями штейна или металла различной крупности, которые не успели выделиться из шлаковой фазы в донную (штейн или шлак) за время пребывания расплавов в металлургическом агрегате.
Основная масса капель имеет размеры 10-100 мкм (0,01-0,1 мм).
Верхний предел капель штейна или металла (100 мкм) может быть рассчитан на основании формулы Стокса с поправками Адамара и Рыбчинского для случая осаждения жидких капель в жидкости:
![]() (52)
(52)
где: V- скорость осаждения капли, м/с;
g- ускорение силы тяжести, м/с2 (9,81);
1 и 2- соответственно плотность более тяжелой и более легкой жидкости, кг/м3;
1 и 2- соответственно вязкость более тяжелой и менее тяжелой жидкости, Пас;
r- радиус осаждающейся капли, м.
Нижний предел крупности (0,5 мкм) штейновых или металлических капель в шлаке определяется устойчивостью мелких капель. Мелкие капли характеризуются большой избыточной поверхностной энергией, а потому и большей растворимостью. Вследствие этого в шлаковой среде должна осуществляться изотермическая перегонка вещества от мелких капель к крупным, из-за чего очень мелкие капли быстро исчезают.
Закономерности такого переноса вещества вытекают из известного в физике закона Гиббса-Томсона:
![]() (53)
(53)
где: С1-пересыщенная концентрация компонента дисперсной фазы у поверхности капли радиуса r;
С2- насыщенная концентрация этого же компонента в объеме дисперсионной среды;
М- молекулярная масса дисперсной среды;
- межфазное натяжение на границе дисперсной фазы (штейн, металл) и дисперсионной среды (шлак);
- плотность дисперсной фазы (штейна, металла).
Из формулы (53) видно, что чем меньше r, тем больше С1/С2 при прочих равных условиях и тем больше скорость переноса вещества от мелких капель к крупным.
