
- •3. Основные понятия о реакционной способности органических молекул
- •1. Концепция теории мезомерии.
- •2. Концепция теории резонанса (Полинг, 1928 г.).
- •3. Делокализованное π-облако изображается пунктиром (в цикле – сплошной линией).
- •4. Классификация химических реакций и промежуточных частиц
- •Стабилизация интермедиатов.
- •Примеры построения названий по систематической номенклатуре
- •7. Кислотные и основные свойства органических соединений
- •Кислотные и основные функции веществ
- •Кислотность и основность по Бренстеду-Лоури.
- •Примеры.
- •Кислотность спиртов.
- •Сольватация аминов.
- •Кислоты и основания Льюиса.
- •Жесткие и мягкие кислоты и основания по Пирсону (жмко).
- •8. Углеводороды
- •8.1 Алканы
- •5. Воздействие анаэробных бактерий на растительные остатки:
- •6.1 Гидролиз карбидов:
- •7.1 Гидрирование алкенов:
- •7.2 Гидрирование алкадиенов:
- •7.3 Гидрирование алкинов:
- •1. Реакции замещения атомов водорода при взаимодействии с активными радикалами.
- •1.1.1 Фтор:
- •1.1.3 Бром:
1. Реакции замещения атомов водорода при взаимодействии с активными радикалами.
1.1 Галогенирование. Алканы вступают в реакцию со всеми галогенами, скорость реакции галогенирования снижается в ряду:
F > Cl > Br > I
1.1.1 Фтор:
СН4
+ 4F2
![]() СF4
+ 4HF
СF4
+ 4HF
1.1.2 Хлор (катализатор – сера, йод, хлориды олова, меди, сурьмы, алюминия):
СН4
+ Cl2
![]() СH3Cl
+ HCl
СH3Cl
+ HCl
1.1.3 Бром:
СН4
+ Br2
![]() СH3Br
+ HBr
СH3Br
+ HBr
1.1.4 Фотохимическое иодирование не удается осуществить вследствие низкой реакционной способности радикала иода.
Механизм реакции галогенирования (SR):
а) инициирование цепи реакции:
Hal2![]() 2Hal•
2Hal•
б) рост цепи:
R–H
+ Hal•![]() R•
+ HHal
R•
+ HHal
R•
+ Hal2
![]() R–Hal + Hal•
R–Hal + Hal•
в) обрыв цепи:
2Hal•
![]() Hal2
Hal2
R•
+ R•
![]() R–R
R–R
R•
+ Hal•![]() R–Hal
R–Hal
Наличие в углеводородной цепи различных углеродных атомов может приводить к образованию различных изомеров. При низких температурах реакция проходит избирательно, которая зависит от двух причин:
легкость отщепления водорода от углеродного атома, которая изменяется в ряду третичный > вторичный > первичный;
различная устойчивость алкильных радикалов.
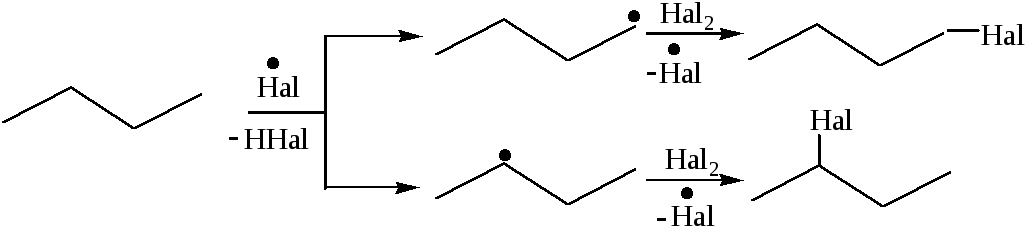
Образующиеся радикалы обладают различной устойчивостью, которая уменьшается в ряду:
третичный > вторичный > первичный > СH3•
Стабильность радикалов определяется делокализацией неспаренных электронов, которая осуществляется за счет сверхсопряжения с С–Н связями. Чем больше таких связей, тем эффективнее делокализация и, следовательно, устойчивее радикал.
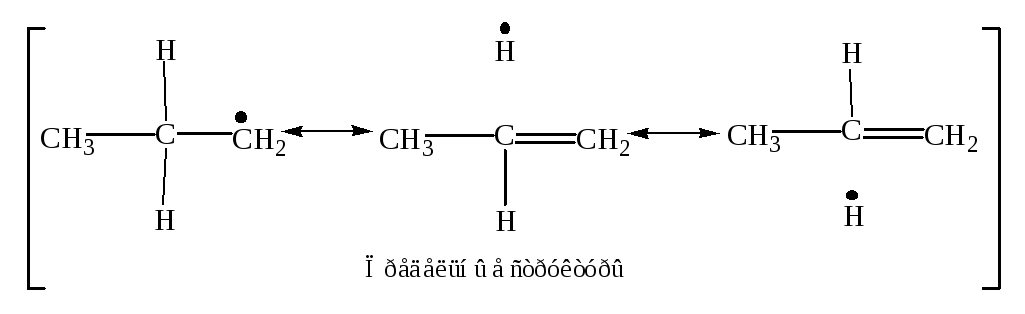
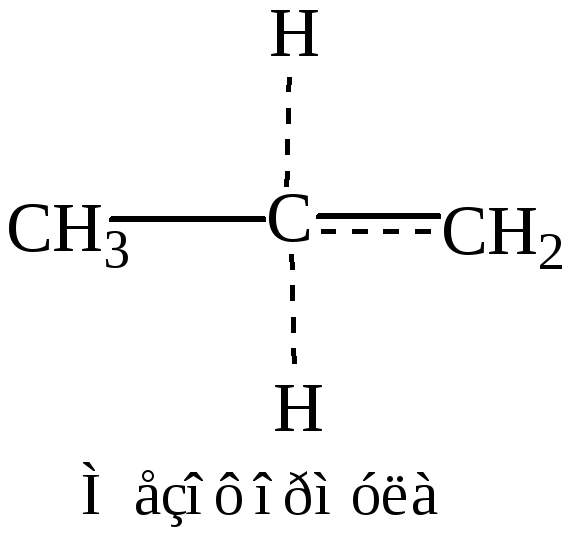
Делокализация неспаренного электрона у вторичного атома осуществляется между шестью атомами водорода и одним углеродным атомом.

Устойчивость радикалов определяет направление реакции и реакционную способность во многих реакциях, в которых образуются свободные радикалы.
При высоких температурах соотношение продуктов реакции определяется активностью радикальных частиц, которые эффективно преодолевают энергетический барьер разрыва при сближении с любым атомом водорода. Поэтому, на первый план выступает общая частота столкновений и ориентация молекул.
Процесс хлорирования в присутствии катализаторов, например, хлоридов некоторых металлов, может иметь ионный цепной характер:
Сl:Cl
+ AlCl3
![]() AlCl4–
+ Cl+
AlCl4–
+ Cl+
Cl+
+
H–СН3
![]() HCl + СН3+
HCl + СН3+
СН3+
+ Сl:Cl
![]() Сl:
СН3
+ Cl+
Сl:
СН3
+ Cl+
1.2 Сульфохлорирование и сульфоокисление.:
R–H +
H2SO4
(дымящая)
![]() R – SO3H
+ H2O
R – SO3H
+ H2O
R–H + SO2
+ Cl2
![]() R–SO2Cl
+ HCl
R–SO2Cl
+ HCl
R
– H
+ SO2
+ O2
![]() R
– SO3H
R
– SO3H
Соли сульфокислот имеют широкое практическое значение – это анионные ПАВ, моющие средства, эмульгаторы, флотореагенты, присадки к техническим маслам, ингибиторы коррозии.
1.3 Нитрование. В зависимости от условий протекания различают:
жидкофазное нитрование (7 – 20% азотная кислота, нормальное давление и температура 110 – 140оС), реакция Коновалова (1888 г.):
R–H +
HNO3
![]() R–NO2
+ H2O
R–NO2
+ H2O
парофазное нитрование (оксидами азота при давлении 2 – 4,5 МПа, температура 150 – 220оС в присутствии кислорода), реакция Титова:
R–CH2–R
+ HNO3
![]() R–NO2
+ R–CH2–NO2
+ H2O
R–NO2
+ R–CH2–NO2
+ H2O
Азотная кислота действует как окислитель, а радикал нитрозония амбидентен, поэтому могут образовываться эфиры азотистой кислоты наряду с нитросоединениями, а так же спирты, карбонильные соединения и карбоновые кислоты.
2. Окисление. В присутствии большого избытка кислорода (воздуха) или окислителей (K2CrO4, K2Cr2O7) при высоких температурах алканы сгорают до воды и углекислого газа:
R–H
+ O2
![]() СO2
+ H2O
СO2
+ H2O
При ограниченном доступе кислорода возможно образование продуктов неполного сгорания предельных углеводородов:
R–H
+ O2
![]() СO
+ H2O
СO
+ H2O
R–H
+ O2
![]() С + H2O
С + H2O
В определенных условиях возможно проведение контролируемого окисления при котором происходит расщепление связей С–С при неполном окислении атомов углерода:
Парофазное окисление используется для получения высших жирных карбоновых кислот. Катализатор – ацетат марганца, температура 150 оС:
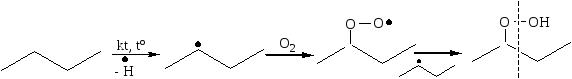
Жидкофазное окисление (А.Н. Башкиров, 1959 г.) в присутствии катализатора, например соединений марганца и температуре 200 оС:
СnН2n+2.![]() СnН2n+1ОН
СnН2n+1ОН
Твердофазное окисление (окислительная деструкция) характерна для старения олефинов под действием атмосферного кислорода, инициированная облучением, перекисью, нагреванием:
R–R
![]() 2R•
2R•
R•
+ O=O
![]() R–O–O•
R–O–O•
R–O–O•
+ R–H
![]() R–O–O–H +R•
R–O–O–H +R•
R–O–O–H
![]() R–O•
+ •O–H
R–O•
+ •O–H
R–O•
+ R–H
![]() R–OH +R•
R–OH +R•
R–O•
+ 2R–H
![]() H2O
+ 3R•
H2O
+ 3R•
3. Термические превращения алканов. Различают следующие процессы:
3.1 Пиролиз (от гр. pyr – огонь, lysis – распад, разложение). Включает разложение и деструктивные превращения высокомолекулярных алканов при температурах выше 600 оС:
2СН4
![]() СН2=
СН2
+ 2Н2
СН2=
СН2
+ 2Н2
2СН4
![]() СН≡СН + 3Н2
СН≡СН + 3Н2
СН4
![]() С + 2Н2
С + 2Н2
3.2 Крекинг (от англ. cracking – расщепление) в отличие от пиролиза протекает при более низких температурах до 600 оС (В.Г. Шухов и С. Гаврилов, 1890 г.) Существует несколько видов крекинга, наиболее известны:
термический крекинг;
каталитический крекинг.
Термический крекинг протекает в основном по цепному радикальному механизму с разрывом С–С и С–Н связей. Так как концентрация радикалов небольшая, основными являются процессы диспропорционирования и β-распада, при температуре 300–350 оС, но наиболее оптимальными являются температуры 450–600 оС.
Каталитический крекинг обеспечивает глубокую переработку нефти при температурах 450–520 оС, катализаторы – алюмосиликаты (Э. Гудри, 1936 г.). Проходят процессы изомеризации, деалкилирования, циклизации и др.
1.5.3. Риформинг (Н.Д. Зелинский, 1902 г.). Катализатор – платина и палладий, алюмоплатиновые, би- и полиметаллические. Основные процессы дегидрогенизация с образованием ароматических соединений.
Широкое распространение получили два варианта риформинга гидроформинг (гидрокрекинг) и платформинг. Основной целью риформинга является получение высококачественных бензина и керосина.
Гидроформинг (350–450 °С, 3–14 МПа, катализатор – оксиды и сульфиды Мо, Ni на алюмосиликатах). Применение водорода обеспечивает гидрирование на катализаторе высокомолекулярных и сернистых соединений с последующим их распадом, гидрирование алкенов.
Платформинг – каталитический крекинг, осуществляемый с помощью палладия, платины (менее 1%) на оксиде алюминия и алюмосиликатах. Основные процессы изомеризация, дегидроциклизация, ароматизация.
Термические некаталитические и каталитические превращения алканов осуществляются по следующей схеме:
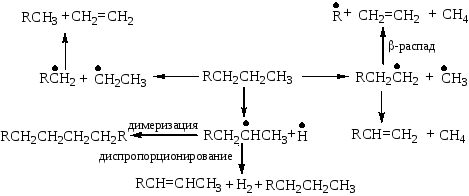
Применение алканов. Алканы являются не только простым и относительно дешевым топливом, но и исходным сырьем для крупнотоннажного производства. Промышленное использование алканов можно иллюстрировать на примере превращений метана:
4СН4
![]() СН2=
СН2
+ СН≡СН + 5Н2
СН2=
СН2
+ СН≡СН + 5Н2
СН4
![]() HCN
HCN
![]() СН2=СН–CN
СН2=СН–CN
![]() синт.
волокно нитрон, натур. каучук
синт.
волокно нитрон, натур. каучук
СН4
![]() CН3NО2
CН3NО2
![]() NО2С(CН2ОН)3
NО2С(CН2ОН)3
![]() взрывчатые вещества
взрывчатые вещества
СН4
![]() СО
+ H2
СО
+ H2
![]() CН3ОН
CН3ОН
![]() CН2О
CН2О
![]() пластмассы
пластмассы
СН4
![]() С + H2
(сажа, резиновая промышленность)
С + H2
(сажа, резиновая промышленность)
![]() NH3
NH3
СН4
![]() СH2Cl2
СH2Cl2
![]() (СH3)2SiCl2
(СH3)2SiCl2
![]() силиконы
силиконы
СН4
![]() СHCl3
(хлороформ)
СHCl3
(хлороформ)
![]() СCl4
СCl4
![]() ССl2F2
(фреон)
ССl2F2
(фреон)
Высшие жирные и твердые парафины используются как топливо (дизельное), смазочный материал, в виде твердого парафина, озокерита, а их производные, в виде солей карбоновых кислот, как моющие средства.
Экологическое послесловие. Загрязнение алканами атмосферы, почвы, водоемов, подземных вод в значительных масштабах происходит при добыче нефти, газа, транспортировке жидких и газообразных углеводородов, переработке, производстве, применении углеводородов.
Экология почвы. Наиболее крупными источниками загрязнения почвы углеводородами являются нефтеразведка, добыча, транспортировка нефти и нефтепродуктов, при их применении и хранении. Особую опасность представляют загрязнение и нарушение верхнего слоя почв северных территорий, что обусловлено очень медленной скоростью их естественного восстановления.
Экология водоемов, подземных вод. Основные источники загрязнения – добыча нефти, транспортировка нефти и нефтепродуктов, промышленные стоки, технологии очистки промышленных стоков, связанные с закачкой их в подземные горизонты.
Экология атмосферы. Основными источниками загрязнения атмосферы являются: выделение углекислого газа в результате сжигания углеводородов, поступление газообразных углеводородов в атмосферу при газо-, нефтедобыче, разрывах газопроводов, промышленных газообразных выбросах, испарениях при переработке, транспортировке, хранении, заполнении различных емкостей нефтью и нефтепродуктами, сушке лакокрасочных покрытий.
