
- •8.2 Алкены
- •3. Дегалогенирование вициальных дигалогеналканов:
- •5. Восстановление алкадиенов и алкинов:
- •7.2.4 Реакция Хека:
- •8. Реакции окисления.
- •10.1 Катионная полимеризация:
- •10.2 Анионная полимеризация:
- •10.3 Радикальная полимеризация:
- •8.3 Алкадиены
- •2. Получение алкадиенов-1,2 (аллены)
- •2.2.1 Присоединение галогенводорода:
- •2.2.2 Присоединение галогена:
- •2.2.3 Присоединение воды:
- •8.3.1 Каучук
- •8.3.2 Природные изопреноиды. Терпены
- •8.4 Алкины
- •4. Реакции отщепления.
- •1. Реакции присоединения.
- •1.1 Реакции электрофильного присоединения.
- •1.1.3 Гидрогалогенирование:
- •1.2 Реакции нуклеофильного присоединения:
- •2. Реакции окисления.
1. Реакции присоединения.
1.1 Реакции электрофильного присоединения.
1.1.1 Гидрирование (катализатор Ni, Pt, Pd):
![]()
1.1.2 Галогенирование. Присоединение галогенов по тройной связи протекает как анти-присоединение, реакция протекает медленнее, чем для алкенов за счет меньшей стабильности винильного катиона и более притянутого к ядрам атомов углерода π-молекулярного облака за счет повышенной электроотрицательности и, следовательно, труднее поляризуемого:
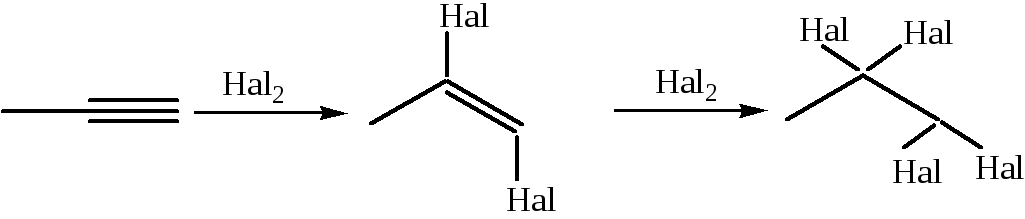
1.1.3 Гидрогалогенирование:
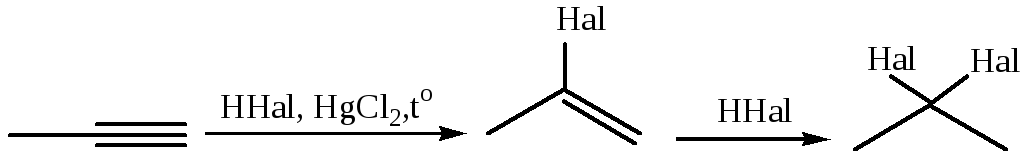
На второй стадии образуются геминальные дигалогеналканы:
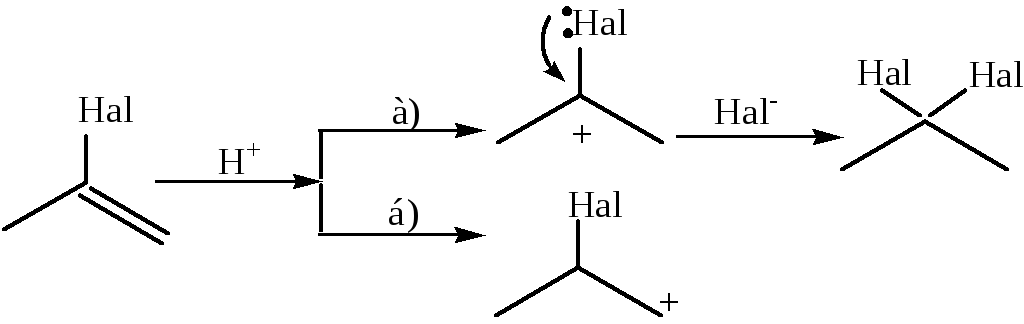
Дестабилизирующее влияние атома галогена в карбкатионе (а) ослаблено за счет +М-эффекта. Атом галогена своей НЭП р-электронов участвует в делокализации "+" заряда. Вследствие большей стабильности карбокатион (а) образуется быстрее и его взаимодействие с нуклеофилом приводит к получению геминального дигалогенпроизводного.
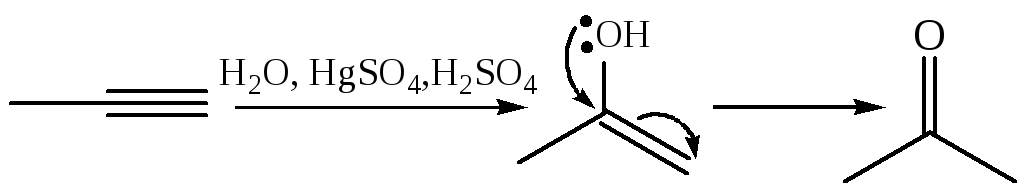
1.1.4 Гидратация (реакция М.Г. Кучерова, 1881 г.):
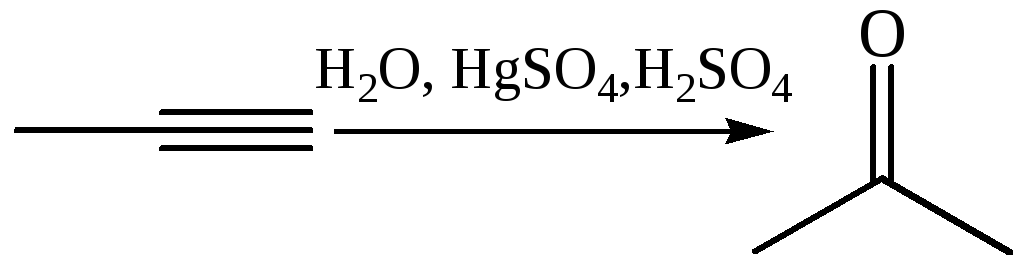
На первой стадии образуются енолы, которые перегруппировываются в карбонильные соединения (правило Эльтекова – Эленмеера). Перегруппировку обеспечивает эффект р,π-сопряжения, вследствии которого электронная плотность перемещается от кислорода к углеродному атому к которому направляется протон гидроксильной группы:
1.1.5 Присоединение Н – электрофилов (НХ, где Х= CN, SR, RCOO):
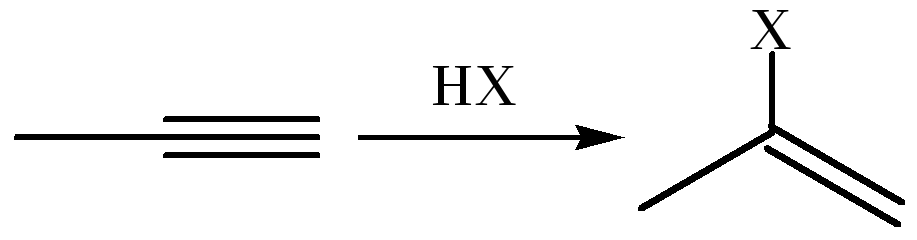
1.2 Реакции нуклеофильного присоединения:

Механизм реакции нуклеофильного присоединения (АN) состоит в том, что алкин атакует частица или молекула, в результате присоединения которой образуется карбоанион, который как сильное основание стабилизируется, отрывая подвижный протон от реагента:

1.3 Гидроборирование. Образующиеся при этом алкенилбораны обрабатывают уксусной кислотой при низкой температуре превращая их в алкены:

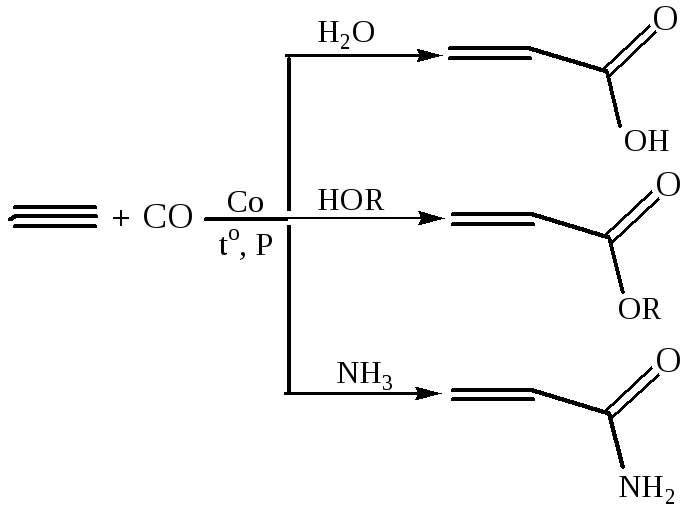
1.4. Карбонилирование (оксосинтез, гидроформилирование):
2. Реакции окисления.
2.1 Ацетиленовые углеводороды обесцвечивают щелочной раствор KMnO4 на холоду:
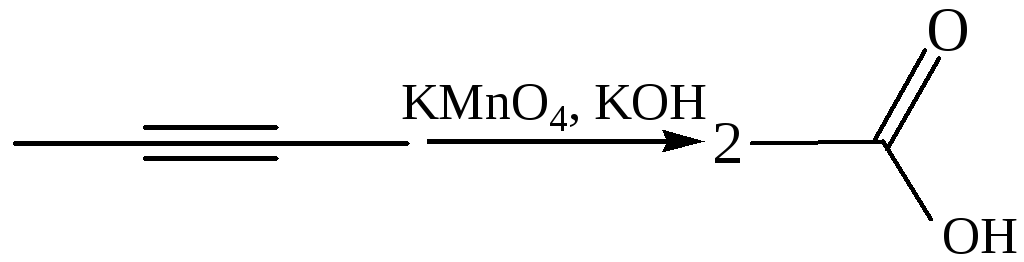
2.2 Реакция с озоном:
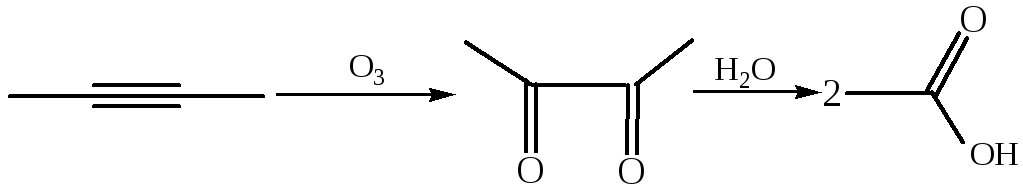
2.3 Жесткое окисление. Сильные окислители (КMnO4, K2Cr2O7, CrO3) в кислой среде расщепляют ацетиленовые углеводороды по тройной связи:

2.4 Реакция горения:
С2Н2
+ 2,5О2
![]() СО2
+ Н2О
СО2
+ Н2О
С2Н2
+ 1,5О2
![]() СО2
+ Н2О
+ С
СО2
+ Н2О
+ С
3. Реакции алкинов по терминальной связи. Согласно протолитической теории, под кислотностью понимают способность отдать протон. В алкинах, благодаря повышенной электроотрицательности sp-гибридного С-атома, терминальная связь обладает заметной полярностью. Поэтому в присутствии сильных оснований возможна ионизация терминальных алкинов с образованием ацетиленид-ионов и передачей протона основанию.
3.1 Образование ацетиленидов:
3.1.1
![]()
3.1.2
![]()
3.1.3
![]()
3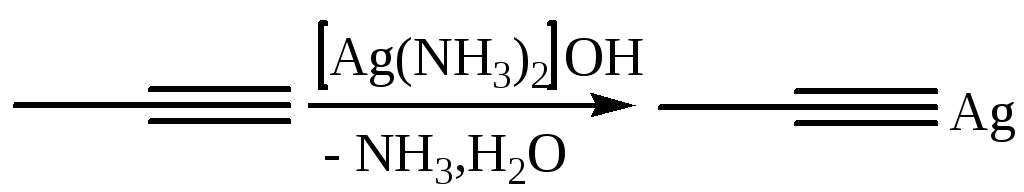 .1.4
.1.4
3.1.5
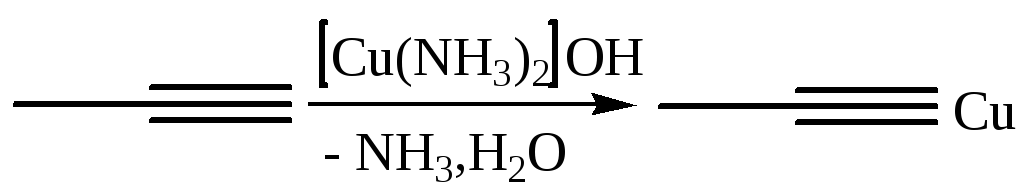
Ацетилениды являются активными нуклеофильными реагентами, их широко используют для введения тройной связи в молекулу:
![]()
3.1.6 Реакции конденсации. Синтез Репе (1949 г.):
![]()
3.1.7 Реакция конденсации. Реакция Фаворского (1905 г.):
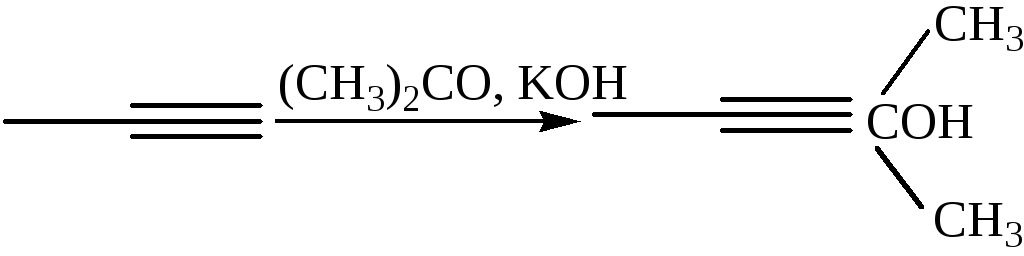
3.1.8 Реакция Саногашира:
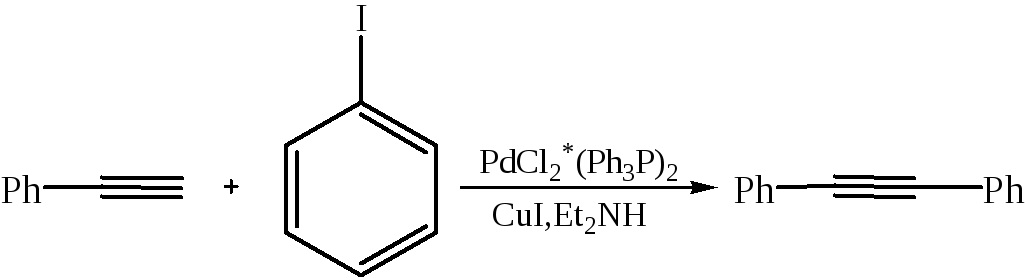
4. Реакции полимеризации.
4.1 Линейная полимеризация. В присутствии металлорганических соединений происходит полимеризация алкинов с образованием сопряженных полиенов:
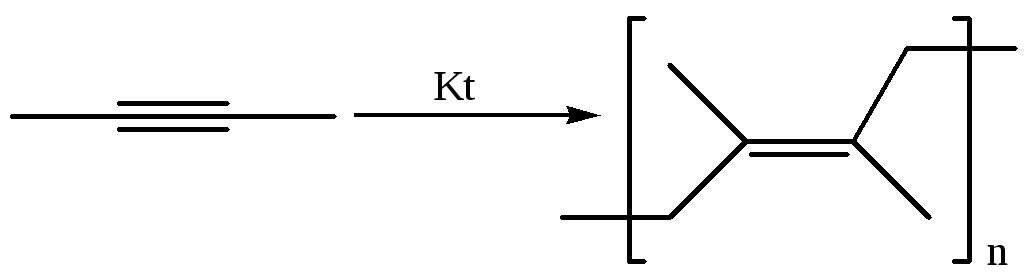
4.2 Линейная полимеризация ацетилена. В присутствии одновалентной меди и окислителя ацетилен образует полимер, состоящий только из атомов С (карбин, полиацетилен):
![]()
4.3 Линейная ди- и тримеризация ацетилена, проходит в присутствии одновалентной меди в кислой среде (реакция Ньюленда):
![]()
4.4 Циклическая олигомеризация (400–500оС, катализатор – активированный уголь, соединения Cr, Ni, Co, Н.Д. Зелинский, В.А. Казанский):
4.4.1
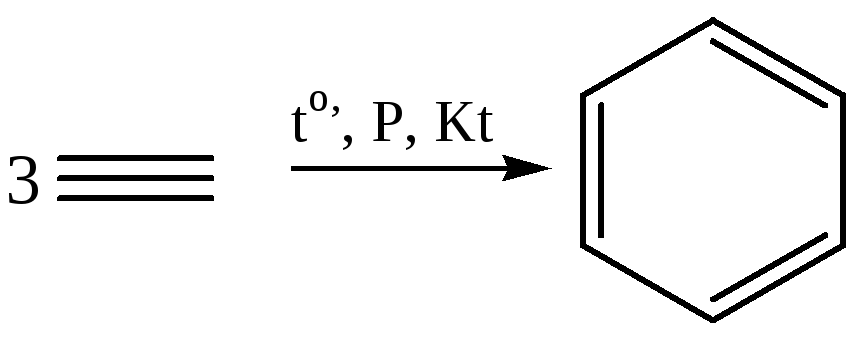
4.4.2
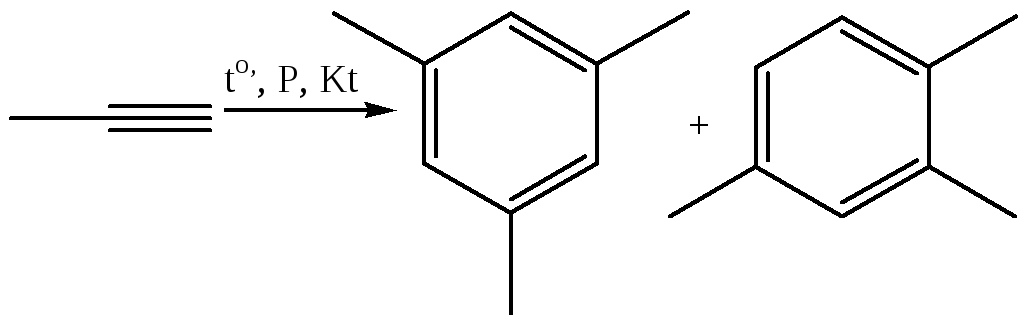
4.4.3 В растворе тетрагидрофурана, катализатор цианида никеля (В. Реппе, 1948 г.):

Применение алкинов. Ацетилен – соединение, дающее начало промышленному производству уксусного альдегида, а на его основе спирта и уксусной кислоты. Ацетилен важен в качестве исходного вещества для получения разнообразных мономеров:
НС≡СН
![]() СН2=СН–С≡СН
СН2=СН–С≡СН
![]() хлоропрен, каучуки
хлоропрен, каучуки
НС≡СН
![]() СН2=СНCl
СН2=СНCl
![]() поливинилхлорид,
перхлорвинил
поливинилхлорид,
перхлорвинил
НС≡СН
![]() СН2=СН–ОСОСН3
СН2=СН–ОСОСН3
![]() поливинилацетат
поливинилацетат
НС≡СН
![]() СН2=СН–CN
СН2=СН–CN
![]() полиакрилонитрил,
волокно (орлон, нитрон)
полиакрилонитрил,
волокно (орлон, нитрон)
Экологические аспекты. Антропогенными источниками поступления в окружающую среду являются как предприятия, принимающие алкины, например, при производстве синтетического каучука, уксусного альдегида, тетрахлорэтана, акрилонитрила, так и предприятия, их производящие.
В организм алкины поступают через легкие и оказывают наркотическое действие, которое нарастает с увеличением молекулярной массы соединения. Длительные контакты с ацетиленом в производственных условиях вызывают функциональные нарушения нервной системы. Его высокие концентрации при небольшом содержании кислорода приводят к потере сознания и отеку легких.
Экологические проблемы производства и использования углеводородов. В окружающей среде медленно, но непрерывно происходит увеличение концентрации летучих углеводородов, главным образом метана. Кроме того, как основной вид моторного топлива, а также как источник тепловой энергии углеводородное сырье при сжигании образует огромное количество углекислого газа, который выбрасывается в атмосферу. Нарушение теплового баланса («парниковый эффект») может привести к глобальным экологическим последствиям, одно из которых затопление низменных участков суши вследствие интенсивного таяния льда в Антарктиде, на Северном полюсе и ледников горных массивов.
Кроме непосредственного экологического загрязнения окружающей среды углеводородами, еще более серьезную опасность представляют токсические продукты, получаемые из углеводородов (галогено-производные, нитросоединения, органические цианиды).
