
- •8.5.2 Соединения ароматического ряда
- •8.5.2.1 Моноароматические соединения
- •1. Дегидроциклизация и дегидрогенизация парафинов:
- •2. Дегидрогенизация циклоалканов:
- •1.2 Алкилирование:
- •8.5.2.2 Полициклические арены с изолированными кольцами
- •2. Реакция Вюрца:
- •3. Димеризация бензола в присутствии солей Pd:
- •1.2 Реакция с амидом натрия:
- •1.3 Взаимодействие с щелочными металлами:
- •8.5.2.3 Полициклические арены с конденсиро-ванными кольцами
- •2. Циклизация ацетилена и бензола:
- •3. Дегидроциклизация алканов:
- •1.4 Окисление:
- •1.5 Гидрирование:
- •9. Реакционные центры и основные механизмы реакций углеводородов
- •1. Генерирование электрофильной частицы
- •3. Стабилизация карбкатиона
- •9.1 Особенности протекания некоторых реакций
- •2. Региоселективность реакций присоединения к несимметричным алкенам и алкинам реагентов типа н–х
- •Современная электронная интерпретация правила Марковникова.
- •4. Стереоспецифичность реакции гидроксилирования алкенов (реакция Вагнера)
- •5. Химические особенности сопряженных диенов
- •6. Влияние заместителей на реакционную способность и ориентацию в реакциях электрофильного замещения в бензольном кольце
- •Резонансные структуры карбкатиона (3)
- •Примеры
- •9.2 Оптическая спектроскопия
- •Уф – спектр ик – спектр
- •3. Ионизация
- •4. Природа растворителя
- •Примеры
- •Конспект лекций гомофункциональные углеводороды
- •Галогенопроизводные углеводородов
- •1.1 Галогенпроизводные алифатического ряда
- •1. Реакции замещения.
- •3.2.1 Реакции магнийорганических соединений
- •3.2.1.1 Взаимодействие с соединениями, имеющими подвижный атом водорода:
- •1.1. Получение алифатических аминов
- •6. Специальные методы
- •3. Взаимодействие аминов с азотистой кислотой
- •6.1.1 Реакция окисления первичных аминов:
- •6.1.2 Реакция окисления первичного ариламина гидропероксидом трифторацетила:
- •6.2 Реакция окисления вторичных аминов:
- •6.3.2 Ацилирование третичных аминов:
- •7. Реакции с электрофильными реагентами ароматических аминов
- •8. Реакции конденсации
- •8.3 Реакции конденсации третичных аминов:
- •2. Реакции ароматических солей диазония без выделения азота
- •3. Реакции диазоалканов
- •1. Желтого типа:
- •2. Сине-зеленого типа:
- •3. Фуксиново-красного типа:
3. Взаимодействие аминов с азотистой кислотой
3.1.1 Взаимодействие первичных ароматических аминов с азотистой кислотой приводит к образованию устойчивых солей диазония:

3.1.2 Взаимодействие первичных алкиламинов с азотистой кислотой:
![]()
3.2 Взаимодействия вторичных ароматических аминов и алкиламинов с азотистой кислотой. Вторичные амины при взаимодействии с азотистой кислотой образуют N-нитрозоамины. Нитрозирующим агентом выступает нитрозилхлорид.
3.2.1

Если ароматический нитрозоамин вводят в реакцию с раствором соляной кислоты в этиловом спирте, то нитрозогруппа мигрирует в пара-положение ароматического кольца. Эта реакция известна как перегруппировка Фишера–Хепа (1886 г):

3.2.2
![]()
3.3 Взаимодействие третичных ароматических аминов с азотистой кислотой. Реакция нитрозирования идет не по аминогруппе, а в ароматическое ядро как SE, в качестве продукта образуется С-нитрозосоединение:

3.3.1 Взаимодействие третичных алкиламинов с азотистой кислотой. Третичные алкиламины в сильнокислых средах практически не реагируют с азотистой кислотой, однако в слабокислых средах, когда аминогруппа не протонируется, третичные амины могут образовывать продукты присоединения:

4. Получение изоцианидов. При нагревании с небольшим количеством хлороформа и щелочи первичные амины превращаются в изоцианиды:
![]()
5. Взаимодействие с сероуглеродом. Первичные амины с сероуглеродом образуют N-замещенные дитиокарбаминовые кислоты, которые хлоридом ртути (II) переводятся в изотиоцианаты, а с избытком амина дают N,N-дизамещенные тиомочевины:

Для вторичных аминов реакция останавливается на стадии дитиокарбаминовых кислот:

Третичные амины не реагируют с сероуглеродом.
6. Реакция окисление аминов. Амины способны восстанавливать различные окислители, однако это свойство далеко не всегда практически реализуется, так как в ходе реакций окисления часто образуются сложные трудноразделимые смеси продуктов. В качестве окислителей применяют Н2О2, RCOOOH, КМПО4, МпО2, соли ртути, тетраацетат свинца и др.
6.1 Реакция окисления первичных и вторичных аминов.Для первичных и вторичных алкил- и ариламинов первоначальными продуктами окисления в мягких условиях являются N-оксиды аминов, которые перегруппировываются в производные гидроксиламина.
6.1.1 Реакция окисления первичных аминов:
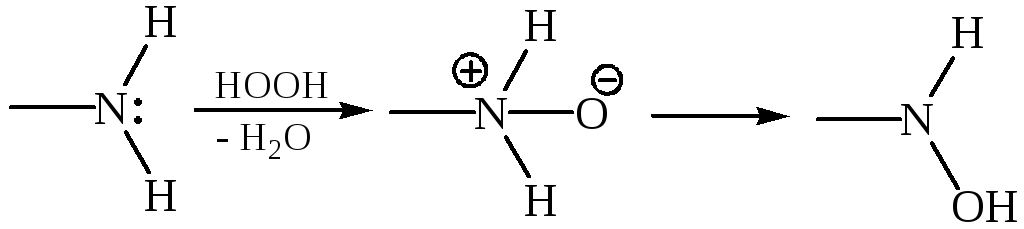
6.1.2 Реакция окисления первичного ариламина гидропероксидом трифторацетила:

6.2 Реакция окисления вторичных аминов:

При окислении пространственно затрудненных вторичных аминов, например, триацетонамина, образуются иминоксильные радикалы, например, 2,2,6,6-тетраметил-4-оксопиперидин-1-оксил:

6.3 Реакция окисления третичных аминов. Третичные амины окисляются до оксидов аминов при применении пероксида водорода или пероксикарбоновых кислот:

6.3.1 Реакция Коупа (1949 г.). При нагревании до 150–200 оС оксиды третичных аминов подвергаются элиминированию при наличии хотя бы одного атома водорода у β-углеродного атома. Например, нагреванием N,N-диметилциклогексилметанаминооксида с количественным выходом получают метиленциклогексан:

