
- •8.5.2 Соединения ароматического ряда
- •8.5.2.1 Моноароматические соединения
- •1. Дегидроциклизация и дегидрогенизация парафинов:
- •2. Дегидрогенизация циклоалканов:
- •1.2 Алкилирование:
- •8.5.2.2 Полициклические арены с изолированными кольцами
- •2. Реакция Вюрца:
- •3. Димеризация бензола в присутствии солей Pd:
- •1.2 Реакция с амидом натрия:
- •1.3 Взаимодействие с щелочными металлами:
- •8.5.2.3 Полициклические арены с конденсиро-ванными кольцами
- •2. Циклизация ацетилена и бензола:
- •3. Дегидроциклизация алканов:
- •1.4 Окисление:
- •1.5 Гидрирование:
- •9. Реакционные центры и основные механизмы реакций углеводородов
- •1. Генерирование электрофильной частицы
- •3. Стабилизация карбкатиона
- •9.1 Особенности протекания некоторых реакций
- •2. Региоселективность реакций присоединения к несимметричным алкенам и алкинам реагентов типа н–х
- •Современная электронная интерпретация правила Марковникова.
- •4. Стереоспецифичность реакции гидроксилирования алкенов (реакция Вагнера)
- •5. Химические особенности сопряженных диенов
- •6. Влияние заместителей на реакционную способность и ориентацию в реакциях электрофильного замещения в бензольном кольце
- •Резонансные структуры карбкатиона (3)
- •Примеры
- •9.2 Оптическая спектроскопия
- •Уф – спектр ик – спектр
- •3. Ионизация
- •4. Природа растворителя
- •Примеры
- •Конспект лекций гомофункциональные углеводороды
- •Галогенопроизводные углеводородов
- •1.1 Галогенпроизводные алифатического ряда
- •1. Реакции замещения.
- •3.2.1 Реакции магнийорганических соединений
- •3.2.1.1 Взаимодействие с соединениями, имеющими подвижный атом водорода:
- •1.1. Получение алифатических аминов
- •6. Специальные методы
- •3. Взаимодействие аминов с азотистой кислотой
- •6.1.1 Реакция окисления первичных аминов:
- •6.1.2 Реакция окисления первичного ариламина гидропероксидом трифторацетила:
- •6.2 Реакция окисления вторичных аминов:
- •6.3.2 Ацилирование третичных аминов:
- •7. Реакции с электрофильными реагентами ароматических аминов
- •8. Реакции конденсации
- •8.3 Реакции конденсации третичных аминов:
- •2. Реакции ароматических солей диазония без выделения азота
- •3. Реакции диазоалканов
- •1. Желтого типа:
- •2. Сине-зеленого типа:
- •3. Фуксиново-красного типа:
6.3.2 Ацилирование третичных аминов:

7. Реакции с электрофильными реагентами ароматических аминов
7.1 Галогенирование. Активность анилина в реакциях галогенирования столь велика, что эти реакции не требуют применения катализатора, а замещение на галоген протекает сразу в три положения быстро и количественно:

7.1.1 Получение моногалогенаминов. Моногалогенамины получают галогенированием анилидов с последующим удалением ацильной группы гидролизом:

7.2 Нитрование. Для снижения основных свойств анилина и предотвращения возможных окислительных процессов при получении n-нитроанилина проводят предварительную защиту аминогруппы ацилированием:

7.2.1 Нитрование третичных аминов. Диалкиламиногруппы R2N являются более сильными активирующими заместителями, чем аминогруппа. Поэтому третичные ароматические амины обрабатывают электрофильными агентами в мягких условиях:

7.3 Сульфирование. Сульфирование анилина проводят концентрированной серной кислотой при 180–200 оС, в промышленности этот метод известен как запекание, продуктом реакции является анилин-4-сульфокислота (сульфаниловая кислота):

8. Реакции конденсации
8.1 Реакции конденсации первичных аминов. Первичные амины взаимодействуют с карбонильными соединениями с образованием иминов, производные алифатических аминов, как правило, малоустойчивы:


Ароматические амины образуют устойчивые имины (основания Шиффа):

Эти реакции протекают как АN по карбонильной группе с промежуточным образованием аминоспирта и последующим отщеплением молекулы воды.
8.2 Вторчные амины (енамины). Вторичные амины не образуют имины, т. к. имеют единственный протон у атома азота. При наличии Н-атома в β-положении к карбонильной группе исходного карбонильного соединения стадия элиминирования протекает с его участием и завершается образованием енамина:

8.3 Реакции конденсации третичных аминов:


9. Реакция изомеризации. При нагревании под давлением возможна изомерия метильных групп при атоме азота:

п-толуидин ксилидин мезидин
10. Гидрирование. При гидрировании анилина в присутствии катализатора образуется циклогексиламин:
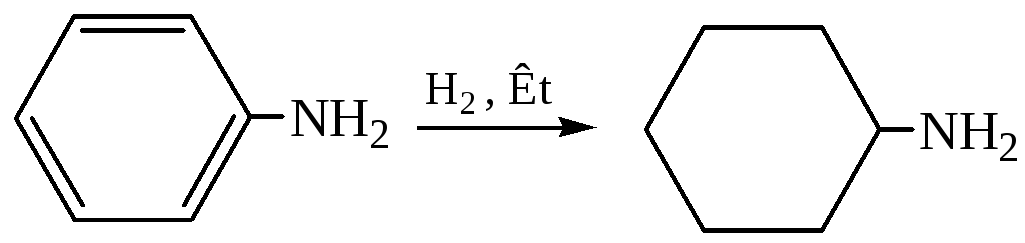
11. Получение диазосоединений
11.1 Реакция диазотирования (П. Грисс, 1858 г.):

На первой стадии образуется катион нитрозония:

На второй стадии образуется катион диазония:

11.2 Получение диазоалканов. В препаративных целях диазоалканы получают взаимодействием нитрозоамидов карбоновых или сульфоновых кислот с сильными основаниями.
11.2.1

N-метил-N-нитрозоамид п-толуосульфокислоты
Реакции диазосоединений
1. Реакции ароматических солей диазония с выделением азота
1.1 Замена диазогруппы на гидроксигруппу. Замена диазогруппы на гидроксигруппу представляет собой реакцию SN у ароматического атома углерода и формально может рассматриваться как гидролиз соли диазония:
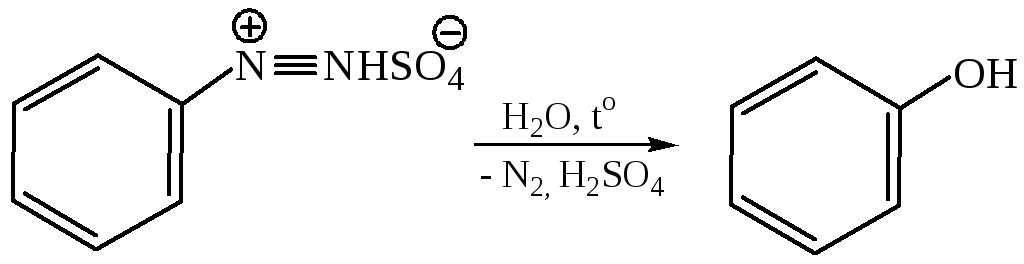
Реакция идет с промежуточным образованием фенил-катиона:

1.2 Введение группы SH:

1.3 Замещение диазогруппы на галогены
1.3.1 Замещение диазогруппы на фтор (реакция Шимана, 1927 г). Реакцию проводят термическим разложением твердого тетрофторобората арендиазония:

1.3.2 Реакция Гаттермана. Замещение диазогруппы на хлор и бром воздействием на диазониевую соль металлической медью и галогеноводородной кислотой:

1.3.3 Замещение диазогруппы на хлор, бром, цианогруппу. Т. Зандмейером было обнаружено, что в присутствии солей одновалентной меди происходит замещение диазогруппы на СI, Br, CN.
1.3.3.1 Замещение диазогруппы на бром:

1.3.3.2 Замещение диазогруппы на хлор:

1.3.3.3 Замещение диазогруппы на цианогруппу:

1.3.2 Замена диазогруппы на йод. Если в диазорастворе присутствует такой сильный нуклеофил, как йодид-ион, то диазогруппа гладко замещается на атом йода. Замена N2→I в этом случае не сопровождается побочными процессами:

1.4 Замещение диазогруппы на нитрогруппу. При обработке суспензии арендиазонийтетрафторбората в водном растворе нитрита натрия металлической медью с препаративным выходом получают нитроарен:

1.5 Замена диазогруппы на водород (реакция дезаминирования). Диазогруппа может быть замещена на водород действием этанола на соль диазония при нагревании:

1.6 Замещение диазогруппы на фрагмент арена (реакция Гомберга-Бахмана, 1924 г.):

1.7 Превращение алкиламинов в алкилбромиды. Модификация реакции Зандмейера применяется для превращения алкиламинов в алкилбромиды:

