
органика
.pdf
нирования по этому положению. Реакция может катализироваться как кислотами, так и щелочами.
В щелочной среде происходит сначала депротонирование альдегида или кетона по α-положению, а затем карбанион реагирует с молекулой галогена. Например, при взаимодействии пропиофенона (фенилэтилкетона) с бромом в присутствии едкого натра продукт реакции – 2-бром-1-фенил-1-пропанон – образуется по следующему механизму.
H |
|
Br Br |
Br |
|
OH |
CCHCH |
CCHCH3 |
||
CCHCH |
_ |
|
||
3 |
3 |
Br |
O |
|
O |
O |
|
||
|
|
|||
В кислой среде реакция идет через енольную форму, в которой углеро-углеродная двойная связь активирована к электрофильному присоединению молекулы галогена (+М-эффект гидроксильной группы). Образующийся дигалогенид сразу же отщепляет молекулу галогеноводорода и превращается в продукт α- галогенирования. Так, например, происходит региоселективное взаимодействие 2-бутанона с хлором в присутствии серной кислоты до 3-хлор-2-бутанона (региоселективность объясняется бóльшей устойчивостью соответствующего енола по сравнению с альтернативным).
|
|
|
|
|
|
|
|
|
|
Cl2 |
Cl Cl |
|
|
|
Cl |
||||||
CH3 |
|
CCH2CH3 |
H |
CH3 |
C=CHCH3 |
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
CH3C |
|
CHCH3 |
|
|
CH3CCHCH3 |
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
AdE |
|
_ |
HCl |
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
O |
|
OH |
OH |
||||||||||||||||||
|
O |
||||||||||||||||||||
Альдегиды и кетоны, имеющие при карбонильном атоме углерода метильную группу, под действием избытка галогена в щелочной среде подвергаются так называемому галоформному расщеп-
лению.
|
|
|
|
|
|
|
3X2 |
|
|
|
|
|
|
|
NaOH |
|
|
|
|
|
|
|
CH3 |
|
C |
|
R |
|
CX3 |
|
C |
|
R |
|
CHX3 + |
RCOO Na |
|
||||||||
|
|
|
|
|
||||||||||||||||||
|
|
NaOH |
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
O |
|
|
|
|
|
|
|
|
|
|
||||||||
галоформ
2.4. Окисление и восстановление альдегидов и кетонов
2.4.1. Окисление альдегидов и кетонов
71
www.mitht.ru/e-library

Альдегиды чрезвычайно легко подвергаются окислению до соответствующих карбоновых кислот. В качестве окислителей могут быть использованы дихромат калия в кислой среде, перманганат калия и другие даже более слабые оксислители.
O
RCH=O  RCOOH
RCOOH
Кетоны более устойчивы к окислению, но при действии сильных окислителей в жестких условиях происходит окислительная деструкция молекулы кетона, т.е. разрываются связи атомов углерода с карбонильным атомом углерода, и происходит окисление остатков до карбоновых кислот. Например, такое окисление 2-бутанона приводит к смеси диоксида углерода, уксусной и пропионовой кислот: при разрыве связи А образуются СО2 и пропионовая кислоты, а при разрыве связи В – две молекулы уксусной кислоты.
A B
K2Cr2O7, t
CH3 C
C CH2CH3
CH2CH3 
 CO2
CO2  CH3COOH + CH3CH2COOH
CH3COOH + CH3CH2COOH
H2SO4
O
Качественной реакцией на альдегиды является реакция «серебряного зеркала» - окисление альдегидов аммиачным раствором оксида серебра до аммонийной соли карбоновой кислоты. При этом происходит восстановление катиона серебра до металлического серебра, которое при тщательном проведении этой пробы выпадает в виде тонкого зеркального слоя на поверхности стеклянной пробирки.
Ag(NH3)2OH |
|
RCH=O _Ag |
RCOO NH4 |
_NH3 |
|
2.4.2. Восстановление альдегидов и кетонов
Альдегиды и кетоны восстанавливаются до первичных и вторичных спиртов соответственно. В качестве восстановителей могут использоваться водород на катализаторе (каталитическое гидрирование), комплексные гидриды – литийалюминийгидрид (LiAlH4) или натрийборгидрид (NaBH4).
RCH=O H2, Ni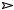 RCH2OH
RCH2OH
72
www.mitht.ru/e-library

Следует отметить, что гидридное восстановление является примером реакции альдегидов и кетонов с Н-нуклеофилами, поскольку при этом происходит присоединение к карбонильной группе гидрид-аниона. Например, алюмогидрид лития легко переносит на карбонильные группы все четыре атома водорода в виде гидриданионов. Образовавшийся таким образом комплексный алкоголят подвергают затем гидролизу.
|
|
3 RCR' |
|
H2O |
RCR' + H AlH3 Li |
RCHR' |
O |
(RCHR')4Al Li |
|
|
4 RCHR' |
|||
O |
O AlH3 Li |
|
O |
OH |
Кроме восстановления до спиртов для альдегидов и кетонов возможно восстановление и до углеводородов:
по Клемменсену
R |
C |
|
|
O |
Zn/Hg |
R |
CH2 |
|
||||
|
|
|
|
|
|
|||||||
R' |
HCl |
R' |
|
|||||||||
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|||||
по Кижнеру – Вольфу |
|
|
|
|||||||||
R |
C |
|
|
O |
|
NH2NH2, KOH R |
CH2 |
|||||
R' |
|
|
|
t |
|
|
R' |
|||||
2.4.3. Реакция Канниццаро
Альдегиды, не имеющие в α-положении атомов водорода, при действии концентрированного раствора едкого кали претерпевают диспропорционирование с образованием карбоновых кислот и спиртов. Например, формальдегид превращается в муравьиную кислоту в виде формиата калия (поскольку реакционная среда щелочная) и метиловый спирт.
KOH
2CH2=O |
HCOO K + CH3OH |
73
www.mitht.ru/e-library

Механизм реакции Канниццаро включает две стадии нуклеофильного присоединения: на первой стадии гидроксид-анион присоединяется по карбонильной группе молекулы формальдегида, а затем от этого аддукта отщепляется атом водорода и вместе со своей парой электронов, т.е. в виде гидрид-аниона присоединяется по карбонильной группе второй молекулы формальдегида.
|
H |
CH2=O |
|
CH2=O |
OH |
HCOO + CH3OH |
|
H C OH |
H C O H + O CH3 |
||
|
O |
O |
|
По такому же механизму из бензальдегида образуется смесь бензоата калия и бензилового спирта.
CH=O |
KOH |
COOK + |
CH OH |
|
|
2 |
Если проводить перекрестную реакцию Канниццаро со смесью какого-либо неенолизующегося альдегида и формальдегида, то формальдегид всегда играет роль восстановителя, т.е. выступает как донор гидрида и окисляется до муравьиной кислоты, например:
CH=O + CH2=O |
KOH |
|
HCOOK |
CH OH |
+ |
||
|
2 |
|
3. Задачи и упражнения
1.Назовите по систематической номенклатуре следующие соединения: а) муравьиный альдегид; б) ацетон; в) бензальдегид; г) масляный альдегид; д) акролеин; е) коричный альдегид; ж) винилметилкетон; з) пропиофенон.
2.Озонолизом симметричного алкена получите: а) уксусный альдегид; б) бензальдегид; в) ацетофенон; г) 2-бутанон.
3.Гидратацией соответствующего алкина по Кучерову получите: а) 2-бутанон; б) ацетофенон; в) 2-гексанон.
74
www.mitht.ru/e-library
4.Гидролизом подходящего геминального дигалогенида получите: а) пропаналь; б) 1-фенил-1-бутанон; в) ацетон; г) циклогексанон.
5.Окислением соответствующего спирта получите: а) 2- метилпентаналь; б) ацетофенон; в) бензальдегид; г) ацетон.
6.Из соответствующих производных карбоновых кислот получите: а) ацетон; б) фенилуксусный альдегид; в) дибензилкетон; г) ацетофенон.
7.Предложите схему получения бензофенона (дифенилкетона) с использованием только бензола и любых неорганических реагентов.
8.Всеми возможными способами получите: а) уксусный альдегид; б) ацетон; в) бензальдегид; г) 1-фенил-1-пропанон.
9.Для каких из перечисленных альдегидов и кетонов возможна ке- то-енольная таутомерия: а) пентаналь; б) формальдегид; в) ацетофенон; г) 1-фенил-1-бутанон; д) 2,4-диметил-3-пентанон; е) циклопентанон? Изобразите соответствующие таутомерные равновесия.
10.Изобразите механизмы следующих реакций: а) уксусный альдегид и 2 эквивалента 1-пропанола в кислой среде; б) бензальдегид и гидросульфит натрия; в) ацетон и анилин; г) ацетофенон и гидроксиламин; д) 2-бутанон и ацетиленид натрия; е) альдольной конденсации бутаналя в присутствии едкого натра; ж) смесь формальдегида и ацетофенона в присутствии едкого натра.
11.Напишите уравнения альдольно-кротоновой конденсации следующих соединений под действием водного едкого натра: а) фенилуксусный альдегид; б) 3-пентанон; в) формальдегид и 3- пентанон; г) масляный альдегид; д) бензальдегид и 1-фенил-1- бутанон; е) бензальдегид и ацетон в соотношении 2:1.
12.Напишите уравнения следующих реакций: а) формальдегид и конц. водный раствор КОН; б) пропаналь и хлор в присутствии едкого натра; в) бензальдегид, формальдегид и КОН; г) ацетофенон и 3 эквивалента хлора в растворе едкого натра; д) дифе-
75
www.mitht.ru/e-library

нилкетон и фенилмагнийбромид с последующей обработкой водой; е) формальдегид и водород на никеле.
13. Напишите уравнения следующих превращений:
а) CH3CH2CH=CHCH2CH3 |
O3 |
A |
H2O |
2CH3OH |
C |
|
|
|
Zn |
B |
|
||||
|
|
|
|
H |
|
|
|
|
|
|
CH3NH2 |
NH2NH2 |
E |
KOH, t |
|
|
|
|
D |
|
|
F |
|
|
|
|
NH2OH |
D |
|
|
|
|
|
|
|
|
|
|
|
б) |
C CH H2O, H |
A |
CH2=O |
B |
H |
|
|
|
Hg2 |
|
NaOH |
|
C |
|
|
|
|
|
HCN |
E |
|
|
|
|
|
|
KCN |
|
|
|
|
|
|
|
|
|
|
|
|
76
www.mitht.ru/e-library
ДЛЯ ЗАМЕТОК
77
www.mitht.ru/e-library
ДЛЯ ЗАМЕТОК
78
www.mitht.ru/e-library
Издание учебное
Помогаев Александр Ильич
Краткий курс органической химии
Учебное пособие
Часть 3
Функциональные производные углеводородов.
Галогенопроизводные, спирты, фенолы, альдегиды и кетоны
Подписано в печать ……….. Формат 60х84/16. Бумага писчая. Отпечатано на ризографе. Уч. изд. листов Тираж 100 экз. Заказ № …..
Лицензия на издательскую деятельность ИД № 03507 (рег. № 003792) код 221
Московская государственная академия тонкой химической технологии им. М.В. Ломоносова
Издательско-полиграфический центр
119571 Москва, пр. Вернадского 86.
79
www.mitht.ru/e-library
