
Решение задач по органической химии
.pdf
тивность этой реакции. Проявляет ли главный продукт этой реакции оптическую активность? Ответ поясните.
Винилметиловый эфир содержит в своей молекуле двойную углерод-углеродную связь с очень высокой электронной плотностью, поскольку метоксигруппа, проявляя сильный положительный мезомерный эффект за счет р-π-сопряжения, является электронодонорным заместителем (+М ›› -I).
CH2 CH
CH OCH3
OCH3
Хлороводород как сильная кислота является типичным электрофильным реагентом, поскольку легко отдает протон, выступающий в реакции акцептором электронной пары. Поэтому данное взаимодействие протекает как электрофильное присоединение (AdЕ).
При присоединении несимметричного реагента к несимметрично замещенной двойной связи могут образоваться два структурных изомера, отличающихся положением заместителя (региоизомеры).
Cl
 CH3 CH OCH3
CH3 CH OCH3
CH2 CH OCH3 + H Cl
CH OCH3 + H Cl
 CH2 CH2 OCH3
CH2 CH2 OCH3
Cl
Реакции электрофильного присоединения обычно протекают региоселективно, т.е. из двух возможных изомеров положения преимущественно образуется один. Для обоснования региоселективности реакции необходимо сравнить стабильность альтернативных промежуточных частиц – интермедиатов, поскольку главный продукт реакции образуется через наиболее устойчивый интермедиат.
Механизм реакции выглядит следующим образом:
CH2 |
CH |
H |
Cl |
|
CH |
OCH3 |
CH2 |
CH |
OCH3 |
OCH3 |
CH2 |
|
|||||||
|
|
|
|
H |
|
|
_Cl |
H |
|
|
|
|
|
|
|
|
|
||
|
|
|
CH |
Cl |
OCH |
CH |
CH |
OCH |
|
|
|
|
|
CH |
|||||
|
|
|
3 |
|
|
3 |
3 |
|
3 |
CH2 |
CH |
OCH3 |
|
|
41 |
|
|
|
|
http://www2 |
.mitht2.ru/e-library3 |
|
|
||||||
H |
|
|
|
|
|||||
|
|
CH |
CH |
OCH |
|
|
|
||
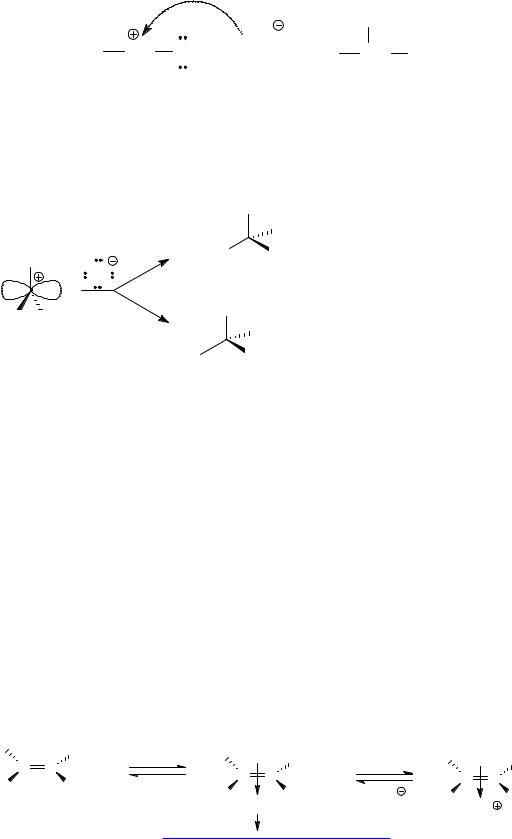
Первый из интермедиатов представляет собой карбокатион, стабилизированный р-π-сопряжением, заряд в нем делокализован, что можно описать двумя граничными структурами. Поэтому он значительно более устойчив, чем второй, в котором положительный заряд локализован на первичном атоме углерода. Таким образом, главный продукт образуется из первого катиона при присоединении к нему хлорид-аниона.
Cl



 Cl
Cl
CH3 CH OCH3  CH3 CH OCH3
CH3 CH OCH3
Главный продукт этой реакции – 1-метокси-1-хлорэтан, в структуре которого имеется хиральный атом углерода, – не проявляет оптической активности, поскольку он представляет собой эквимолярную смесь энантиомеров, т.е. рацемат. Его образование не является стереонаправленным процессом, т.к.
|
|
CH3 |
|
|
|
|
H |
(R)-1-метокси-1-хлорэтан |
|
CH3 |
CH3O |
Cl |
||
|
||||
Cl |
|
|
||
CH3O H |
CH3 |
|
||
|
H |
(S)-1-метокси-1-хлорэтан |
||
|
|
|||
|
Cl |
OCH3 |
||
|
|
|||
хлорид-анион может присоединиться к плоскому карбокатиону с равной вероятностью как с одной стороны, так и с другой стороны от плоскости, поэтому энантиомеры образуются в соотношении 1:1.
Задача 3. Изобразите механизм взаимодействия (Е)-2-
пентена с бромом в темноте при охлаждении. Обратите внимание на стереохимию.
Взаимодействие алкенов с бромом происходит в нормальных условиях очень легко, реакция идет по механизму электрофильного присоединения (АdЕ). Вначале образуется π- комплекс, в котором партнеры по реакции связаны электростатическими силами между π-электронной плотностью алкена и положительным концом диполя, возникающего при поляризации неполярной ковалентной связи бром-бром. Затем происхо-
CH3 |
H |
Br2 |
CH |
H |
|
|
CH |
|
C |
C |
|
3 |
|
|
H |
||
|
C |
|
|
3 |
||||
H |
CH2CH3 |
|
C |
_ |
|
C |
C |
|
|
H |
42CH2CH3 |
Br |
H |
CH CH |
|||
|
|
|
|
Br |
|
|
2 3 |
|
|
|
|
|
|
|
|
|
Br |
http://www.mitht.ru/e-library
Br
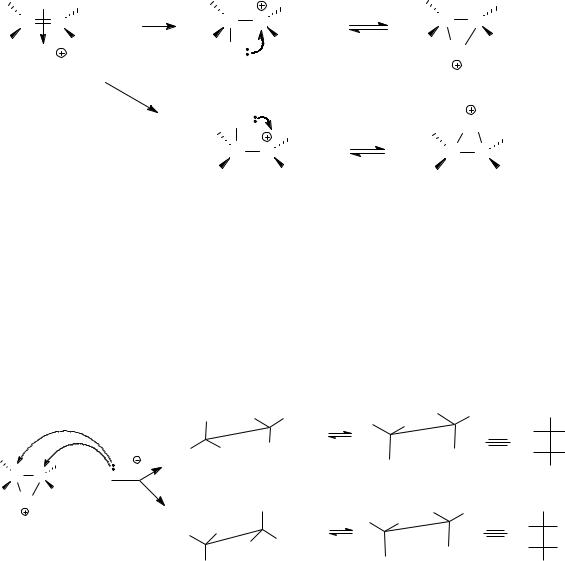
дит гетеролитический разрыв связи бром-бром и образуется новый π-комплекс алкена с катионом брома.
Затем происходит синхронный процесс гетеролитического разрыва π-связи и образование ковалентной связи между атомом брома, предоставляющим вакантную орбиталь, и одним из атомов углерода двойной связи, предоставляющим заполненную орбиталь. Образовавшийся карбокатион превращается затем в более устойчивый циклический катион бромония.
CH |
H |
CH |
|
H |
CH3 |
|
|
H |
3 |
3 |
C |
|
C |
C |
|||
C |
C |
|
C |
H |
CH2CH3 |
|||
H |
CH CH |
H |
Br |
CH CH |
Br |
|||
|
2 3 |
|
2 3 |
|
|
|||
|
Br |
|
|
|
|
|
|
|
|
|
CH |
Br |
H |
CH |
|
Br |
H |
|
|
3 |
C |
3 |
C |
C |
||
|
|
|
C |
|
|
|||
|
|
H |
|
CH2CH3 |
H |
|
|
CH2CH3 |
Поскольку вероятность атаки брома с разных сторон от плоскости двойной связи одинакова, то получаются энантиомерные катионы бромония в соотношении 1:1, т.е. образуется рацемический катион бромония.
На последней стадии реакции происходит нуклеофильное раскрытие трехчленного катиона бромония бромид-анионом с образованием энантиомерных дибромидов.
|
|
|
Br H |
C2H5 |
Br |
Br |
H |
C2H5 |
I |
|
|
|
|
H |
Br |
H |
|
|
|
|
|
|
|
|||
II |
H |
CH3 |
H |
Br |
|
CH3 |
Br |
H |
CH3 |
Br I |
|
|
|
C2H5 |
CH3 |
||
C C |
|
|
|
|
|
|
|
|
H Br |
CH2CH3 |
II |
|
Br |
|
H |
Br |
C2H5 |
|
|
|
H |
|||||
|
|
CH3 |
H |
|
Br |
H |
Br |
|
|
|
C2H5 |
|
|
||||
|
|
|
H |
|
|
H |
Br |
|
|
|
|
Br |
|
|
CH3 |
C2H5 |
CH3 |
|
|
|
|
|
|
43
http://www.mitht.ru/e-library

Легко убедиться в том, что раскрытие бромид-анионом второго энантиомера бромоний-катиона приведет к тем же энантиомерным дибромидам.
|
|
|
|
|
Br |
H |
Br |
|
C2H5 |
|
|
|
|
CH3 |
H |
H |
Br |
|
|
H |
Br |
|
|
|
C2H5 |
|
|
|
||||
|
|
|
|
H |
CH3 |
C2H5 |
H |
Br |
||
|
Br |
|
I |
Br |
|
|
CH3 |
|||
CH |
H |
|
|
|
|
|||||
|
|
|
|
|
||||||
3 |
C |
|
|
|
|
|
|
|
|
|
C |
|
Br |
|
|
|
|
|
|
C2H5 |
|
H |
|
CH2CH3 |
Br H |
C2H5 Br |
Br |
|
H |
|||
|
|
|
||||||||
|
I II |
II |
H |
|
|
Br |
H |
|||
|
|
|
CH3 |
H |
Br |
|
C |
|
Br |
H |
|
|
|
|
H |
|
|||||
|
|
|
|
|
|
CH |
2 |
|
5 |
CH3 |
|
|
|
|
|
|
3 |
|
|
|
|
Таким образом, взаимодействие (Е)-2-пентена с бромом по механизму электрофильного присоединения происходит стереоспецифично как анти-присоединение атомов брома с образованием рацемической смеси (2S,3R)- и (2R,3S)-2,3- дибромпентанов.
Задача 4. Изобразите механизм взаимодействия 1-
метилциклогексена с хлором в этаноле при охлаждении. Изобразите наиболее устойчивые конформации главного продукта реакции.
В указанных условиях алкены реагируют с галогенами в присутствии большого избытка нуклеофильного растворителя по механизму электрофильного присоединения (АdЕ). Данное взаимодействие является реакцией хлорэтоксилирования, в которой к одному атому углерода двойной связи алкена присоединяется атом хлора, а к другому – этоксигруппа.
Вначале субстрат и молекула хлора образуют π-комплекс, который затем с гетеролитическим разрывом π-связи и связи
Cl2 |
|
|
|
|
|
|
|
CH3 |
|
Cl |
H |
CH |
Cl |
|
CH |
|
CH |
44 |
3 |
|
H |
3 |
|
|
3 |
Cl |
|
|
|
||
|
Cl |
|
|
|
|
|
|
Clhttp://www.mitht.ru/e-library
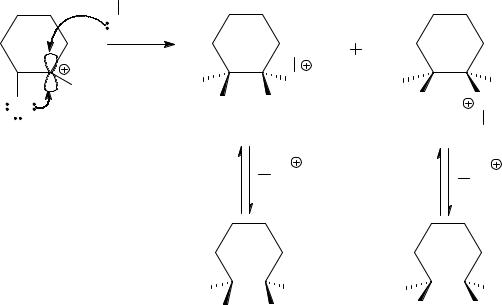
хлор-хлор и превращается в карбокатион. Поскольку при присоединении катиона хлора к атому углерода последний становится хиральным, то, разумеется, образуется рацемический карбокатион.
Присоединение этанола как нуклеофила к карбокатиону происходит стереонаправленно, т.к. атом хлора своей р- орбиталью «прикрывает» одну из сторон возможной нуклеофильной атаки. Поэтому образуется продукт, в котором атом хлора и этоксигруппа находятся в транс-положении друг к другу, в виде рацемата. На последней стадии происходит депротонирование продуктов присоединения этанола.
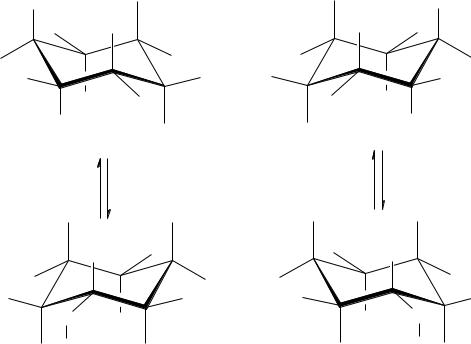
Ниже приведены конформации энантиомеров, на которых указаны абсолютные конфигурации хиральных атомов углерода. Очевидно, что наиболее устойчивыми являются те конфор-
|
H |
|
|
|
|
OC2H5 |
H |
|
|
|
|
|
|
|
CH3 |
H |
OC2H5 |
Cl |
CH3 |
Cl |
Cl |
CH3 |
H |
OC2H5 |
|
|
|
|
H |
|
|
H |
|
H |
H |
|
Cl |
|
|
OC2H5 Cl |
|
H |
|
|
|
CH3 |
|
|
|
|
|
|
|
|||||
|
|
|
CH |
|
OC2H5 |
||||||
|
|
|
3 |
|
|
|
|
|
|
||
мации, в которых два заместителя – атом хлора и этоксигруппа
– экваториальны.
45
http://www.mitht.ru/e-library
Cl |
Cl |
S |
R |
CH3 |
CH3 |
R |
S |
OC2H5 |
OC2H5 |
|
CH3 |
CH3 |
|
Cl S |
R |
S |
Cl |
O |
O R |
||
C H |
|
C2H5 |
|
2 |
5 |
|
|
Кроме указанного главного продукта в этой реакции образуется и минорный продукт – соответствующий вицинальный дихлорид как продукт присоединения молекулы хлора по двойной связи (также в виде рацемата).
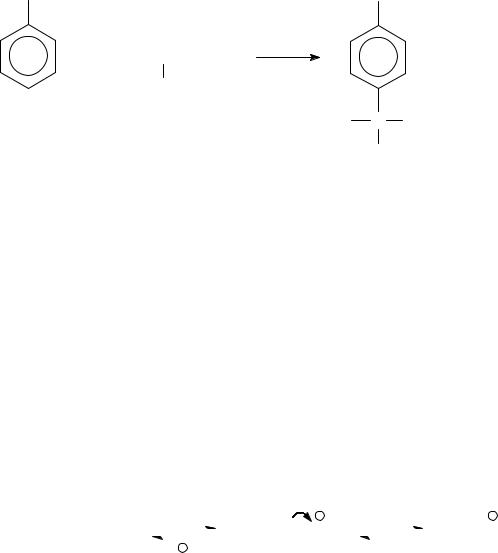
Задача 5. Изобразите механизм взаимодействия метокси-
бензола (метилфенилового эфира) с изобутилхлоридом в присутствии трихлорида алюминия. Обоснуйте региоселективность этой реакции по субстрату и реагенту.
46
http://www.mitht.ru/e-library
OCH3 |
|
OCH3 |
|
+ CH3CHCH2Cl |
AlCl3 |
+ |
HCl |
|
CH3
CH3 C CH3
CH3
Эта реакция представляет собой алкилирование ароматических соединений по Фриделю-Крафтсу, происходящее по механизму электрофильного замещения. В уравнении приведен главный продукт, поскольку продукты замещения и в мета-, и в орто-положения образуются в незначительных количествах.
Сначала образуется электрофильная частица – карбокатион – в результате взаимодействия изобутилхлорида с трихлоридом алюминия в качестве кислоты Льюиса. Образующийся при этом изобутил-катион, как первичный карбокатион, является неустойчивой частицей, которая способна к перегруппировке путем 1,2-сдвига атома водорода с парой электронов в значительно более устойчивый третичный карбокатион.
H
CH3 |
|
CHCH2Cl + AlCl3 |
|
|
|
CH3 |
|
|
|
|
|
|
|
|
|
~ H |
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
C |
|
CH2 |
|
CH3 |
|
C |
|
CH3 |
||||||||||
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|||||||||||||||||
_ |
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|||||||||||||||||
|
CH3 |
AlCl4 |
|
CH3 |
|
|
|
CH3 |
|||||||||||||||
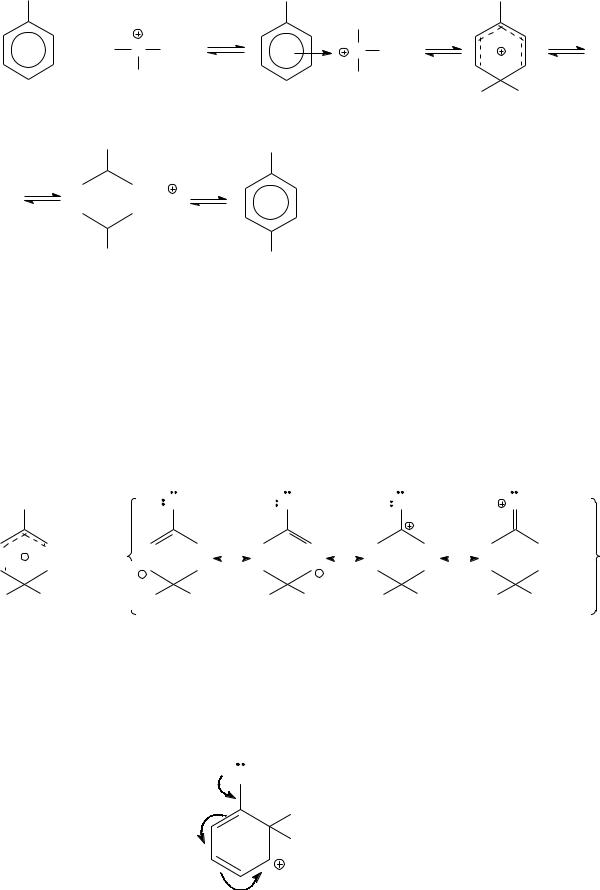
Затем образовавшаяся электрофильная частица – трет- бутил-катион – вступает в реакцию электрофильного замещения с ароматическим соединением – метоксибензолом.
47
http://www.mitht.ru/e-library
OCH3 |
OCH3 |
OCH3 |
|
CH3 |
|
+ CH3 C CH3 |
C CH3 |
|
CH3 |
CH3 |
C(CH3)3 |
|
H |
OCH3 OCH3


 H
H
C(CH3)3 C(CH3)3
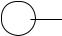
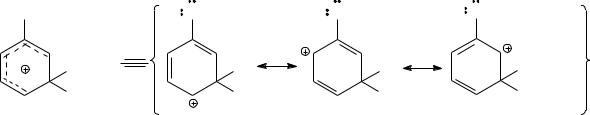
Региоселективность замещения обусловлена большей стабилизацией пара-σ-комплекса по сравнению с орто- и мета -σ-комплексами.
Строение пара-σ-комплекса, в котором положительный заряд делокализован не только в цикле, но и с участием атома кислорода метоксильной группы (р-π-сопряжение), описывается четырьмя граничными структурами.
OCH3 |
OCH3 |
OCH3 |
OCH3 |
OCH3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H C(CH3)3 |
|
|
|
H C(CH3)3 H C(CH3)3 H C(CH3)3 H C(CH3)3 |
|||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Аналогично можно описать и строение орто-σ-комплекса, однако его устойчивость ниже из-за стерического фактора, который возникает именно в этом комплексе в связи со значительным пространственным взаимодействием метоксигруппы и очень объемного трет-бутила.
 OCH3
OCH3
C(CH3)3
H
48
http://www.mitht.ru/e-library
мета-σ-Комплекс в меньшей степени дестабилизирован пространственными взаимодействиями, чем орто-σ-комплекс, однако электронная стабилизация за счет сопряжения с метоксигруппой в нем отсутствует, поэтому он менее всего стабилизирован.
OCH3 |
OCH3 |
OCH3 |
OCH3 |
H |
H |
H |
H |
C(CH3)3 |
C(CH3)3 |
C(CH3)3 |
C(CH3)3 |
49
http://www.mitht.ru/e-library
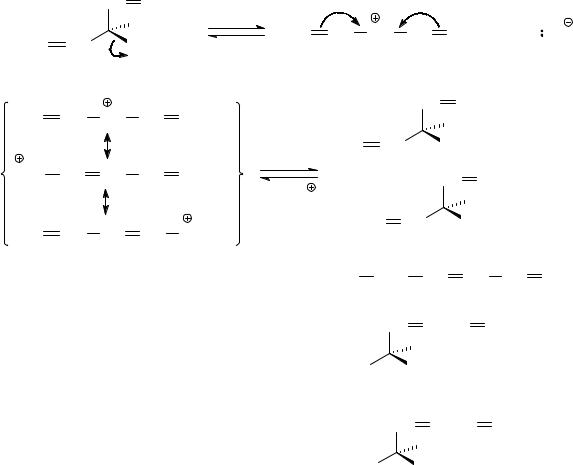
Задача 6. Изобразите механизм взаимодействия (S)-3-бром-
1,4-гексадиена с водой.
Галогенопроизводные вступают в реакции нуклеофильного замещения, протекающие в зависимости от строения и условий по моноили бимолекулярному механизму. Данный бромид относится к галогенопроизводным аллильного типа, которые могут образовывать очень устойчивый карбокатион, в котором положительный заряд делокализован (три граничные структуры). Кроме того, вода в этой реакции является не только нуклеофильным реагентом, но и, взятая в избытке, выполняет роль полярного протонного растворителя, который хорошо стабилизирует как катионы, так и анионы. Поэтому здесь весьма вероятен механизм SN1. Делокализация заряда в промежуточном катионе приводит к образованию не только продукта формального замещения атома брома у С(3) в виде рацемического 1,4-гексадиен-3-ола, но и к образованию продуктов аллильных перегруппировок: рацемического 3,5-гексадиен-2-ола и 2,4- гексадиен-1-ола.
|
|
CH |
CHCH3 |
|
|
|
|
||
|
|
|
H |
CH2 CH CH CH CHCH3 + Br |
|||||
CH2 |
CH |
Br |
|||||||
|
|
|
|
|
|||||
CH2 CH |
CH |
CH |
CHCH3 |
|
|
CH CHCH3 |
|||
|
|
|
H |
||||||
|
|
|
|
2 H2O |
CH2 |
CH |
|
OH |
|
CH2 |
CH |
CH |
CH |
CHCH3 _ H O |
|
|
|
CH CH2 |
|
|
|
|
|
3 |
|
|
|
H |
|
CH2 CH |
CH |
CH |
CHCH3 |
CH3CH CH |
OH |
||||
|
|
|
|
||||||
|
|
|
|
|
HO |
CH2 |
CH CH CH CHCH3 |
||
|
|
|
|
|
|
CH |
CHCH CH2 |
||
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
CH3 |
OH |
|||
|
|
|
|
|
|
CH |
CHCH CH2 |
||
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
HO |
CH3 |
|||
50
http://www.mitht.ru/e-library
