
Решение задач по органической химии
.pdf
Задача 7. Изобразите механизм взаимодействия (S)-2-
бромбутаннитрила с цианидом натрия в диметилформамиде. Обладает ли продукт реакции оптической активностью? Ответ поясните.
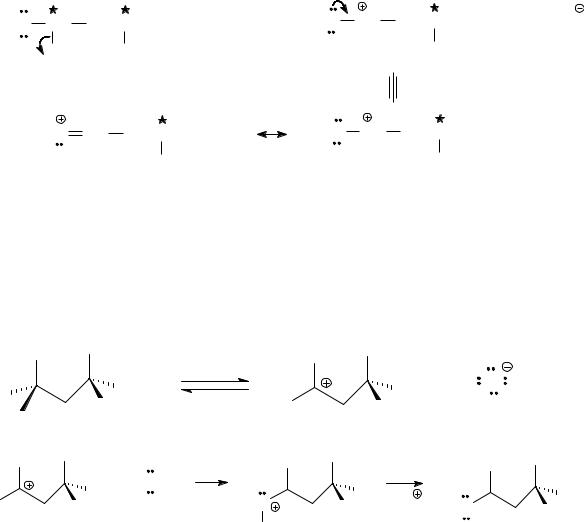
Очевидно, что реакция должна преимущественно протекать по механизму бимолекулярного замещения (SN2), поскольку необходимый для мономолекулярного замещения карбокатион дестабилизирован электроноакцепторной циано-группой. Кроме того, диметилформамид как апротонный полярный растворитель не оказывает необходимого содействия для стабилизации первой стадии (ионизации) в мономолекулярном механизме замещения.
Бимолекулярное нуклеофильное замещение происходит как синхронный процесс разрыва связи углерод-галоген и образования связи углерод-нуклеофил. Стереохимический результат такого замещения вытекает из строения переходного состояния, в котором уходящая группа и нуклеофил максимально удалены друг от друга и располагаются на одной оси с атомом углерода, при котором происходит замещение.
CH CH |
CH2CH3 |
CH CH |
||||
2 |
3 |
|
|
|
||
|
|
Br |
C |
N |
2 |
3 |
H |
|
H |
|
|||
Br C |
N |
N C H |
|
|
N C C |
N |
Продукт реакции – 2-этилпропандинитрил – не обладает оптической активностью, поскольку его молекула не является хиральной. Асимметрический атом углерода, присутствовавший в исходном бромиде, в процессе нуклеофильного замещения превратился в атом углерода, имеющий два одинаковых заместителя.
51
http://www.mitht.ru/e-library
Задача 8. Изобразите механизм взаимодействия (1R,3R)-3-
метил-1-метокси-1-хлорпентана с метанолом. Обладает ли продукт реакции оптической активностью? Ответ поясните.
Данное галогенопроизводное должно реагировать с метанолом преимущественно по механизму мономолекулярного замещения, поскольку карбокатион, образующийся на первой стадии этого механизма при ионизации хлорида, стабилизирован р-π-сопряжением.
CH3O CH CH2CHCH2CH3 
 CH3O CH CH2CHCH2CH3 +
CH3O CH CH2CHCH2CH3 +  Cl
Cl
Cl |
CH3 |
CH3 |
CH O CH |
CH CHCH CH |
CH3O CH CH2CHCH2CH3 |
||
3 |
2 |
2 |
3 |
|
|
CH3 |
|
|
CH3 |
Кроме того, метанол выполняет функцию полярного протонного растворителя, способного достаточно эффективно стабилизировать как карбокатион (в результате сольватации), так и хлорид-анион (за счет образования межмолекулярных водородных связей).
|
OCH CH2CH3 |
|
|
CH2CH3 |
|
|
|
||
|
3 |
|
|
OCH3 |
|
+ |
Cl |
|
|
H |
|
H |
|
H |
|
H |
|
||
|
|
|
|
|
|
||||
Cl |
|
CH3 |
|
|
CH |
|
|
|
|
|
|
|
|
|
3 |
|
|
|
|
|
CH2CH3 |
|
OCH |
CH CH |
|
|
CH2CH3 |
||
OCH3 |
|
|
2 |
3 |
|
OCH |
|||
|
|
|
|
3 |
|
|
|
|
|
|
|
+HOCH |
|
|
|
|
3 |
|
|
|
H |
|
H |
|
|
|
|
||
H |
|
3 |
CH3O |
_H CH O |
|
H |
|||
CH |
|
|
CH |
|
|||||
|
3 |
|
|
|
3 |
|
CH |
||
|
|
|
3 |
|
|
|
|||
|
|
|
|
|
|
|
|
|
3 |
H
В результате замещения атома хлора происходит уничтожение асимметричности первого атома углерода, т.к. новый заместитель является аналогичным одному из трех других. Конфигурация же третьего атома углерода, не принимавшего участие в реакции, сохраняется неизменной. Поэтому образующийся в качестве продукта реакции (3R)-3-метил-1,1- диметоксипентан, как хиральный объект, обладает оптической активностью.
52
http://www.mitht.ru/e-library
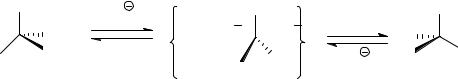
Задача 9. Как будет изменяться удельное оптическое вра-
щение при взаимодействии (R)-2-иодбутана с иодидом калия в ацетоне? Ответ обоснуйте.
При действии иодида калия на (R)-2-иодбутан в ацетоне возможна нуклеофильная атака иодид-аниона как нуклеофила на электрофильный атом С(2) галогенопроизводного. В ацетоне как апротонном диполярном растворителе такое взаимодействие должно происходить преимущественно по механизму бимолекулярного нуклеофильного замещения (SN2). Переходное состояние при этом должно выглядеть следующим образом.
|
CH3 |
I |
|
|
CH |
|
|
CH |
|
H |
|
3 |
|
H |
3 |
||
|
|
|
I..........I |
|
|
|||
CH3CH2 |
I |
|
CH CH |
H |
_ I |
I |
CH2CH3 |
|
|
|
|
3 |
2 |
|
|
|
|
переходное
состояние
Таким образом, в процессе взаимодействия устанавливается равновесие между энантиомерными 2-иодбутанами. Поскольку термодинамические характеристики энантиомеров абсолютно одинаковы, образуется смесь равных количеств энантиомеров, т.е. рацемическая смесь. Поэтому в процессе установления равновесия удельное оптическое вращение будет уменьшаться по абсолютной величине, пока не станет равным нулю.
53
http://www.mitht.ru/e-library
Задача 10. Изобразите механизм реакции (2R,3S)-2-бром-3-
метилпентана при нагревании с КОН в этаноле. Обратите внимание на стереохимию.
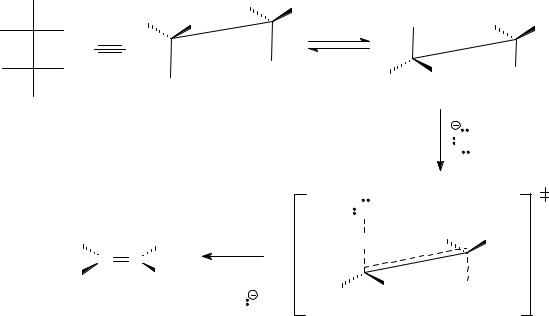
Данная реакция протекает по механизму бимолекулярного элиминирования (Е2). Поскольку основание, под действием которого отщепляется протон, необъемно, то элиминирование осуществляется регионаправленно в соответствии с правилом Зайцева. Кроме того, бимолекулярное элиминирование происходит стереонаправленно, т.к. в переходном состоянии принимает участие заторможенная конформация с анти- расположением уходящих атомов водорода и брома.
Для изображения переходного состояния этой реакции необходимо правильно нарисовать подходящую конформацию с заданными конфигурациями хиральных центров.
CH3 |
|
|
|
|
Br |
H |
|
|
|
Br |
H |
CH3 |
|
H |
|
H |
H CH3 |
||
|
|
|
|
||||||
CH3 |
H |
|
|
|
|
CH |
CH3 |
CH2CH3 Br |
|
|
|
|
CH2CH3 |
3 |
|
|
|
||
CH2CH3 |
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
CH3 |
C C |
H |
|
|
|
H |
H |
CH3 |
|
|
|
|
|
|
|
||||
CH CH |
|
CH |
|
|
|
|
|
||
3 |
2 |
|
3 |
|
CH3 |
|
|
||
|
|
|
|
r |
CH2CH3 Br |
||||
|
|
|
|
|
|
|
|
||
(Z)-3-метил-2-пентен |
|
|
переходное состояние |
||||||
|
|
|
|
|
|
||||
54
http://www.mitht.ru/e-library
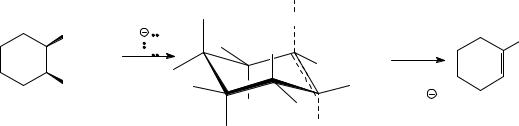
Задача 11. Изобразите механизм реакции цис-1-изопропил-
2-хлорциклогексана с гидроксидом калия в этаноле при нагревании. Сравните скорость этой реакции со скоростью аналогичной реакции для транс-1-изопропил-2- хлорциклогексана. Ответ обоснуйте.
Данная реакция протекает по механизму бимолекулярного элиминирования (Е2). В переходном состоянии молекула исходного соединения должна принять конформацию, в которой связи с уходящими атомами хлора и водорода располагаются копланарно, т.е. в одной плоскости. Это возможно только тогда, когда и хлор, и атом водорода находятся на аксиальных связях. В случае цис-конфигурации это конформация «кресло» с аксиальным атомом хлора и экваториальной изопропильной группой (заметим кстати, что эта конформация энергетически наиболее выгодная). Из двух атомов водорода, которые располагаются на аксиальных связях у соседних атомов углерода, в переходном состоянии участвует именно тот, отщепление которого приводит к термодинамически наиболее устойчивому алкену (по правилу Зайцева).
|
|
|
|
|
|
|
OH |
|
|
CH(CH3)2 |
|
H |
CH(CH3)2 |
|
OH |
H |
|||
|
|
|||
Cl |
|
CH(CH3)2 _ |
|
|
|
|
|
||
|
|
_Cl |
||
Cl
переходное состояние
В переходном состоянии аналогичной реакции транс-1- изопропил-2-хлорциклогексана участвует энергетически наименее выгодная конформация, в которой оба заместителя – и хлор, и изопропил – располагаются на аксиальных связях. Поэтому энергия этого переходного состояния значительно выше, чем энергия переходного состояния в выше рассмотренном механизме для цис-изомера. Следовательно, скорость реакции транс-изомера должна быть намного меньше. Кроме того, продукт реакции не является продуктом элиминирования по правилу Зайцева, т.к. соответствующий этому правилу атом водорода у наименее гидрогенизированного атома углерода в переходном состоянии не располагается на аксиальной связи, по-
55
http://www.mitht.ru/e-library
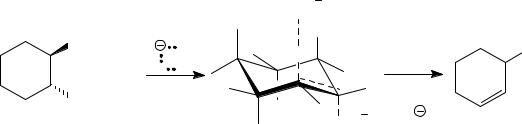
этому отщепляется атом водорода от наиболее гидрогенизированного атома углерода.
|
HO |
|
|
CH(CH3)2 |
CH(CH3)2 |
||
H |
|
CH(CH3)2 |
|
OH |
|
||
Cl |
|
|
_H O |
|
|
2 |
|
|
Cl |
|
_Cl |
|
|
|
|
переходное состояние
56
http://www.mitht.ru/e-library
Задача 12. Изобразите механизм и обоснуйте стереоселек-
тивность взаимодействия (S)-2-бром-1-фенилпропана с амидом натрия при нагревании.
Амид натрия является сильным основанием, которое при нагревании вызывает значительное преобладание реакции элиминирования. Поэтому для данной реакции необходимо изобразить механизм бимолекулярного элиминирования (Е2).
Реакции Е2 протекают как синхронный процесс разрыва и образования связей через переходное состояние, в котором должна реализоваться заторможенная конформация с анти- расположением уходящих атомов брома и водорода у соседних атомов углерода. Поскольку термическое элиминирование под действием небольших по объему оснований происходит региоселективно в соответствии с правилом Зайцева, то необходимо рассматривать конформации исходного соединения, образующиеся при вращении вокруг связи С(1)-С(2).
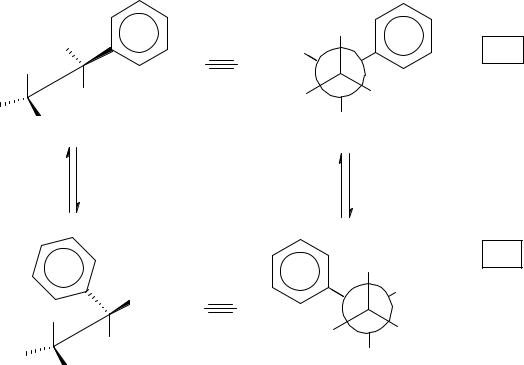
Сначала необходимо изобразить равновесие двух заторможенных конформаций с анти-расположенными атомами водорода и брома у соседних атомов, обращая внимание на конфигурацию хирального центра.
H |
H |
Br |
|
А |
|||
Br |
|||
|
|
||
H |
CH3 |
H |
|
CH3 |
|
H |
|
H |
|
||
|
|
Br Б
|
H |
H |
|
Br |
H |
|
CH3 |
|
CH3 |
H |
H |
H
В переходном состоянии элиминирования могут принимать участие обе конформации, но конформация А обладает меньшей энергией по сравнению с конформацией Б, т.к. в кон-
57
http://www.mitht.ru/e-library
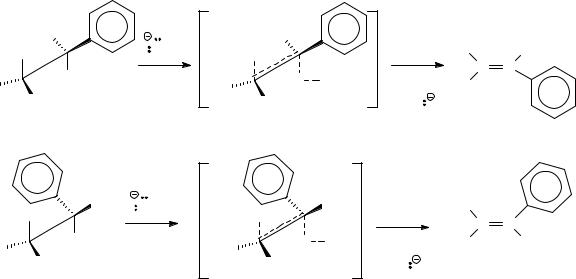
формации А имеется только одно гош-взаимодействие (между бромом и фенилом), а в Б – два (между бромом и фенилом и между фенилом и метилом). Поэтому переходное состояние с участием конформации А будет обладать меньшей энергией, и, следовательно, скорость дегидробромирования в этом случае будет больше.
|
H |
|
|
H |
|
|
|
|
|
|
|
NH2 |
|
|
|
|
CH3 |
H |
|
|
Br |
Br |
|
|
|
||||
|
H |
|
|
H |
|
|
_NH |
C |
C |
CH |
|
|
NH |
2 |
H |
|
|||
|
|
CH3 |
|
|
3 |
|
|||
3 |
H |
|
H |
|
|
_Br |
|
|
|
|
|
|
|
|
|
|
|||
H |
NH |
|
H |
|
CH3 |
|
Br |
2 |
Br |
|
|
C |
C |
H |
|
H |
|
_NH |
||
|
NH |
H |
H |
|||
CH3 |
|
CH3 |
2 |
3 |
|
|
H |
|
H |
|
_Br |
|
|
В результате будет образовываться больше (Е)-1- фенилпропена, чем (Z)-1-фенилпропена.
58
http://www.mitht.ru/e-library
Задача 13. Изобразите механизм реакции пара-
бромэтилбензола с амидом натрия при нагревании. Какой продукт является главным? Ответ обоснуйте.
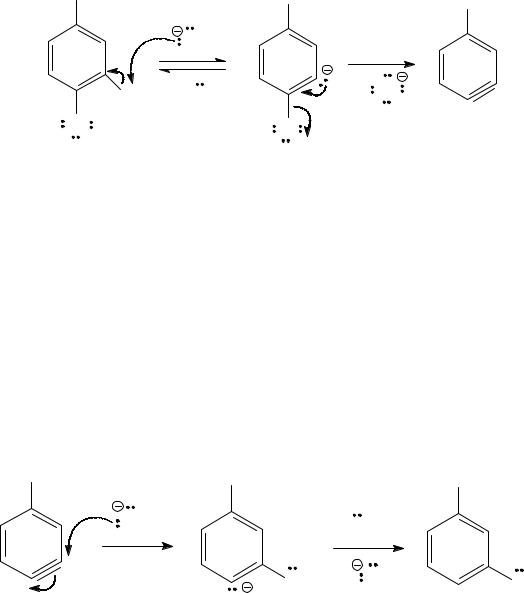
Арилгалогениды, не имеющие в ароматическом кольце электроноакцепторных заместителей, в жестких условиях реагируют с нуклеофилами, являющимися сильными основаниями, по ариновому механизму, протекающему как отщепление – присоединение.
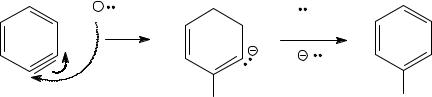
Сначала под действием амид-аниона как сильного основания происходит элиминирование бромоводорода с образованием арина (I).
C2H5 |
C2H5 |
C2H5 |
NH2 |
|
|
H _ NH3 |
|
_ Br |
Br |
Br |
|
I
Арины являются чрезвычайно неустойчивыми соединениями, которые легко реагируют с нуклеофилами. В результате присоединения амид-аниона к арину (I) могут образоваться два аниона (II) и (III). В арил-анионах неподеленная электронная пара находится на орбитали, лежащей в плоскости ароматического кольца, так что заряд не может быть делокализован за счет сопряжения. Поскольку неподеленная пара локализована, стабильность арил-аниона зависит от влияния положительного индуктивного эффекта этильной группы: чем этот заместитель ближе к отрицательно заряженному атому, тем сильнее его +I- эффект дестабилизирует анион.
C2H5 |
C2H5 |
C H |
|
|
|
2 |
5 |
|
NH2 |
NH3 |
|
|
NH2 |
_ NH |
NH |
|
2 |
||
|
|
|
2 |
II
59
http://www.mitht.ru/e-library
C2H5 |
|
C2H5 |
C2H5 |
|||
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|



 NH2
NH2  NH3
NH3
_  NH2
NH2
 NH2
NH2  NH2
NH2
III
Следовательно, менее дестабилизированным является анион II, из которого взаимодействием с аммиаком как донором протонов и образуется главный продукт реакции – мета- этиланилин. Из аниона III образуется второй продукт – пара- этиланилин.
60
http://www.mitht.ru/e-library
