
- •Іv галогеновуглеводні
- •2 Ізомерія
- •3 Фізичні властивості
- •4 Хімічні властивості
- •Вплив деяких чинників на реакційну здатність галогеновуглеводнів
- •Вінілхлорид Перехідний стан Ацетальдегід
- •2 Реакції sn із Карбонвмісними нуклеофілами
- •3 Реакції sn з Нітрогенвмісними нуклеофілами.
- •4 Реакції sn з Галогеновмісними нуклеофілами
- •5 Реакції sn із Сульфурвмісними нуклеофілами
- •Іі Реакції елімінування.
- •Конкурентність реакцій нуклеофільного заміщення та елімінування
- •IV Реакції вуглецевого ланцюгу
- •5 Способи добування
- •IV Одержання гемінальних дигалогенпохідних із карбонільних сполук:
- •V Одержання із карбоксилатів.
- •VI Одержання йодопохідних.
- •VII Одержання фторовуглеводнів
- •6 Використання галогеновуглеводнів
Іі Реакції елімінування.
Іншим характерним типом реакцій для галогенопохідних є реакції елімінування, які у даному випадку належать до процесів дегідрогалогенування, оскільки від молекули галогенопохідного субстрата відщеплюються одночасно атоми галогену і Гідрогену.
Залежно від взаємного розташування відщеплених атомів реакції елімінування поділяються на три типи.
-Елімінування, при якому атоми Hal і Н під дією сильної основи відщеплюються від одного атома Карбону, внаслідок чого утворюються карбени – молекули, що містять атом Карбону з неподіленою електронною парою. За рахунок цієї пари електронів карбени виявляють себе сильними електрофілами з великою реакційною здатністю, що використовується в деяких специфічних процесах органічного синтезу. Прикладом -елімінування може бути реакція утворення карбену при взаємодії хлороформу із спиртовим розчином лугу:
CH3Cl + NaOH ------------ :CCl2 + NaCl + H2O
Хлороформ спирт Дихлоркарбен

 -Елімінування,
при якому дегідрогалогенування проходить
по 1.3-положенням і утворюється тричленний
цикл:
-Елімінування,
при якому дегідрогалогенування проходить
по 1.3-положенням і утворюється тричленний
цикл:
-С—С—С-- -------- + HHal

H Hal
Ці реакції не мають практичного значення. Вони технічно складні, оскільки реакційні центри віддалені один від одного і взаємний вплив атомів послаблений.
-Елімінування – найважливіший з усіх типів дегідрогалогенування, який застосовується при добуванні алкенів:



 -С—С—
--------
С==С + HHal
-С—С—
--------
С==С + HHal
H Hal
Далі ми будемо розглядати саме -елімінування, тому символ опустимо.
У реакціях дегідрогалогенування нуклеофіл, який одночасно є основою, витісняє галоген і відщеплює протон від С-Н-кислотного центра. Зрозуміло, що для відривання протону від С–Н необхідна сильна основа, тому звичайно застосовують алкоксид-іони (R–О-) у середовищі відповідного спирту (R-OH) чи концентровані спиртові розчини лугів:
СН2-СН2 + (СН3)3СОК --------------- CH2=CH + (CH3)3C(OH) + KBr
(CH3)3COH
H Br
Брометан Третбутанолят Етен Третбутиловий
 калію
спирт
калію
спирт

+ NaOH (конц) --------------- + NaBr + H2O
C2H5OH
Бромциклогексан Циклогексен
У випадку несиметричних галогеновуглеводнів необхідно брати до уваги правило Зайцева:
у реакціях дегідрогалогенування атом Гідрогену відщеплюється переважно від сусіднього найменш гідрогенізованого атома Карбону.
Наприклад:
СН3-CHBr-CH2-CH3 + NaOH(конц) -------------- CH3-CH=CH-CH3 + NaBr + H2O
2-Бромбутан С2Н5ОН Бутен-2
Механізм мономолекулярного елімінування Е1 реалізується при дегідрогалогенуванні третинних галогеновуглеводнів і окремих вторинних галогенопохідних, які містять обємні замісники поруч із реакційним центром, а також при використанні неконцентрованих основ (у схемах реакції основа позначається :В – від англ. Base – основа). Механізм складається з двох стадій. Перша – лімітуюча. Вона протікає повільно і визначає загальну швидкість реакції. Протягом першої стадії відбувається відщеплення галогену і утворення карбкатіона:

+
+


 --С—С--
--С—С + Х-
--С—С--
--С—С + Х-
Н Х Н
Галогенопохідне Карбкатіон
Друга стадія – швидка атака основою: В атома Гідрогену, сполученого з -атомом Карбону, і утворення подвійного звязку
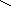
 +
+



 --С—С
С==С + ВН+
--С—С
С==С + ВН+


 Н
Н
В:
Реакційна здатність галогенопохідних у реакціях за механізмом Е1 зменшується при переході від третинних алкилгалогенідів до вторинних. Оскільки швидкість реакції визначається головним чином концентрацією тільки однієї речовини – субстрата галогеновуглеводню, то реакція належить до мономолекулярних.
Механізм бімолекулярного елімінування Е2 характерний для первинних галогеновуглеводнів, а також для вторинних галогенопохідних з невеликими замісниками біля реакційних центрів. Швидкість реакції за механізмом Е2 залежить від концентрації обох реагентів – галогенопохідного субстрата і основи, тому належить до бімолекулярних.
Механімз складається з однієї стадії, під час якої основа відриває протон від С-Н-кислотного центра і одночасно витісняє нуклеофуг – галогенід-іон. Реакція протікає сінхронно, через перехідний стан, наприклад:


CH3 CH3 CH3 CH3
(СН3)3СО- + Н—С—СН—Br ------------- (CH3)3CO----H----C----CH----Br --------
CH3 CH3
Третбутанолят 2-Бром—3метилбутан Перехідний стан
CH3
--------- CH3—C—OH + CH3—C==CH—CH3 + Br-
CH3 CH3
Третбутиловий 2-Метилбутен-2
спирт
