
- •6. Четвертичная структура белков
- •1. Различия белков по форме молекул
- •2. Различия белков по молекулярной массе
- •5. Растворимость белков
- •9. Классификация белков
- •1. Простые белки
- •2. Сложные белки
- •1. Ферменты
- •2. Регуляторные белки
- •3. Рецепторные белки
- •4. Транспортные белки
- •5. Структурные белки
- •6. Защитные белки
- •7. Сократительные белки
- •1. Субстратная специфичность
- •2. Каталитическая специфичность
- •13. Кофакторы
- •1. Роль металлов в присоединении субстрата в активном центре фермента
- •2. Роль металлов в стабилизации третичной и четвертичной структуры фермента
- •3. Роль металлов в ферментативном катализе
- •Витамин рр (Никотиновая кислота)
- •14.Строение ферментов.
- •15.Ингибирование активности фермнтов.
- •1. Конкурентное ингибирование
- •16. Аллостерическая регуляция
- •17.Регуляция каталитической активности ферментов
- •18Кинетика ферментативных реакций.
- •19.Классификация и номенклатура ферментов
- •1. Оксидоредуктазы
- •5. Изомеразы
- •20.Эндерганические и экзерганические реакции в живой клетке.
- •21.Строение митохондрийи структурная организация дыхательной цепи.
- •22.Окислительное фосфорилирование
- •23.Биохимия питания.
- •24.Витамины.
- •25.Катаболизм основных пищевых веществ.
- •26.Окислительное декарбоксилирование пвк Окислительное декарбоксилирование пировиноградной кислоты
- •28Цикл лимонной кислоты.
- •27Цтк схема Регуляция цикла
- •29.Основные углеводы животных.
- •30.Аэробный гликолиз.
- •31.Биосинтез глюкозы.
- •32.Гликоген.
- •33.Анаэробный гликолиз.
- •34.Липиды
- •35.Переваривание липидов пищи.
- •36.Депонирование и мобилизация.
- •Депонирование жиров в жировой ткани
- •37.Распад жирных кислот в клетке.
- •38.Кетоновые тела
- •39.Биосинтез жирных кислот.
- •40Холестерол
- •41Липопротеины
- •42.Липидный состав.
- •43.Биологические мембраны.
- •44.Механизм переноса веществ через мембрвну
- •53.Декарбоксилирование аминокислот
- •54.Биосинтез гемма.
- •55.Распад гемма.
- •58.Происхождение атомов.
17.Регуляция каталитической активности ферментов
В биологических системах часто встречается механизм регуляции активности ферментов с помощью ковалентной модификации аминокислотных остатков. Быстрый и широко распространённый способ химической модификации ферментов - фосфорилирование/дефосфорилирование. Фос-форилирование осуществляется ферментами протеинкиназами, а дефосфорилирование - фосфопротеинфосфатазами. Присоединение остатка фосфорной кислоты приводит к изменению конформации активного центра и его каталитической активности. При этом результат может быть двояким: одни ферменты при фосфорилировании активируются, другие, напротив, становятся менее активными. Изменение активности фермента, вызванное фосфорилированием, обратимо. Например, под действием глюкагона (в период между приёмами пищи) в клетках происходит уменьшение синтеза энергетического материала - жира, гликогена и усиление его распада (мобилизация), вызванного фосфо-рилированием ключевых ферментов этих процессов
18Кинетика ферментативных реакций.
Ферментативная кинетика занимается исследованием закономерностей влияния химической природы реагирующих веществ (ферментов, субстратов) и условий их взаимодействия (концентрация, рН среды, температуры, присутствие активаторов или ингибиторов) на скорость ферментативной реакции. Главной целью изучения кинетики ферментативных реакций является получение информации, которая может способствовать выяснению молекулярного механизма действия фермента.
19.Классификация и номенклатура ферментов
Каждый фермент имеет 2 названия. Первое - короткое, так называемое рабочее, удобное для повседневного использования. Второе (более полное) - систематическое, применяемое для однозначной идентификации фермента.
А. Рабочее название
В названии большинства ферментов содержится суффикс "аза", присоединённый к названию субстрата реакции, например уреаза, сахараза, липаза, нуклеаза
Классы ферментов
систематическую номенклатуру, согласно которой все ферменты разбиты на 6 основных классов в зависимости от типа катализируемой химической реакции.
1. Оксидоредуктазы
Катализируют различные окислительно-восстановительные реакции с участием 2 субстратов (перенос е- или атомов водорода с одного субстрата на другой).
Дегидрогеназы. В этот подкласс входят ферменты, катализирующие реакции дегидрирования (отщепления водорода). В качестве акцепторов электронов используются коферменты NAD+, NADP+, FAD, FMN (см. ниже). Все ферменты этой группы обладают высокой субстратной специфичностью. Пример реакции:

2.Трансферты
Катализируют перенос функциональных групп от одного соединения к другому. Подразделяют в зависимости от переносимой группы.
Наименование
ферментов составляют по формуле
"субстрат-гидролаза" или прямым
присоединением к названию субстрата
суффикса "аза", например протеаза,
липаза, фосфолипаза, рибо-нуклеаза.
Пример реакции
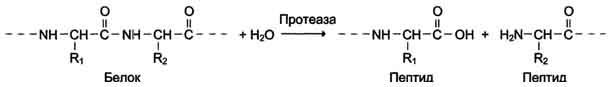
4. Лиазы
К лиазам относят ферменты, отщепляющие от субстратов негидролитическим путём определённую группу (при этом могут отщепляться СО2, Н2О, NH2,SН2и др.) или присоединяющие чаще всего молекулу воды по двойной связи.

